早教吧作业答案频道 -->化学-->
水是地球表面上普遍存在的化合物,我们可以用我们学习的物质结构与性质的有关知识去认识它.(1)水的组成元素为氢和氧.氧的基态原子的价电子排布图为,氧的第一电离能在同周期
题目详情
水是地球表面上普遍存在的化合物,我们可以用我们学习的物质结构与性质的有关知识去认识它.
(1)水的组成元素为氢和氧.氧的基态原子的价电子排布图为___,氧的第一电离能在同周期元素中由大到小排第___位.
(2)根据杂化轨道理论,水分子中的氧原子采取的杂化形式是___;根据价层电子对互斥理论,水分子的VSEPR模型名称为___;根据等电子体原理,写出水合氢离子的一个等电子体(写结构式)___.
(3)水分子可以形成许多水合物.
①水分子可以作配体和铜离子形成水合铜离子[Cu(H2O)4]2+,1mol水合铜离子中含有σ键数目为___.
②图1是水合盐酸晶体H5O2+•Cl-中H5O2+离子的结构.
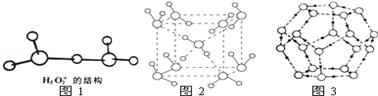
在该离子中,存在的作用力有___.
a.配位键 b.极性键 c.非极性键 d.离子键 e.金属键 f.氢键 g.范德华力 h.π键 i.σ键
(4)韩国首尔大学科学家将水置于一个足够强的电场中,在20℃时,水分子瞬间凝固形成了“暖冰”.请从结构上解释生成暖冰的原因___.
(5)最新研究发现,水能凝结成13种类型的结晶体,除普通冰以外其余各自的冰都有自己奇特的性质:有在-30℃才凝固的超低温冰,它的坚硬程度可和钢相媲美,能抵挡炮弹轰击;有在180℃高温下依然不变的热冰;还有的冰密度比水大,号称重冰.图2为冰的一种骨架形式,依此为单位向空间延伸.
①该冰中的每个水分子有___个氢键;
②冰融化后,在液态水中,水分子之间仍保留有大量氢键将水分子联系在一起,分子间除了无规则的分布及冰结构碎片以外,一般认为还会有大量呈动态平衡的、不完整的多面体的连接方式.右图的五角十二面体是冰熔化形成的理想多面体结构.假设图2中的冰熔化后的液态水全部形成如图3的五角十二面体,且该多面体之间无氢键,则该冰熔化过程中氢键被破坏的百分比为___.
③如果不考虑晶体和键的类型,哪一物质的空间连接方式与这种冰连接类似?___;
④已知O-H…O距离为295pm,列式计算此种冰晶体的密度___g/cm3.
(已知2952=8.70×104,2953=2.57×107,
=1.41,
=1.73)
(1)水的组成元素为氢和氧.氧的基态原子的价电子排布图为___,氧的第一电离能在同周期元素中由大到小排第___位.
(2)根据杂化轨道理论,水分子中的氧原子采取的杂化形式是___;根据价层电子对互斥理论,水分子的VSEPR模型名称为___;根据等电子体原理,写出水合氢离子的一个等电子体(写结构式)___.
(3)水分子可以形成许多水合物.
①水分子可以作配体和铜离子形成水合铜离子[Cu(H2O)4]2+,1mol水合铜离子中含有σ键数目为___.
②图1是水合盐酸晶体H5O2+•Cl-中H5O2+离子的结构.

在该离子中,存在的作用力有___.
a.配位键 b.极性键 c.非极性键 d.离子键 e.金属键 f.氢键 g.范德华力 h.π键 i.σ键
(4)韩国首尔大学科学家将水置于一个足够强的电场中,在20℃时,水分子瞬间凝固形成了“暖冰”.请从结构上解释生成暖冰的原因___.
(5)最新研究发现,水能凝结成13种类型的结晶体,除普通冰以外其余各自的冰都有自己奇特的性质:有在-30℃才凝固的超低温冰,它的坚硬程度可和钢相媲美,能抵挡炮弹轰击;有在180℃高温下依然不变的热冰;还有的冰密度比水大,号称重冰.图2为冰的一种骨架形式,依此为单位向空间延伸.
①该冰中的每个水分子有___个氢键;
②冰融化后,在液态水中,水分子之间仍保留有大量氢键将水分子联系在一起,分子间除了无规则的分布及冰结构碎片以外,一般认为还会有大量呈动态平衡的、不完整的多面体的连接方式.右图的五角十二面体是冰熔化形成的理想多面体结构.假设图2中的冰熔化后的液态水全部形成如图3的五角十二面体,且该多面体之间无氢键,则该冰熔化过程中氢键被破坏的百分比为___.
③如果不考虑晶体和键的类型,哪一物质的空间连接方式与这种冰连接类似?___;
④已知O-H…O距离为295pm,列式计算此种冰晶体的密度___g/cm3.
(已知2952=8.70×104,2953=2.57×107,
| | 2 |
| | 3 |
▼优质解答
答案和解析
(1)由于简并轨道(能级相同的轨道)中电子优先单独占据1个轨道,且自旋方向相同,原子的能量最低,O原子能量最低排布是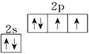 ;
;
同一周期内主族元素的第一电离能从左到右在总体增大的趋势中有些曲折.当外围电子在能量相等的轨道上形成全空、半满或全满结构时,原子的能量较低,元素的第一电离能较大,由于N元素的2p能级3个轨道处于半满,He元素的2P能级3个轨道处于全满,所以它们的第一电离能大小顺序是I1(He)>I1(F)>I1(N)>I1(O)>I1(C)>I1(Be)>I1(B),
故答案为: ;4;
;4;
(2)H2O中价层电子对个数=2+
(6-2×1)=4,且含有2个孤电子对,所以H2O的VSEPR模型为四面体,分子空间构型为V型,中心原子杂化方式为sp3,H3O+中O原子的质子数为8,H原子的质子数为1,所以H3O+的质子数为11,电子数=11-1=10,NH3的原子数目为4,电子数目为10,则与H3O+互为等电子体,结构式为: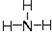 ,
,
故答案为:sp3;四面体形;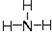 ;
;
(3)①Cu2+含有空轨道,H2O含有孤对电子,可形成配位键,铜离子配体数为4,配离子[Cu(H2O)4]2+中1个Cu2+与4个H2O形成配位键,1个H2O含2个O-H键,所以1mol水合铜离子中含有σ键数目为12NA,
故答案为:12NA;
②根据图1水合盐酸晶体H5O2+•Cl-中H5O2+离子的结构知:
a.氢离子含有空轨道,氧原子含有孤电子对,所以能形成配位键;
b.O-H形成极性键;
c.无非极性键;
d.因H5O2+中无阴阳离子,所以不存在离子键;
e.因H5O2+中无金属所以不存在金属键;
f.氢键存在于不直接相连的H与电负性较大的O原子间;
g.因H5O2+中无分子,所以不存在范德华力;
h.因H5O2+中无双键或三键,所以不存在π键;
i.O-H形成σ键,
故答案为:a b f i;
(4)水分子之间主要通过氢键形成固体,水分子是极性分子,在电场作用下定向有规则的排列,水分子间更易形成氢键,
故答案为:水分子是极性分子,在电场作用下定向有规则的排列,分子间通过氢键结合而成固体;
(5)①晶体冰中,每两个水分子间有一个氢键,平均属于每个水分子有半个,一个水分子与周围的四个水分子以氢键结合,故1mol冰中有2 mol氢键,
故答案为:2;
②冰融化为液态水时,水分子数目不变,图2中每个水分子平衡含有氢键数目为4×
=2,图3中每个水分子平衡含有氢键数目为3×
=1.5,则该冰熔化过程中氢键被破坏的百分比为
×100%=25%,
故答案为:25%;
③二氧化硅是原子晶体,Si-O通过共价键形成四面体结构,四面体之间通过共价键形成空间网状结构,以立方体中的水分子为研究对象,每个水分子形成4条氢键,SiO2空间连接方式与这种冰连接类似,
故答案为:SiO2;
④体心立方晶胞中水分子个数=1+8×
=2;设体心立方中晶胞的棱长为X,O-H…O距离为A,则3X2=(2A)2,体心立方的密度ρ=
=
g/cm3=1.51g/cm3;
故答案为:
=1.51.
 ;
;同一周期内主族元素的第一电离能从左到右在总体增大的趋势中有些曲折.当外围电子在能量相等的轨道上形成全空、半满或全满结构时,原子的能量较低,元素的第一电离能较大,由于N元素的2p能级3个轨道处于半满,He元素的2P能级3个轨道处于全满,所以它们的第一电离能大小顺序是I1(He)>I1(F)>I1(N)>I1(O)>I1(C)>I1(Be)>I1(B),
故答案为:
 ;4;
;4;(2)H2O中价层电子对个数=2+
| 1 |
| 2 |
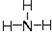 ,
,故答案为:sp3;四面体形;
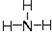 ;
;(3)①Cu2+含有空轨道,H2O含有孤对电子,可形成配位键,铜离子配体数为4,配离子[Cu(H2O)4]2+中1个Cu2+与4个H2O形成配位键,1个H2O含2个O-H键,所以1mol水合铜离子中含有σ键数目为12NA,
故答案为:12NA;
②根据图1水合盐酸晶体H5O2+•Cl-中H5O2+离子的结构知:
a.氢离子含有空轨道,氧原子含有孤电子对,所以能形成配位键;
b.O-H形成极性键;
c.无非极性键;
d.因H5O2+中无阴阳离子,所以不存在离子键;
e.因H5O2+中无金属所以不存在金属键;
f.氢键存在于不直接相连的H与电负性较大的O原子间;
g.因H5O2+中无分子,所以不存在范德华力;
h.因H5O2+中无双键或三键,所以不存在π键;
i.O-H形成σ键,
故答案为:a b f i;
(4)水分子之间主要通过氢键形成固体,水分子是极性分子,在电场作用下定向有规则的排列,水分子间更易形成氢键,
故答案为:水分子是极性分子,在电场作用下定向有规则的排列,分子间通过氢键结合而成固体;
(5)①晶体冰中,每两个水分子间有一个氢键,平均属于每个水分子有半个,一个水分子与周围的四个水分子以氢键结合,故1mol冰中有2 mol氢键,
故答案为:2;
②冰融化为液态水时,水分子数目不变,图2中每个水分子平衡含有氢键数目为4×
| 1 |
| 2 |
| 1 |
| 2 |
| 2-1.5 |
| 2 |
故答案为:25%;
③二氧化硅是原子晶体,Si-O通过共价键形成四面体结构,四面体之间通过共价键形成空间网状结构,以立方体中的水分子为研究对象,每个水分子形成4条氢键,SiO2空间连接方式与这种冰连接类似,
故答案为:SiO2;
④体心立方晶胞中水分子个数=1+8×
| 1 |
| 8 |
| 2m |
| NA×X3 |
| 18×2 | ||||
(
|
故答案为:
| 18×2 | ||||
(
|
看了水是地球表面上普遍存在的化合物...的网友还看了以下:
二年级的孩子英语不好,暑假有必要去补习吗?我小孩二年级英语太差,我想利用暑假给报个补习班,担心三年 2020-06-10 …
英语翻译该同学在我公司实习期间表现优秀,严格遵守公司各项规章制度,对待工作认真负责,与同事相处融洽 2020-06-28 …
如图,同是一次春游,同学们各有不同的收获。下列说法错误的是()A.学习仅仅局限在学校B.我们所看, 2020-07-07 …
英语翻译鉴于XXX身边的同学、我的同事以及我本人对他(XXX)都有很高的评介,我真诚的向贵校推荐他 2020-07-12 …
英语翻译我是一个非常有责任感和团队意识的人,并且具有吃苦耐劳精神,踏实认真、上进负责,能有效的解决 2020-07-20 …
下列说法正确的是()A.初中学习是我们终身学习的重要基础,只要学习成绩优秀,未来一定能取得成功B. 2020-07-25 …
写出句子中带点字词的意思那节大字课的前半堂我净和同座的同学说悄悄话了.在这方面田老师培育了我,给我开 2020-11-07 …
“减负”后,对学生的学习能力提出了新的要求。我们要经常进行合作学习,在小组中为了完成共同的任务,每个 2020-12-01 …
我们中学生通过思品学科的学习,锻炼了我们的各种混合思维能力。无论是逻辑思维能力还是发散思维能力都能得 2020-12-07 …
我接下来该怎么去做?我有一个非常要好的朋友,也是同班同学,我们无话不说,只是后来我跟她表白后我们就开 2021-01-12 …