早教吧作业答案频道 -->化学-->
黄铁矿(主要成分为FeS2)的利用对资源和环境具有重要意义.(1)工业上煅烧黄铁矿可制取SO2.已知下列热化学方程式4FeS2(s)+11O2(g)═2Fe2O3(s)+8SO2(g)△H=akJ/molS(s)+O2(g)═SO2(g
题目详情
黄铁矿(主要成分为FeS2)的利用对资源和环境具有重要意义.
(1)工业上煅烧黄铁矿可制取SO2.已知下列热化学方程式
4FeS2(s)+11O2(g)═2Fe2O3(s)+8SO2(g)△H=akJ/mol
S(s)+O2(g)═SO2(g)△H=bkJ/mol
Fe(s)+2S(s)═FeS2(s)△H=ckJ/mol
则4Fe(s)+3O2(g)=2Fe2O3(s)△H=___kJ/mol
(2)一种酸性条件下催化氧化黄铁矿的物质转化关系如图I所示.
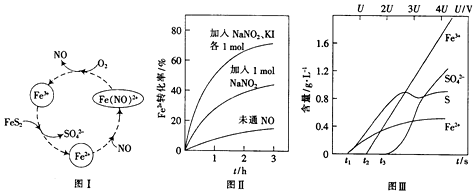
(1)写出图1中Fe3+与FeS2反应的离子方程式:___.
(2)硝酸也可将FeS2氧化为Fe3+和SO42-,使用浓硝酸比使用稀硝酸反应速率慢,其原因是___.
(3)控制Fe2+的浓度、溶液体积和通入O2的速率一定,图II所示为改变其他条件时Fe2+被氧化的转化率随时间的变化.
①加入NaNO2发生反应:2H++3NO2-═NO3-+2NO+H2O.若1mol NaNO2完全反应则转移电子的数目为___mol.
②加入NaNO2、KI发生反应:4H++2NO2-+2I-═2NO+I2+2H2O.解释图II中该条件下能进一步提高单位时间内Fe2+转化率的原因:___.
(4)为研究FeS2作电极时的放电规律,以FeS2作阳极进行电解,由FeS2放电产生粒子的含量与时间、电压(U)的关系如图 III所示.
①写出t1至t2间FeS2所发生的电极反应式:___.
②当电压的值介于3U~4U之间,FeS2放电所得主要粒子为___.
(1)工业上煅烧黄铁矿可制取SO2.已知下列热化学方程式
4FeS2(s)+11O2(g)═2Fe2O3(s)+8SO2(g)△H=akJ/mol
S(s)+O2(g)═SO2(g)△H=bkJ/mol
Fe(s)+2S(s)═FeS2(s)△H=ckJ/mol
则4Fe(s)+3O2(g)=2Fe2O3(s)△H=___kJ/mol
(2)一种酸性条件下催化氧化黄铁矿的物质转化关系如图I所示.

(1)写出图1中Fe3+与FeS2反应的离子方程式:___.
(2)硝酸也可将FeS2氧化为Fe3+和SO42-,使用浓硝酸比使用稀硝酸反应速率慢,其原因是___.
(3)控制Fe2+的浓度、溶液体积和通入O2的速率一定,图II所示为改变其他条件时Fe2+被氧化的转化率随时间的变化.
①加入NaNO2发生反应:2H++3NO2-═NO3-+2NO+H2O.若1mol NaNO2完全反应则转移电子的数目为___mol.
②加入NaNO2、KI发生反应:4H++2NO2-+2I-═2NO+I2+2H2O.解释图II中该条件下能进一步提高单位时间内Fe2+转化率的原因:___.
(4)为研究FeS2作电极时的放电规律,以FeS2作阳极进行电解,由FeS2放电产生粒子的含量与时间、电压(U)的关系如图 III所示.
①写出t1至t2间FeS2所发生的电极反应式:___.
②当电压的值介于3U~4U之间,FeS2放电所得主要粒子为___.
▼优质解答
答案和解析
(1)①4FeS2(s)+11O2(g)═2Fe2O3(s)+8SO2(g)△H=akJ/mol
②S(s)+O2(g)═SO2(g)△H=bkJ/mol
③Fe(s)+2S(s)═FeS2(s)△H=ckJ/mol,①+4×③-8×②得,4Fe(s)+3O2(g)=2Fe2O3(s)△H=(a+4c-8b)kJ/mol,
故答案为:a+4c-8b;
(1)Fe3+与FeS2反应生成Fe2+与SO4-和H+,故离子方程式为14Fe3++FeS2+8H2O=15Fe2++2SO4-+16H+,
故答案为:14Fe3++FeS2+8H2O=15Fe2++2SO4-+16H+;
(2)硝酸比使用稀硝酸反应速率慢,其原因是稀硝酸反应后被还原为NO,浓硝酸被还原为NO2,NO可作催化剂,NO2不能,
故答案为:稀硝酸反应后被还原为NO,浓硝酸被还原为NO2,NO可作催化剂,NO2不能;
(3)①2H++3NO2-═NO3-+2NO+H2O~2mole-
3 2
1
,
故答案为:
;
②图II中该条件下能进一步提高单位时间内Fe2+转化率的原因是生成的催化剂NO更多,加快了反应速率,
故答案为:生成的催化剂NO更多,加快了反应速率;
(4)①FeS2失电子发生氧化反应,故电极方程式FeS2-2e-=Fe2++2S,
故答案为:FeS2-2e-=Fe2++2S;
②据图象分析,介于3U~4U之间,FeS2放电所得主要粒子为Fe3+、SO42-,
故答案为:Fe3+、SO42-.
②S(s)+O2(g)═SO2(g)△H=bkJ/mol
③Fe(s)+2S(s)═FeS2(s)△H=ckJ/mol,①+4×③-8×②得,4Fe(s)+3O2(g)=2Fe2O3(s)△H=(a+4c-8b)kJ/mol,
故答案为:a+4c-8b;
(1)Fe3+与FeS2反应生成Fe2+与SO4-和H+,故离子方程式为14Fe3++FeS2+8H2O=15Fe2++2SO4-+16H+,
故答案为:14Fe3++FeS2+8H2O=15Fe2++2SO4-+16H+;
(2)硝酸比使用稀硝酸反应速率慢,其原因是稀硝酸反应后被还原为NO,浓硝酸被还原为NO2,NO可作催化剂,NO2不能,
故答案为:稀硝酸反应后被还原为NO,浓硝酸被还原为NO2,NO可作催化剂,NO2不能;
(3)①2H++3NO2-═NO3-+2NO+H2O~2mole-
3 2
1
| 2 |
| 3 |
故答案为:
| 2 |
| 3 |
②图II中该条件下能进一步提高单位时间内Fe2+转化率的原因是生成的催化剂NO更多,加快了反应速率,
故答案为:生成的催化剂NO更多,加快了反应速率;
(4)①FeS2失电子发生氧化反应,故电极方程式FeS2-2e-=Fe2++2S,
故答案为:FeS2-2e-=Fe2++2S;
②据图象分析,介于3U~4U之间,FeS2放电所得主要粒子为Fe3+、SO42-,
故答案为:Fe3+、SO42-.
看了黄铁矿(主要成分为FeS2)的...的网友还看了以下:
我国启动一项涉及千家万户营养健康问题的“补铁工程”,卫生部已批准以酱油为食物载体,逐步开展补铁工程 2020-05-13 …
(16分)韩国矿产资源匮乏,科技和经济实力雄厚,汽车、造船工业十分发达。图中的浦项市有世界著名的钢 2020-05-14 …
城市①和④的钢铁工业都很发达,它们发展钢铁工业的共同有利条件是()A.靠近原料产地B.靠近消费市场 2020-05-14 …
工业生产为我们提供丰富多样的生活资料。我国工业部门齐全,轻重工业发展都较快。根据所学知识回答问题。 2020-05-14 …
有关印度的工业的分布叙述,错误的是[]A.印度是世界上最大的软件出口国B.钢铁工业是印度传统的工业 2020-05-14 …
读“工业区位因素的影响力随时间变化曲线图”,回答分别以甲、乙为主导因素的工业部门是A.长春的汽车工 2020-05-14 …
工业生产为我们提供丰富多样的生活资料.我国工业部门齐全,轻重工业发展都较快.根据所学知识回答l8- 2020-05-14 …
读“长江沿江地带钢铁工业中心分布图”,完成下列要求.(1)填出图中英文字母所代表的钢铁工业基地.A 2020-05-14 …
读“长江沿江地带钢铁工业中心分布图”,完成下列要求.(1)填出图中英文字母所代表的钢铁工业基地.A 2020-05-14 …
读“长江沿江地带钢铁工业中心分布图”,完成下列要求.(1)填出图中英文字母所代表的钢铁工业基地.A 2020-05-14 …