早教吧作业答案频道 -->化学-->
观察如图装置,回答下列问题:(1)装置C中Pb上发生的电极反应方程式为.(2)若装置E的目的是在Cu材料上镀银,则极板N的材料为,X溶液为.(3)当装置A中Cu电极质量改变0.32g时,
题目详情
观察如图装置,回答下列问题:
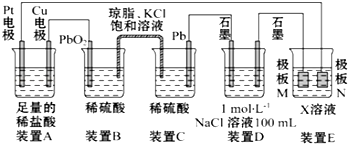
(1)装置C中Pb上发生的电极反应方程式为___.
(2)若装置E的目的是在Cu材料上镀银,则极板N的材料为___,X溶液为___.
(3)当装置A中Cu电极质量改变0.32g时,常温下装置D溶液的PH为___(设装置D电解过程产生的气体完全逸出,且溶液体积不变).
(4)垃圾渗滤液中含有大量的氨氮物质(用NH3表示)和氯化物,把垃圾渗滤液加入到装置E的电解池(M、N电极为惰性材料)进行电解除去NH3,净化污水.该净化过程分两步:第一步电解产生氧化剂,第二步氧化剂氧化氨氮物质生成N2.
①写出电解时N极的电极反应式:___.
②写出第二步反应的化学方程式:___.

(1)装置C中Pb上发生的电极反应方程式为___.
(2)若装置E的目的是在Cu材料上镀银,则极板N的材料为___,X溶液为___.
(3)当装置A中Cu电极质量改变0.32g时,常温下装置D溶液的PH为___(设装置D电解过程产生的气体完全逸出,且溶液体积不变).
(4)垃圾渗滤液中含有大量的氨氮物质(用NH3表示)和氯化物,把垃圾渗滤液加入到装置E的电解池(M、N电极为惰性材料)进行电解除去NH3,净化污水.该净化过程分两步:第一步电解产生氧化剂,第二步氧化剂氧化氨氮物质生成N2.
①写出电解时N极的电极反应式:___.
②写出第二步反应的化学方程式:___.
▼优质解答
答案和解析
(1)B和C装置形成原电池,铅作负极,二氧化铅作正极,原电池放电时,正极上二氧化铅得电子和硫酸根离子反应生成硫酸铅,发生还原反应,C装置中Pb上的电极反应式为:Pb-2e-+SO42-═PbSO4,
故答案为:Pb-2e-+SO42-═PbSO4;
(2)电镀时,镀层作阳极,镀件作阴极,电解质溶液中阳离子和镀层金属相同,若装置D的目的是在某镀件上镀银,则X为硝酸银溶液,N作阳极,应该是银,若装置E的目的是验证金属的电化学防腐,则极板N的材料为惰性电极(或石墨等不溶性惰性材料),被保护的金属连接电源阴极,
故答案为:Ag;AgNO3;
(3)当装置A中Cu电极质量改变0.32g时,n(Cu)=
=0.005mol,则转移了0.01mol电子,装置D中n(NaCl)=1mol/L×0.1L=0.1mol,阳极发生2Cl-2e-=Cl2↑,阴极发生2H++2e-=H2↑,消耗了0.01mol氢离子,则溶液中产生0.01mol氢氧根离子,氢氧根离子浓度为:
=0.1mmol/L,该溶液的pH=13,
故答案为:13;
(4)①根据图示知道:N电极是电解池的阳极,该电极上发生失电子的氧化反应,可以得到氧化剂,根据离子的放电顺序,即氯离子失电子产生氯气的过程,电极反应式为:2Cl--2e-=Cl2↑,
故答案为:2Cl--2e-=Cl2↑;
②第二步氧化剂氯气氧化氨氮物质即氨气生成N2的过程,发生的反应为:3Cl2+2NH3=N2+6HCl或3Cl2+8NH3=N2+6NH4Cl,
故答案为:3Cl2+2NH3=N2+6HCl或3Cl2+8NH3=N2+6NH4Cl.
故答案为:Pb-2e-+SO42-═PbSO4;
(2)电镀时,镀层作阳极,镀件作阴极,电解质溶液中阳离子和镀层金属相同,若装置D的目的是在某镀件上镀银,则X为硝酸银溶液,N作阳极,应该是银,若装置E的目的是验证金属的电化学防腐,则极板N的材料为惰性电极(或石墨等不溶性惰性材料),被保护的金属连接电源阴极,
故答案为:Ag;AgNO3;
(3)当装置A中Cu电极质量改变0.32g时,n(Cu)=
| 0.32g |
| 64g/mol |
| 0.01mol |
| 0.1L |
故答案为:13;
(4)①根据图示知道:N电极是电解池的阳极,该电极上发生失电子的氧化反应,可以得到氧化剂,根据离子的放电顺序,即氯离子失电子产生氯气的过程,电极反应式为:2Cl--2e-=Cl2↑,
故答案为:2Cl--2e-=Cl2↑;
②第二步氧化剂氯气氧化氨氮物质即氨气生成N2的过程,发生的反应为:3Cl2+2NH3=N2+6HCl或3Cl2+8NH3=N2+6NH4Cl,
故答案为:3Cl2+2NH3=N2+6HCl或3Cl2+8NH3=N2+6NH4Cl.
看了观察如图装置,回答下列问题:(...的网友还看了以下:
化学平衡状态题下列说法可以充分说明反应A(g)+B(g)=C(g)+D(g)达到平衡状态的是A反应 2020-04-26 …
在哪有5个音阶指型的应用,很多前辈说:mi型对应C调,si型对应F调,La型对应G调,Re型对应D 2020-05-16 …
英语中G-H-是什么意思我在查词时发现godn.C神G-上帝还有heaven.U常H-天堂,天国… 2020-06-04 …
已知A(g)+B(g)⇌C(g)+D(g)反应的平衡常数和温度的关系如下:|温度/℃7009008 2020-07-05 …
反应A(g)+B(g)═C(g)+D(g)过程中的能量变化如图所示,则下列说法正确的是()A.该反 2020-07-13 …
如图所示为800℃时A、B、C三种气体在密闭容器中反应时浓度的变化,只从图上分析不能得出的结论是( 2020-07-26 …
如果其他情况不变,净税收和政府购买增加同一数额时,则()。如果其他情况不变,净税收和政府购买增加同一 2020-11-17 …
家庭是我们成长的摇篮,学校是我们成长的温室,所以我们A.最好永远呆在家里B.最好一直留在学校里读书C 2020-11-22 …
遗传物质控制蛋白质合成的时候,氨基酸对应的密码子是DNA上的同步还是mRNA?DNA链碱基序列G-C 2020-12-21 …
(高二化学)下列反应中,在高温下不能自发进行的是(需要详解,谢谢!)A.CO(g)=C(g)+1/2 2020-12-24 …