早教吧作业答案频道 -->化学-->
粗铜精炼后的阳极泥含有Cu、Au(金)和PbSO4等杂质,湿法处理阳极泥进行综合利用的流程如图:(1)用CuSO4做电解液电解含铜、金、铅的粗铜,阳极的电极反应式有:Pb-2e-+SO42-=PbSO4和.(2
题目详情
粗铜精炼后的阳极泥含有Cu、Au(金)和PbSO4等杂质,湿法处理阳极泥进行综合利用的流程如图:
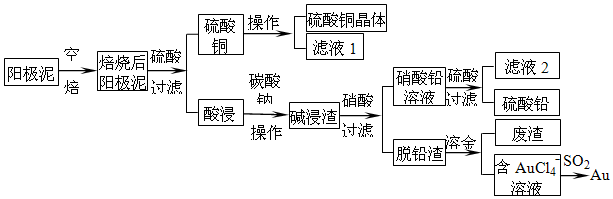
(1)用CuSO4做电解液电解含铜、金、铅的粗铜,阳极的电极反应式有:Pb-2e-+SO42-=PbSO4和___.
(2)碱浸渣的主要成分是___、___.(写化学式)
(3)操作I的主要步骤为___.
(4)写出用SO2还原AuCl4-的离子方程式___.
(5)为了减少废液排放、充分利用有用资源,工业上将滤液2并入硝酸进行循环操作,请指出流程图中另一处类似的做法___.
(6)已知298K时,Ksp(PbCO3)=1.5×10-13,Ksp(PbSO4)=1.8×10-8,将1mol PbSO4固体放入1L Na2CO3溶液中,充分反应后达到平衡,溶液中c(CO32-)为5mol/L,溶液体积在反应前后保持不变,则平衡后c(SO42-)=___.

(1)用CuSO4做电解液电解含铜、金、铅的粗铜,阳极的电极反应式有:Pb-2e-+SO42-=PbSO4和___.
(2)碱浸渣的主要成分是___、___.(写化学式)
(3)操作I的主要步骤为___.
(4)写出用SO2还原AuCl4-的离子方程式___.
(5)为了减少废液排放、充分利用有用资源,工业上将滤液2并入硝酸进行循环操作,请指出流程图中另一处类似的做法___.
(6)已知298K时,Ksp(PbCO3)=1.5×10-13,Ksp(PbSO4)=1.8×10-8,将1mol PbSO4固体放入1L Na2CO3溶液中,充分反应后达到平衡,溶液中c(CO32-)为5mol/L,溶液体积在反应前后保持不变,则平衡后c(SO42-)=___.
▼优质解答
答案和解析
由实验流程可知,粗铜精炼后的阳极泥含有Cu、Au(金)和PbSO4等杂质,焙烧后金属铜成为氧化铜,酸浸可以得到硫酸铜溶液,硫酸铜溶液经过蒸发浓缩,降温结晶,过滤、洗涤,干燥获得硫酸铜晶体;酸浸后的固体中含有Au(金)和PbSO4等杂质经碳酸钠浸洗,硫酸铅转化成碳酸铅,得碱浸渣为Au、PbCO3,浓硝酸氧化后,过滤得到硝酸铅溶液,滤液加硫酸生成硫酸铅沉淀,再过滤得到硫酸铅;脱铅滤渣主要是金,加王水溶金,得到含有AuCl4-的溶液,AuCl4-可以被SO2还原得到Au,
(1)电解精炼的粗铜作阳极会发生氧化反应,其中单质铜和活泼性比Cu强的金属都会发生溶解,因此粗铜中的铜和铅会发生失电子的氧化反应,电极反应式为Cu-2e-=Cu2+、Pb-2e-+SO42-=PbSO4,
故答案为:Cu-2e-=Cu2+;
(2)酸浸后的固体中含有Au(金)和PbSO4等杂质经碳酸钠浸洗,硫酸铅转化成碳酸铅,得碱浸渣为Au、PbCO3,
故答案为:Au、PbCO3;
(3)操作I的步骤是从硫酸铜溶液中获得硫酸铜晶体,因此该步骤是蒸发浓缩、冷却结晶、过滤、洗涤、干燥等步骤,故答案为:蒸发浓缩,降温结晶,过滤;
(4)SO2还原AuCl4-中还原剂和氧化剂都比较明确,因此很容易推测出氧化产物是SO42-,还原产物是Au,由氧化还原反应得失电子守恒先缺项配平,然后根据电荷守恒再配平,则得到的反应方程式为2AuCl4-+3SO2+6H2O=2Au+3SO42-+8Cl-+12H+,
故答案为:2AuCl4-+3SO2+6H2O=2Au+3SO42-+8Cl-+12H+;
(5)滤液1是在结晶硫酸铜时剩下的滤液,还含有少量的未析出的硫酸铜,因此并入前面的硫酸铜溶液进行循环,有利于充分利用,
故答案为:将滤液1并入CuSO4溶液中;
(6)将1mol PbSO4固体放入1L Na2CO3溶液中,溶液中c(SO42-)=1mol/L,根据Ksp(PbCO3)=c(CO32-)×c(Pb2+)=1.5×10-13和c(CO32-)=5 mol/L可知,溶液中的c(Pb2+)=3×10-14mol/L,再根据c(Pb2+)和Ksp(PbSO4)=c(SO42-)×c(Pb2+)可知,饱和溶液中c(SO42-)=
=6×105mol/L>1mol/L,所以溶液中的硫酸根离子没有沉淀,所以c(SO42-)=1mol/L,
故答案为:1mol/L.
(1)电解精炼的粗铜作阳极会发生氧化反应,其中单质铜和活泼性比Cu强的金属都会发生溶解,因此粗铜中的铜和铅会发生失电子的氧化反应,电极反应式为Cu-2e-=Cu2+、Pb-2e-+SO42-=PbSO4,
故答案为:Cu-2e-=Cu2+;
(2)酸浸后的固体中含有Au(金)和PbSO4等杂质经碳酸钠浸洗,硫酸铅转化成碳酸铅,得碱浸渣为Au、PbCO3,
故答案为:Au、PbCO3;
(3)操作I的步骤是从硫酸铜溶液中获得硫酸铜晶体,因此该步骤是蒸发浓缩、冷却结晶、过滤、洗涤、干燥等步骤,故答案为:蒸发浓缩,降温结晶,过滤;
(4)SO2还原AuCl4-中还原剂和氧化剂都比较明确,因此很容易推测出氧化产物是SO42-,还原产物是Au,由氧化还原反应得失电子守恒先缺项配平,然后根据电荷守恒再配平,则得到的反应方程式为2AuCl4-+3SO2+6H2O=2Au+3SO42-+8Cl-+12H+,
故答案为:2AuCl4-+3SO2+6H2O=2Au+3SO42-+8Cl-+12H+;
(5)滤液1是在结晶硫酸铜时剩下的滤液,还含有少量的未析出的硫酸铜,因此并入前面的硫酸铜溶液进行循环,有利于充分利用,
故答案为:将滤液1并入CuSO4溶液中;
(6)将1mol PbSO4固体放入1L Na2CO3溶液中,溶液中c(SO42-)=1mol/L,根据Ksp(PbCO3)=c(CO32-)×c(Pb2+)=1.5×10-13和c(CO32-)=5 mol/L可知,溶液中的c(Pb2+)=3×10-14mol/L,再根据c(Pb2+)和Ksp(PbSO4)=c(SO42-)×c(Pb2+)可知,饱和溶液中c(SO42-)=
| 1.8×10-8 |
| 3×10-14 |
故答案为:1mol/L.
看了粗铜精炼后的阳极泥含有Cu、A...的网友还看了以下:
直流电机换向极与主极的极性在电动机与发电机状况怎么不一样?电动机时:换向极极性与转向方向上主极极性相 2020-03-31 …
关于南北极极昼极夜的问题(1)极点一年是不是只有春分和夏至这两天不是极昼极夜,这两天极点状态是什么 2020-05-13 …
化合物V是中药黄芩中的主要活性成分之一,具有抗氧化和抗肿瘤作用。化合物V也可通过下图所示方法合成: 2020-06-24 …
CO和CO2的混合气体36g,完全燃烧后测得CO2的体积为22.4L(标准状况下).(1)求混合气 2020-06-27 …
(8分)铅蓄电池是最常见的二次电池,它是由两组平行排列的栅状铅合金极板作为主架,正极板上覆盖PbO 2020-06-28 …
含参函数取到极值后为什么要检验参数如:已知函数f(x)=lnx-1/2ax^2-2x,在x=2处取 2020-07-11 …
化学:Cu作为两个电极电解CuSO4时,电极会被氧化吗?为什么rt,如果不会,为什么?如果会,那么什 2020-10-31 …
关于原电池电极式1.铅蓄电池:(负极—Pb正极—PbO2电解液—稀硫酸)总化学方程式Pb+PbO2+ 2020-11-01 …
杂合子基因型为Aa,下列相关描述最能体现基因分离定律实质的是()A.杂合子自交后代表现型之比为3:1 2020-11-24 …
工地上堆放了一对搅拌好的三合土,呈圆锥形,工人叔叔测得底面周长约为120M,高是6M.π取31.请你 2020-12-30 …