早教吧作业答案频道 -->化学-->
某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验.Ⅰ.将NaOH溶液与NH4Cl溶液混合生成NH3•H2O,从而验证NaOH的碱性大于NH3•H2O继而可以验证Na的金属性大于N,你认为此设计是
题目详情
某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验.
Ⅰ.将NaOH溶液与NH4Cl溶液混合生成NH3•H2O,从而验证NaOH的碱性大于NH3•H2O继而可以验证Na的金属性大于N,你认为此设计是否合理?并说明理由:___.
Ⅱ.
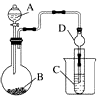
(1)利用图装置可以验证非金属性的变化规律.干燥管D的作用是___.
(2)实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属性大于硫:烧瓶中发生反应的离子方程式为___.
装置C中的实验现象为有淡黄色沉淀生成,离子方程式为___.
(3)若要用此装置证明酸性:H2CO3>H2SiO3进而证明非金属性:C>Si,则A中加___观察到C中溶液的现象为___.
Ⅰ.将NaOH溶液与NH4Cl溶液混合生成NH3•H2O,从而验证NaOH的碱性大于NH3•H2O继而可以验证Na的金属性大于N,你认为此设计是否合理?并说明理由:___.
Ⅱ.

(1)利用图装置可以验证非金属性的变化规律.干燥管D的作用是___.
(2)实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属性大于硫:烧瓶中发生反应的离子方程式为___.
装置C中的实验现象为有淡黄色沉淀生成,离子方程式为___.
(3)若要用此装置证明酸性:H2CO3>H2SiO3进而证明非金属性:C>Si,则A中加___观察到C中溶液的现象为___.
▼优质解答
答案和解析
Ⅰ.将NaOH溶液与NH4Cl溶液混合生成NH3•H2O,可以说明NaOH的碱性大于NH3•H2O,但不能说明Na的金属性大于N,因为要验证金属性的强弱,必须通过比较最高价氧化物所对应的水化物的碱性来进行比较,而NH3•H2O不是氮元素的最高价氧化物的水化物,
故答案为:不合理,用碱性强弱比较金属性强弱时,一定要用元素的最高价氧化物的水化物的碱性强弱比较,而NH3•H2O不是氮元素的最高价氧化物的水化物;
Ⅱ.(1)球形干燥管D能够防止倒吸,可以避免C中液体进入锥形瓶中,故答案为:防止倒吸;
(2)设计实验验证非金属性:Cl>S,利用氯气与Na2S的氧化还原反应可验证,则装置A、B、C中所装药品应分别为浓盐酸、KMnO4、Na2S溶液,烧瓶中发生反应的离子方程式为:2MnO4-+10Cl-+16H+=2Mn2++5Cl2+8H2O,装置C中的实验现象为有淡黄色沉淀生成,装置C中发生反应的离子方程式为S2-+Cl2═S↓+2Cl-,
故答案为:2MnO4-+10Cl-+16H+=2Mn2++5Cl2+8H2O;S2-+Cl2═S↓+2Cl-;
(5)若要证明非金属性:C>Si,可以通过二氧化碳和硅酸钠反应生成难溶性的硅酸来证明,由于B中加Na2CO3,故A中可以加硫酸,通过硫酸和碳酸钠的反应来制取CO2,然后的CO2通入C中的Na2SiO3中,可以发生反应:Na2SiO3+CO2+H2O=H2SiO3↓+Na2CO3,产生白色胶状沉淀,从而可以证明酸性:H2CO3>H2SiO3,故非金属性:C>Si.
故答案为:稀硫酸;有白色胶状沉淀产生.
故答案为:不合理,用碱性强弱比较金属性强弱时,一定要用元素的最高价氧化物的水化物的碱性强弱比较,而NH3•H2O不是氮元素的最高价氧化物的水化物;
Ⅱ.(1)球形干燥管D能够防止倒吸,可以避免C中液体进入锥形瓶中,故答案为:防止倒吸;
(2)设计实验验证非金属性:Cl>S,利用氯气与Na2S的氧化还原反应可验证,则装置A、B、C中所装药品应分别为浓盐酸、KMnO4、Na2S溶液,烧瓶中发生反应的离子方程式为:2MnO4-+10Cl-+16H+=2Mn2++5Cl2+8H2O,装置C中的实验现象为有淡黄色沉淀生成,装置C中发生反应的离子方程式为S2-+Cl2═S↓+2Cl-,
故答案为:2MnO4-+10Cl-+16H+=2Mn2++5Cl2+8H2O;S2-+Cl2═S↓+2Cl-;
(5)若要证明非金属性:C>Si,可以通过二氧化碳和硅酸钠反应生成难溶性的硅酸来证明,由于B中加Na2CO3,故A中可以加硫酸,通过硫酸和碳酸钠的反应来制取CO2,然后的CO2通入C中的Na2SiO3中,可以发生反应:Na2SiO3+CO2+H2O=H2SiO3↓+Na2CO3,产生白色胶状沉淀,从而可以证明酸性:H2CO3>H2SiO3,故非金属性:C>Si.
故答案为:稀硫酸;有白色胶状沉淀产生.
看了某化学兴趣小组为探究元素性质的...的网友还看了以下:
数列的通项an和与前n项之和Sn的关系(1)已知数列{an}的前n项之和Sn=3n^2-2n,求a 2020-04-09 …
若连续型随机变量X~N(3,4),则(N(0,1)最后是X–3/2还是X–3/若连续型随机变量X~ 2020-04-12 …
(1)设k∈R,当k变化时,直线(2k-1)x-(k+3)y-(k-11)=0有什么不变的性质(2 2020-04-27 …
用力F把铁块压紧在竖直墙上不动,那么,当F变化时(设铁块对墙的压力为N,物体受墙的摩擦力的变化情况 2020-05-17 …
数列问题(速求!)此处的a和S旁的1,n+1,n都是下标1.已知数列满足a1=2,an+1=3的n 2020-06-06 …
概率的证明做题时突然想到了一个问题:暗箱中开始有m个红球,n个白球.每次从暗箱中取出一球后,将此球 2020-06-12 …
有一块厚铁板M,冲下圆柱体N(N能很紧密地塞回原孔).现把铁板和铁柱同时放到炉内加热较长时间,在取 2020-07-06 …
幂级数求和函数时提出x,n的取值应该是不变,只是后面的x^n变为x^(n-1)吧?那为什么陈文灯的 2020-07-14 …
如图所示是放大桌面微小形变的装置,M和N是平稳面,当用力F压桌面时,此时平面镜M上的入射角将(选填 2020-07-17 …
裂变反应衰变次数怎样计算?铀239经过n次β衰变产生钚239,则β衰变次数n为几次?请给出此类问题 2020-07-19 …