早教吧作业答案频道 -->化学-->
如图是在实验室进行二氧化硫制备与验证性质实验的组合装置,部分固定装置未画出.(1)装置B中试剂X是,装置D中盛放NaOH溶液的作用是.(2)关闭弹簧夹2,打开弹簧夹1,注入硫酸
题目详情
如图是在实验室进行二氧化硫制备与验证性质实验的组合装置,部分固定装置未画出.
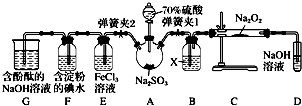
(1)装置B中试剂X是___,装置D中盛放NaOH溶液的作用是___.
(2)关闭弹簧夹2,打开弹簧夹1,注入硫酸至浸没三颈烧瓶中固体,检验SO2与Na2O2反应是否有氧气生成的操作及现象是___.
(3)关闭弹簧夹1后,打开弹簧夹2,残余气体进入E、F、G中,能说明I-还原性弱于SO2的现象为___;发生反应的离子方程式是___.
(4)为了验证E中SO2与FeCl3发生了氧化还原反应,设计了如下实验:
取E中的溶液,往溶液中加入用稀硝酸酸化的BaCl2溶液,产生白色沉淀,说明SO2与FeCl3发生了氧化还原反应.上述方案是否合理?___(填“合理”或“不合理”),原因是___.

(1)装置B中试剂X是___,装置D中盛放NaOH溶液的作用是___.
(2)关闭弹簧夹2,打开弹簧夹1,注入硫酸至浸没三颈烧瓶中固体,检验SO2与Na2O2反应是否有氧气生成的操作及现象是___.
(3)关闭弹簧夹1后,打开弹簧夹2,残余气体进入E、F、G中,能说明I-还原性弱于SO2的现象为___;发生反应的离子方程式是___.
(4)为了验证E中SO2与FeCl3发生了氧化还原反应,设计了如下实验:
取E中的溶液,往溶液中加入用稀硝酸酸化的BaCl2溶液,产生白色沉淀,说明SO2与FeCl3发生了氧化还原反应.上述方案是否合理?___(填“合理”或“不合理”),原因是___.
▼优质解答
答案和解析
A中制备二氧化硫,X干燥二氧化硫,C中检验SO2与Na2O2反应是否有氧气,D中氢氧化钠溶液吸收剩余的二氧化硫,防止污染空气.E装置验证二氧化硫的还原性,F检验I-还原性弱于SO2,G装置验证二氧化硫为酸性气体,并吸收二氧化硫,防止污染空气.
(1)装置B中试剂X干燥氯气,盛放试剂是浓硫酸,二氧化硫与氢氧化钠反应生成亚硫酸钠和水,离子方程式为SO2+2OH-=SO32-+H2O,所以装置D中盛放NaOH溶液的作用是:吸收未反应的SO2,防止污染空气,
故答案为:浓硫酸;吸收未反应的SO2,防止污染空气;
(2)检验SO2与Na2O2反应是否有氧气生成的方法是:将带火星的木条放在D试管口处,看木条是否复燃,
故答案为:将带火星的木条放在D试管口处,看木条是否复燃;
(3)F中的离子方程式为:SO2+I2+2H2O=2I-+SO42-+4H+,该反应中二氧化硫为还原剂,碘离子为还原产物,氧化还原反应中,还原剂的还原性强于还原产物,能说明I-还原性弱于SO2,现象为:F中溶液蓝色褪去,
故答案为:F中溶液蓝色褪去; SO2+I2+2H2O=2I-+SO42-+4H+;
(4)FeCl3与SO2作用,三价铁具有氧化性,二氧化硫具有还原性,三价铁能将二氧化硫氧化为硫酸,自身被还原为亚铁离子,即2FeCl3+SO2+2H2O═2FeCl2+H2SO4+2HCl,可通过检验硫酸根离子,检验该反应的发生,硝酸具有强氧化性,但该实验中硝酸的存在干扰该SO2与FeCl3反应的验证,3SO2SO2+2HNO3+2H2O=3H2SO4+2NO,所以取E中的溶液,往溶液中加入用稀硝酸酸化的BaCl2溶液,产生白色沉淀,硫酸根离子不一定来自于SO2与FeCl3反应产物,故该实验设计不合理,
故答案为:不合理;E中溶解的SO2与稀硝酸反应也生成SO42-.
(1)装置B中试剂X干燥氯气,盛放试剂是浓硫酸,二氧化硫与氢氧化钠反应生成亚硫酸钠和水,离子方程式为SO2+2OH-=SO32-+H2O,所以装置D中盛放NaOH溶液的作用是:吸收未反应的SO2,防止污染空气,
故答案为:浓硫酸;吸收未反应的SO2,防止污染空气;
(2)检验SO2与Na2O2反应是否有氧气生成的方法是:将带火星的木条放在D试管口处,看木条是否复燃,
故答案为:将带火星的木条放在D试管口处,看木条是否复燃;
(3)F中的离子方程式为:SO2+I2+2H2O=2I-+SO42-+4H+,该反应中二氧化硫为还原剂,碘离子为还原产物,氧化还原反应中,还原剂的还原性强于还原产物,能说明I-还原性弱于SO2,现象为:F中溶液蓝色褪去,
故答案为:F中溶液蓝色褪去; SO2+I2+2H2O=2I-+SO42-+4H+;
(4)FeCl3与SO2作用,三价铁具有氧化性,二氧化硫具有还原性,三价铁能将二氧化硫氧化为硫酸,自身被还原为亚铁离子,即2FeCl3+SO2+2H2O═2FeCl2+H2SO4+2HCl,可通过检验硫酸根离子,检验该反应的发生,硝酸具有强氧化性,但该实验中硝酸的存在干扰该SO2与FeCl3反应的验证,3SO2SO2+2HNO3+2H2O=3H2SO4+2NO,所以取E中的溶液,往溶液中加入用稀硝酸酸化的BaCl2溶液,产生白色沉淀,硫酸根离子不一定来自于SO2与FeCl3反应产物,故该实验设计不合理,
故答案为:不合理;E中溶解的SO2与稀硝酸反应也生成SO42-.
看了如图是在实验室进行二氧化硫制备...的网友还看了以下:
今天化学实验考查内容是“实验室制取氧气及氧气性质的验证”.实验一:制取氧气用双氧水、二氧化锰制取氧 2020-04-08 …
化学小组z同学们准备制取氧气.实验室现有双氧水、下氧化锰,以及下列仪器:(1)仪器①名称,仪器②名 2020-04-08 …
下列叙述正确的是()A.碱性氧化物都是金属氧化物B.非金属氧化物都是酸性氧化物C.凡能电离出H+的 2020-05-02 …
过氧化氢制取氧气二氧化锰可以做过氧化氢的的催化剂,制取氧气.H可代替二氧化锰做过氧化氢溶液分解反应 2020-05-13 …
稀H2SO4为什么是非氧化性酸?一般情况下,S(+6)变成(+4)吗?我看的那些答案都说,主要体现 2020-05-14 …
甲醛和氢氧化铜反应生成二氧化碳?新制氢氧化铜悬浊液(斐林试剂)应该是过量的氢氧化钠和硫酸铜配制的, 2020-05-16 …
为什么可溶性碱可由对应的碱性氧化物与水反应制得不溶性碱则不能由对应的碱性氧化物与水反应制得可溶性碱 2020-06-19 …
梨的果皮锈色遗传由两对基因控制,梨果皮的基色呈绿色,由隐性基因r控制,有些品种因为形成木栓层而呈褐 2020-06-26 …
铝制品不宜长期盛放酸性食品和碱性食品是因为铝制品表层物质属于()A.金属铝B.碱性氧化物C.酸性氧化 2020-11-02 …
铝制品不宜长期盛放酸性食品和碱性食品是因为铝制品表层物质属于()A.金属铝B.碱性氧化物C.酸性氧化 2020-11-02 …