实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低,最低可以还原到﹣3价.某同学取一定量的铁铝合金与一定量很稀的硝酸充分
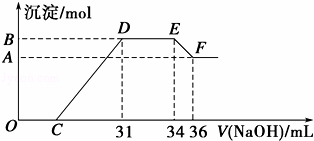
实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低,最低可以还原到﹣3价.某同学取一定量的铁铝合金与一定量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入4mol•L ﹣1 的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示.试回答下列问题:
(1)请写出该合金中铁与硝酸反应的离子方程式 .
(2)图中OC段没有沉淀生成,此阶段发生反应的离子方程式为 .
(3)在DE段,沉淀的物质的量没有变化,则此阶段发生反应的离子方程式为 .
(4)B与A的差值为 mol.
(5)B点对应的沉淀的物质的量为 mol,C点对应的氢氧化钠溶液的体积为 mL.
考点 : 离子方程式的有关计算.
分析: 铝粉和铁粉的混合物与一定量很稀HNO 3 充分反应,被氧化为Al 3+ 、Fe 3+ ,通过题意,反应始终没有气体生成,可以得出不会有氮的氧化物生成,又有硝酸的浓度越稀,对应还原产物中氮元素的化合价越低,可以推测N元素由+5变成了﹣3价,由图可得硝酸过量,加入氢氧化钠溶液应先与硝酸反应,再生成沉淀,当沉淀完全后,由图知继续加入氢氧化钠溶液,沉淀量不变,可得与NH 4 + 发生了反应,则随着NaOH的滴加,发生的反应依次有:
①H + +OH ﹣ =H 2 O,
②Fe 3+ +3OH ﹣ =Fe(OH) 3 ↓,Al 3+ +3OH ﹣ =Al(OH) 3 ↓,
③NH 4 + +OH ﹣ ═NH 3 •H 2 O,
④Al(OH) 3 +OH ﹣ =AlO 2 ﹣ +2H 2 O.
(1)金属铁和稀硝酸反应生成硝酸铁、一氧化氮和水,据此回答;
(2)O→C 之间没有沉淀生成,说明硝酸过量,O→C之间发生的反应酸碱中和反应;
(3)D与E一段沉淀的量没有发生变化,为NH 4 NO 3 和NaOH反应;
(4)E与F之间沉淀的量减少,为Al(OH) 3 溶解在氢氧化钠溶液中,利用发生的化学反应来计算;
(5)沉淀的总量可根据NH 4 + 的量,根据NH 4 + +OH ﹣ ═NH 3 •H 2 O 得出n(NH 4 + ),根据氧化还原反应,N元素由+5价变为﹣3价,而金属都由0价变为+3价,可以运用电子守恒得出金属的物质的量.
铝粉和铁粉的混合物与一定量很稀HNO 3 充分反应,被氧化为Al 3+ 、Fe 3+ ,通过题意,反应始终没有气体生成,可以得出不会有氮的氧化物生成,又有硝酸的浓度越稀,对应还原产物中氮元素的化合价越低,可以推测N元素由+5变成了﹣3价,由图可得硝酸过量,加入氢氧化钠溶液应先与硝酸反应,再生成沉淀,当沉淀完全后,由图知继续加入氢氧化钠溶液,沉淀量不变,可得与NH 4 + 发生了反应,则随着NaOH的滴加,发生的反应依次有:
①H + +OH ﹣ =H 2 O,
②Fe 3+ +3OH ﹣ =Fe(OH) 3 ↓,Al 3+ +3OH ﹣ =Al(OH) 3 ↓,
③NH 4 + +OH ﹣ ═NH 3 •H 2 O,
④Al(OH) 3 +OH ﹣ =AlO 2 ﹣ +2H 2 O
(1)根据图示得到的溶液和氢氧化钠反应产生沉淀的情况可以知道,金属铁和稀硝酸反应生成硝酸铁、一氧化氮和水,反应的离子方程式为:8Fe+30H + +3NO 3 ﹣ =8Fe 3+ +3NH 4 + +9H 2 O,故答案为:8Fe+30H + +3NO 3 ﹣ =8Fe 3+ +3NH 4 + +9H 2 O;
(2)OC之间没有沉淀生成,说明硝酸过量,OC之间发生的反应酸碱中和反应,离子方程式为H + +OH ﹣ ═H 2 O,故答案为:H + +OH ﹣ ═H 2 O;
(3)DE一段沉淀的量没有发生变化,为NH 4 NO 3 和NaOH反应,反应的离子方程式为NH 4 + +OH ﹣ ═NH 3 •H 2 O,故答案为:NH 4 + +OH ﹣ ═NH 3 •H 2 O;
(4)由图可知,EF段消耗的氢氧化钠溶液为36mL﹣34m=2mL,故该计算参加反应的氢氧化钠为0.002L×4mol/L=0.008mol,根据Al(OH) 3 +OH ﹣ =AlO 2 ﹣ +2H 2 O可知,Al(OH) 3 的物质的量为0.008mol,即为B、A的差值,故答案为:0.008;
(5)图中OC段没有沉淀生成,此阶段发生的离子方程式为H + +OH ﹣ =H 2 O;在DE段沉淀的物质的量没有变化,应为NH 4 + 和OH ﹣ 的反应,此阶段发生反应的离子方程式为NH 4 + +OH ﹣ ═NH 3 •H 2 O;根据NH 4 + +OH ﹣ ═NH 3 •H 2 O 得:n(NH 4 + )=(34﹣31)×1
问个化学题,关于混合物的提纯的~下列各组固体混合物,可用作溶解、过滤的方法加以分类的是()A.硝酸钾 2020-03-31 …
1.在一副七巧板中,能够完全重合的三角形有几对?2.在衣服七巧板中不同形状的图形有几种?3.利用七 2020-04-07 …
将含有不溶性物质的硝酸钾固体的混合物放入一定量的水中充分搅拌,得到的实验数据如表1;硝酸钾在不同温 2020-04-25 …
有关集合的问题,已知集合A={X|3≤X<7},集合B={X|2<X<10},求{A与B并集}相对 2020-04-26 …
某一配合物的化学式为crcl3·6h2o向其水溶液中加入硝酸银溶液有1/3的cl沉淀析出,此配合的 2020-05-13 …
现有水300克倒入适量的硝酸钾固体恰好配成60℃的饱和溶液(1)若此时恒温蒸发掉100克水,则析出 2020-05-13 …
在括号里填上合适的关联词泸州油纸伞作为一项民间工艺,()太追求时尚,()失去了油纸伞本身的文化韵味 2020-05-13 …
某金属元素与硝酸根形成化合物的相对分子质量为N,与硫酸根形成的化合物的相对分子质量为M.则该金属的 2020-05-14 …
32g铜与150mL一定浓度的硝酸盐恰好完全反应.产生的NO2和NO混合气体在标准情况下体积11. 2020-05-17 …
共价化合物中某元素化合价的数值元素化合价的数值就是这种元素的一个原子跟其他元素的原子形成的共用电子 2020-05-17 …