早教吧作业答案频道 -->化学-->
红枣包装中常使用一种“504双吸剂”,其成分为铁粉、生石灰等.实验小组同学对一包使用过的“504双吸剂”进行了如下探究.提出问题久置后,固体的成分是什么?查阅资料(1)
题目详情
红枣包装中常使用一种“504双吸剂”,其成分为铁粉、生石灰等.实验小组同学对一包使用过的“504双吸剂”进行了如下探究.
【提出问题】久置后,固体的成分是什么?
【查阅资料】(1)铁与氯化铁溶液在常温下发生反应生成氯化亚铁;
(2)铁可以被磁铁吸引,Fe2O3、CaO、Ca(OH)2、CaCO3均不被磁铁吸引.
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3.
【实验探究】实验方案一:
【实验分析】
(1)酚酞溶液颜色发生改变是因为溶液中含有___(填离子符号)离子;甲同学认为通过实验不能得出一定含Ca(OH)2的结论,理由是___(用化学方程式表示),该反应的基本类型为___.
(2)乙同学认为通过实验不能得出一定不含Fe2O3的结论,理由是___.她设计实验方案二继续进行探究.
实验方案二:
【实验分析】
(1)④中发生的两个复分解反应的化学方程式是___、___.
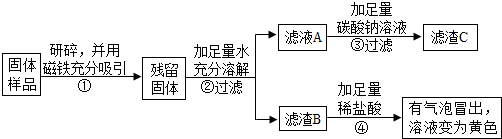
(2)通过实验二可确定固体样品中一定还含有___.
(3)为确定固体样品中是否含有氢氧化钙,实验小组同学又经过实验测得上述残留固体总质量为1.66g,滤渣B质量为1.0g,滤渣C的质量为1.0g.
【实验结论】综合上述实验及所给数据,可判断实验小组同学们的猜想___(填“成立”或“不成立”).
【实验反思】探究硫酸和氢氧化钠反应后硫酸是否有剩余,还可选择一种试剂___.
【提出问题】久置后,固体的成分是什么?
【查阅资料】(1)铁与氯化铁溶液在常温下发生反应生成氯化亚铁;
(2)铁可以被磁铁吸引,Fe2O3、CaO、Ca(OH)2、CaCO3均不被磁铁吸引.
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3.
【实验探究】实验方案一:
| 实验操作 | 实验现象 | 实验结论 |
| (1)取适量固体放于烧杯中,加足量蒸馏水溶解,静置后取上层清液,滴加无色酚酞溶液 | 固体溶解时烧杯外壁发烫 | 固体中一定含有① ___ |
| 酚酞溶液变为② ___色 | 固体中一定含有氢氧化钙 | |
| (2)另取少量固体放于试管中,滴加足量的盐酸 | 固体逐渐消失,有大量无色气体产生,得到浅绿色溶液 | 固体中一定含有③ ___,一定不含Fe2O3 |
| (3)将步骤(2)中产生的气体通入到澄清的石灰水中 | 澄清石灰水变浑浊 | 固体中一定含有④ ___ |
(1)酚酞溶液颜色发生改变是因为溶液中含有___(填离子符号)离子;甲同学认为通过实验不能得出一定含Ca(OH)2的结论,理由是___(用化学方程式表示),该反应的基本类型为___.
(2)乙同学认为通过实验不能得出一定不含Fe2O3的结论,理由是___.她设计实验方案二继续进行探究.
实验方案二:
【实验分析】
(1)④中发生的两个复分解反应的化学方程式是___、___.

(2)通过实验二可确定固体样品中一定还含有___.
(3)为确定固体样品中是否含有氢氧化钙,实验小组同学又经过实验测得上述残留固体总质量为1.66g,滤渣B质量为1.0g,滤渣C的质量为1.0g.
【实验结论】综合上述实验及所给数据,可判断实验小组同学们的猜想___(填“成立”或“不成立”).
【实验反思】探究硫酸和氢氧化钠反应后硫酸是否有剩余,还可选择一种试剂___.
▼优质解答
答案和解析
【实验探究1】甲同学的方案:
(1)取少量固体放于试管中,加足量蒸馏水溶解,静置后取上层清液滴加无色酚酞溶液,固体溶解时试管外壁发烫,说明一定含有氧化钙,氧化钙溶于水放出大量的热,试管底部有不容物,溶液变红,不一定含有氢氧化钙,因为氧化钙和水反应生成氢氧化钙,也能使酚酞试液变红;
(2)另取少量固体放于试管中,滴加足量的稀盐酸,有大量无色气体产生,得到浅绿色溶液,固体中一定含有铁,不一定不含Fe2O3,因为氧化铁和盐酸反应生成氯化铁,铁和氯化铁反应生成氯化亚铁,溶液也是浅绿色.
(3)将步骤(2)中产生的气体通入到澄清的石灰水中,石灰水变浑浊,说明固体中一定含有碳酸钙,碳酸钙与盐酸反应产生二氧化碳使石灰水变浑浊;
【实验分析】(1)酚酞遇碱变红色所以酚酞溶液颜色发生改变是因为溶液中含OH-离子,氧化钙和水反应生成氢氧化钙,化学方程式为:CaO+H2O=Ca(OH)2,该反应属于化合反应;
(2)氧化铁和盐酸反应生成的氯化铁也会与铁反应生成氯化亚铁,所以乙同学认为通过实验不能得出一定不含Fe2O3的结论,理由是:氧化铁和盐酸反应生成氯化铁,铁和氯化铁反应生成氯化亚铁,溶液也是浅绿色;
【实验探究2】(1))④中发生的两个复分解反应是碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,氧化铁和盐酸反应生成氯化铁和水,化学方程式是:Na2CO3+2HCl=2NaCl+H2O+CO2↑,Fe2O3+6HCl=2FeCl3+3H2O;
(2)对滤渣B的探究:①取滤渣B于试管中,加入足量稀盐酸,有气泡冒出,溶液变为黄色,说明一定含有碳酸钙和氧化铁,碳酸钙与盐酸反应产生气泡,氧化铁与盐酸反应产生氯化铁溶于水呈黄色;
【实验结论】经过实验测得上述残留固体中含钙物质的总质量为1.6g,而滤渣B中CaCO3的质量为1.0g,故氧化钙或氢氧化钙或两者混合物质量为0.6g,与碳酸钠反应生成的滤渣C碳酸钙的质量为1.0g,C中钙元素质量是:1.0g×
×100%=0.4g,根据反应前后钙元素守恒,假设0.6g全是氧化钙,则含钙元素质量为0.6g×
×100%=0.428g,假设全是氢氧化钙,则钙元素质量为0.6×
×100%=0.324g,而C中钙元素质量为0.4g,因此是氧化钙和氢氧化钙的混合物,即久置固体的成分是:Fe、Fe2O3、CaO、Ca(OH)2、CaCO3,所以可判断实验小组同学们的猜想成立;
【实验反思】紫色石蕊遇酸变红色,所以探究硫酸和氢氧化钠反应后硫酸是否有剩余,还可选择一种试剂:紫色石蕊试液.
故答案为:【实验探究1】CaO,红,Fe,CaCO3;
【实验分析】(1)OH-,CaO+H2O=Ca(OH)2,化合反应;
(2)氧化铁和盐酸反应生成氯化铁,铁和氯化铁反应生成氯化亚铁,溶液也是浅绿色;
【实验探究2】(1)Na2CO3+2HCl=2NaCl+H2O+CO2↑,Fe2O3+6HCl=2FeCl3+3H2O;
(2)Fe2O3;
【实验结论】成立;
【实验反思】紫色石蕊试液.
(1)取少量固体放于试管中,加足量蒸馏水溶解,静置后取上层清液滴加无色酚酞溶液,固体溶解时试管外壁发烫,说明一定含有氧化钙,氧化钙溶于水放出大量的热,试管底部有不容物,溶液变红,不一定含有氢氧化钙,因为氧化钙和水反应生成氢氧化钙,也能使酚酞试液变红;
(2)另取少量固体放于试管中,滴加足量的稀盐酸,有大量无色气体产生,得到浅绿色溶液,固体中一定含有铁,不一定不含Fe2O3,因为氧化铁和盐酸反应生成氯化铁,铁和氯化铁反应生成氯化亚铁,溶液也是浅绿色.
(3)将步骤(2)中产生的气体通入到澄清的石灰水中,石灰水变浑浊,说明固体中一定含有碳酸钙,碳酸钙与盐酸反应产生二氧化碳使石灰水变浑浊;
【实验分析】(1)酚酞遇碱变红色所以酚酞溶液颜色发生改变是因为溶液中含OH-离子,氧化钙和水反应生成氢氧化钙,化学方程式为:CaO+H2O=Ca(OH)2,该反应属于化合反应;
(2)氧化铁和盐酸反应生成的氯化铁也会与铁反应生成氯化亚铁,所以乙同学认为通过实验不能得出一定不含Fe2O3的结论,理由是:氧化铁和盐酸反应生成氯化铁,铁和氯化铁反应生成氯化亚铁,溶液也是浅绿色;
【实验探究2】(1))④中发生的两个复分解反应是碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,氧化铁和盐酸反应生成氯化铁和水,化学方程式是:Na2CO3+2HCl=2NaCl+H2O+CO2↑,Fe2O3+6HCl=2FeCl3+3H2O;
(2)对滤渣B的探究:①取滤渣B于试管中,加入足量稀盐酸,有气泡冒出,溶液变为黄色,说明一定含有碳酸钙和氧化铁,碳酸钙与盐酸反应产生气泡,氧化铁与盐酸反应产生氯化铁溶于水呈黄色;
【实验结论】经过实验测得上述残留固体中含钙物质的总质量为1.6g,而滤渣B中CaCO3的质量为1.0g,故氧化钙或氢氧化钙或两者混合物质量为0.6g,与碳酸钠反应生成的滤渣C碳酸钙的质量为1.0g,C中钙元素质量是:1.0g×
| 40 |
| 100 |
| 40 |
| 56 |
| 40 |
| 74 |
【实验反思】紫色石蕊遇酸变红色,所以探究硫酸和氢氧化钠反应后硫酸是否有剩余,还可选择一种试剂:紫色石蕊试液.
故答案为:【实验探究1】CaO,红,Fe,CaCO3;
| 实验操作 | 实验现象 | 实验结论 |
| (1)取适量固体放于烧杯中,加足量蒸馏水溶解,静置后取上层清液,滴加无色酚酞溶液 | 固体溶解时烧杯外壁发烫 | 固体中一定含有①氧化钙 |
| 酚酞溶液变为②红色 | 固体中一定含有氢氧化钙 | |
| (2)另取少量固体放于试管中,滴加足量的盐酸 | 固体逐渐消失,有大量无色气体产生,得到浅绿色溶液 | 固体中一定含有③铁,一定不含Fe2O3 |
| (3)将步骤(2)中产生的气体通入到澄清的石灰水中 | 澄清石灰水变浑浊 | 固体中一定含有④碳酸钙 |
(2)氧化铁和盐酸反应生成氯化铁,铁和氯化铁反应生成氯化亚铁,溶液也是浅绿色;
【实验探究2】(1)Na2CO3+2HCl=2NaCl+H2O+CO2↑,Fe2O3+6HCl=2FeCl3+3H2O;
(2)Fe2O3;
【实验结论】成立;
【实验反思】紫色石蕊试液.
看了 红枣包装中常使用一种“504...的网友还看了以下:
语文怎么拿高分英语成绩不稳定我就无语了我初中的时候语文老是才八十多一百二的这次中考才七十多我就晕了 2020-04-11 …
在分类的时候小数和整数算入分数中么? 2020-06-03 …
北方交大高一期中45题第二问不会.45、(6分)A、B、C、X是中学化学常见物质,均由短周期元素组 2020-06-05 …
关于气体的问题通常如“常见短出”或者其它的气体进入瓶中,应哪个管进,哪个出的问题应该靠什么来区分是 2020-06-10 …
求ln(sinx)在π/2到0的反常积分求1/[(1+x^2)*(1+x^a)]在+∞到0上的反常 2020-06-10 …
高等数学中的数学专有名词用英文怎么表达?数列,极限,导数,微分,积分,常数,级数,幂级数,二重积分 2020-06-10 …
因式分解中常用的方法.通常先将几部分进行因式分解,再将结果因式分解.这是什么方法啊? 2020-07-15 …
由C、H两种元素组成的化合物叫烃.常温常压下,分子中碳原子个数小于或等于4的烃通常为气体.常温常压 2020-07-17 …
怎么由x^2-400x-120000=0变形为(X-600)(X+200)=0一定要非常非常详细的 2020-08-02 …
十分常见是病句么十分常见常见已经包含了程度的意思了吧可十分是什么作用呢 2020-11-11 …