早教吧作业答案频道 -->化学-->
海带中含有丰富的碘.为了从海带中提取碘,某研究性学习小组设计并进行了以下实验.请回答以下有关问题:(1)灼烧海带时,是将处理好的海带用酒精湿润后在干锅中进行,请问有酒精
题目详情
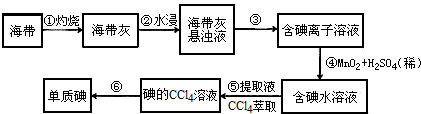
海带中含有丰富的碘.为了从海带中提取碘,某研究性学习小组设计并进行了以下实验.
请回答以下有关问题:
(1)灼烧海带时,是将处理好的海带用酒精湿润后在干锅中进行,请问有酒精进行湿润的目的是___.
(2)步骤③的实验操作名称是___;在实验室进行该项操作时,用到的玻璃仪器除了漏斗、玻璃棒外还有___.
(3)步骤④反应的离子方程式为___;该步骤所用氧化剂还可以用___替代.
(4)用CCl4从碘水中萃取碘并用分液漏斗分离两种溶液,其实验操作可分解为如下几步:
(A)把盛有溶液的分液漏斗放在铁架台的铁圈上;
(B)把50mL碘水和15mLCCl4加入分液漏斗中,并盖好玻璃塞;
(C)检验分液漏斗的活塞与上口的玻璃塞是否漏水;
(D)倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
(E)旋开活塞,用烧杯接受溶液;
(F)从分液漏斗上口倒出上层水溶液;
(G)将漏斗上口的玻璃塞打开或使塞上边凹槽或小孔对准漏斗口上的小孔;
(H)静置、分层.
①正确操作步骤的顺序是(用上述各操作的编号字母填空):
___→___→___→A→G→___→E→F.
②(G)步骤操作的目的是___.
(5)已知3I2+6OH-=5I-+IO3-+3H2O,5I-+IO3-+6H+=3I2↓+3H2O.在进行第⑥步操作时,先在碘的CCl4中加入适量40%NaOH溶液,至CCl4层变为___色,分液.接下来的操作方法是___.

请回答以下有关问题:
(1)灼烧海带时,是将处理好的海带用酒精湿润后在干锅中进行,请问有酒精进行湿润的目的是___.
(2)步骤③的实验操作名称是___;在实验室进行该项操作时,用到的玻璃仪器除了漏斗、玻璃棒外还有___.
(3)步骤④反应的离子方程式为___;该步骤所用氧化剂还可以用___替代.
(4)用CCl4从碘水中萃取碘并用分液漏斗分离两种溶液,其实验操作可分解为如下几步:
(A)把盛有溶液的分液漏斗放在铁架台的铁圈上;
(B)把50mL碘水和15mLCCl4加入分液漏斗中,并盖好玻璃塞;
(C)检验分液漏斗的活塞与上口的玻璃塞是否漏水;
(D)倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
(E)旋开活塞,用烧杯接受溶液;
(F)从分液漏斗上口倒出上层水溶液;
(G)将漏斗上口的玻璃塞打开或使塞上边凹槽或小孔对准漏斗口上的小孔;
(H)静置、分层.
①正确操作步骤的顺序是(用上述各操作的编号字母填空):
___→___→___→A→G→___→E→F.
②(G)步骤操作的目的是___.
(5)已知3I2+6OH-=5I-+IO3-+3H2O,5I-+IO3-+6H+=3I2↓+3H2O.在进行第⑥步操作时,先在碘的CCl4中加入适量40%NaOH溶液,至CCl4层变为___色,分液.接下来的操作方法是___.
▼优质解答
答案和解析
(1)酒精为易燃物品,燃烧生成二氧化碳和水,用酒精进行湿润处理好的海带,然后进行灼烧,能促进海带快速燃烧,
故答案为:促进海带快速燃烧;
(2)分离固体和液体用过滤,海带灼烧后得到海带灰浸泡后得到海带灰的浊液,将悬浊液分离为残渣和含碘离子溶液应选择过滤的方法,过滤时需要制作过滤器的漏斗、固定仪器的铁架台、引流用的玻璃棒、承接滤液的烧杯,所以用到的玻璃仪器除了漏斗、玻璃棒外还有烧杯,
故答案为:过滤;烧杯;
(3)碘离子在酸性条件下可被MnO2氧化生成单质碘:离子方程式为:2I-+MnO2+4H+=Mn2++I2+2H2O;通入氯气,Cl2+2I-=I2+2Cl-,加入氢离子和过氧化氢起的作用为氧化剂,也能将碘离子转化为单质碘,离子方程式为2H++2I-+H2O2═I2+2H2O,
故答案为:2I-+MnO2+4H+=I2+Mn2++2H2O;氯水、H2O2等;
(4)①检查分液漏斗是否漏液→把50mL碘水和15mLCCl4加入分液漏斗中,盖好玻璃塞→倒转分液漏斗,振荡→把盛有溶液的分液漏斗放在铁架台的铁圈上→静置,分层→打开分液漏斗上口玻璃塞或使塞上的凹槽对准漏斗上口的小孔→旋开活塞,用烧杯盛接溶液→从分液漏斗上口倒出上层溶液,所以正确的操作顺序是:CBDAGH,
故答案为:CBDAGH;
②不打开活塞,液体在大气压作用下无法流出,目的是保持分液漏斗内外压力平衡,使液体易于流下,
故答案为:保证漏斗中液体顺利流出;
(5)碘和氢氧化钠反应生成碘化钠、次碘酸钠和水,反应的化学方程式为:I2+2NaOH═NaI+NaIO+H2O,碘单质被消耗,CCl4层变为无色,分液,再在所得水溶液中加入过量的稀硫酸,在酸性条件下,+1价的碘和-1价的碘发生氧化还原反应I-+IO-+2H+=I2+H2O,过滤得碘单质.
故答案为:无;在所得水溶液中加入过量的稀硫酸,过滤得碘单质.
故答案为:促进海带快速燃烧;
(2)分离固体和液体用过滤,海带灼烧后得到海带灰浸泡后得到海带灰的浊液,将悬浊液分离为残渣和含碘离子溶液应选择过滤的方法,过滤时需要制作过滤器的漏斗、固定仪器的铁架台、引流用的玻璃棒、承接滤液的烧杯,所以用到的玻璃仪器除了漏斗、玻璃棒外还有烧杯,
故答案为:过滤;烧杯;
(3)碘离子在酸性条件下可被MnO2氧化生成单质碘:离子方程式为:2I-+MnO2+4H+=Mn2++I2+2H2O;通入氯气,Cl2+2I-=I2+2Cl-,加入氢离子和过氧化氢起的作用为氧化剂,也能将碘离子转化为单质碘,离子方程式为2H++2I-+H2O2═I2+2H2O,
故答案为:2I-+MnO2+4H+=I2+Mn2++2H2O;氯水、H2O2等;
(4)①检查分液漏斗是否漏液→把50mL碘水和15mLCCl4加入分液漏斗中,盖好玻璃塞→倒转分液漏斗,振荡→把盛有溶液的分液漏斗放在铁架台的铁圈上→静置,分层→打开分液漏斗上口玻璃塞或使塞上的凹槽对准漏斗上口的小孔→旋开活塞,用烧杯盛接溶液→从分液漏斗上口倒出上层溶液,所以正确的操作顺序是:CBDAGH,
故答案为:CBDAGH;
②不打开活塞,液体在大气压作用下无法流出,目的是保持分液漏斗内外压力平衡,使液体易于流下,
故答案为:保证漏斗中液体顺利流出;
(5)碘和氢氧化钠反应生成碘化钠、次碘酸钠和水,反应的化学方程式为:I2+2NaOH═NaI+NaIO+H2O,碘单质被消耗,CCl4层变为无色,分液,再在所得水溶液中加入过量的稀硫酸,在酸性条件下,+1价的碘和-1价的碘发生氧化还原反应I-+IO-+2H+=I2+H2O,过滤得碘单质.
故答案为:无;在所得水溶液中加入过量的稀硫酸,过滤得碘单质.
看了 海带中含有丰富的碘.为了从海...的网友还看了以下:
为什么可以用四氯化碳萃取碘水中的碘?改用酒精萃取行么?为什么可以用四氯化碳萃取碘水中的碘? 2020-05-17 …
行政法律关系的客体不包括( )。 A.物质财富 B.行为 C.精神财富 D.权利和义务 2020-05-30 …
行政法律关系主体包括行政主体和( )。 A.行政相对方 B. 物质财富 C. 行为 D. 精神财富 2020-05-30 …
甲种酒精纯酒精含量为72%,乙种酒精纯酒精含量为58%,混合后纯酒精含量为62%,如果每种酒精取的 2020-06-21 …
甲种酒精纯酒精含量为72%,乙种酒精纯酒精含量为58%,混合后纯酒精含量为62%,如果每种酒精取的 2020-06-21 …
生命是一个逐渐丰富的过程,作为新时期的中学生,我们要积极扩展生活阅历,让生命充满色彩与活力,活出生命 2020-10-30 …
“财富是蒙上帝的恩赐的人获得成功的标志,选民要以奋斗的精神取得事业的成功,并且具有节制、忍耐、简朴、 2020-11-25 …
行政法律关系的客体可以概括为:A.行政相对方B.物质财富和精神财富C.行为D.事件多选题 2020-12-14 …
“财富是蒙上帝的恩赐的人获得成功的标志,选民要以奋斗的精神取得事业的成功,并且具有节制、忍耐、简朴、 2021-01-02 …
生命是一个逐渐丰富的过程,作为新时期的中学生,我们要积极扩展生活阅历,让生命充满色彩与活力,话出生命 2021-01-12 …