早教吧作业答案频道 -->化学-->
肼可作为火箭发动机的燃料,与N2O4反应生成N2和水蒸气.已知:①N2(g)+2O2(g)=N2O4(l)△H1=-19.5kJ•mol-1②N2H4(l)+O2(g)=N2(g)+2H2O(g)△H2=-534.2kJ•mol-1(1)写出肼和N2O4反应反应生成N
题目详情
肼可作为火箭发动机的燃料,与N2O4反应生成N2和水蒸气.已知:
①N2(g)+2O2(g)=N2O4(l)△H1=-19.5kJ•mol-1
②N2H4(l)+O2(g)=N2(g)+2H2O(g)△H2=-534.2kJ•mol-1
(1)写出肼和N2O4反应反应生成N2和水蒸气的热化学方程式___;
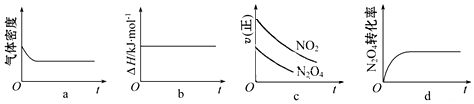
(2)火箭残骸中常现红棕色气体,当温度升高时,气体颜色变深,原因是存在如下反应:N2O4(g)⇌2NO2(g)△H>0,一定温度下,将1mol N2O4充入一恒压密闭容器中发生上述反应,下列示意图正确且能说明反应达到平衡状态的是___.
(3)肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液.肼-空气燃料电池放电时负极的电极反应式是___.
(4)传统制备肼的方法,是以NaClO氧化NH3,制得肼的稀溶液.该反应的离子方程式是___.肼可作为火箭发动机的燃料,与N2O4反应生成N2和水蒸气.已知:
①N2(g)+2O2(g)=N2O4(l)△H1=-19.5kJ•mol-1
②N2H4(l)+O2(g)=N2(g)+2H2O(g)△H2=-534.2kJ•mol-1
(1)写出肼和N2O4反应反应生成N2和水蒸气的热化学方程式___;
(2)火箭残骸中常现红棕色气体,当温度升高时,气体颜色变深,原因是存在如下反应:N2O4(g)⇌2NO2(g)△H>0,一定温度下,将1mol N2O4充入一恒压密闭容器中发生上述反应,下列示意图正确且能说明反应达到平衡状态的是___.

(3)肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液.肼-空气燃料电池放电时负极的电极反应式是___.
(4)传统制备肼的方法,是以NaClO氧化NH3,制得肼的稀溶液.该反应的离子方程式是___.242
22241-1
242222-1
242
24224

3
①N2(g)+2O2(g)=N2O4(l)△H1=-19.5kJ•mol-1
②N2H4(l)+O2(g)=N2(g)+2H2O(g)△H2=-534.2kJ•mol-1
(1)写出肼和N2O4反应反应生成N2和水蒸气的热化学方程式___;
(2)火箭残骸中常现红棕色气体,当温度升高时,气体颜色变深,原因是存在如下反应:N2O4(g)⇌2NO2(g)△H>0,一定温度下,将1mol N2O4充入一恒压密闭容器中发生上述反应,下列示意图正确且能说明反应达到平衡状态的是___.

(3)肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液.肼-空气燃料电池放电时负极的电极反应式是___.
(4)传统制备肼的方法,是以NaClO氧化NH3,制得肼的稀溶液.该反应的离子方程式是___.肼可作为火箭发动机的燃料,与N2O4反应生成N2和水蒸气.已知:
①N2(g)+2O2(g)=N2O4(l)△H1=-19.5kJ•mol-1
②N2H4(l)+O2(g)=N2(g)+2H2O(g)△H2=-534.2kJ•mol-1
(1)写出肼和N2O4反应反应生成N2和水蒸气的热化学方程式___;
(2)火箭残骸中常现红棕色气体,当温度升高时,气体颜色变深,原因是存在如下反应:N2O4(g)⇌2NO2(g)△H>0,一定温度下,将1mol N2O4充入一恒压密闭容器中发生上述反应,下列示意图正确且能说明反应达到平衡状态的是___.

(3)肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液.肼-空气燃料电池放电时负极的电极反应式是___.
(4)传统制备肼的方法,是以NaClO氧化NH3,制得肼的稀溶液.该反应的离子方程式是___.242
22241-1
242222-1
242
24224

3
▼优质解答
答案和解析
(1)肼可作为火箭发动机的燃料,与氧化剂N22O44反应生成N22和水蒸气,
①N22(g)+2O22(g)=N22O44(l)△H11=-19.5kJ•mol-1-1
②N22H44(l)+O22(g)=N22(g)+2H22O(g)△H22=-534.2kJ•mol-1-1
根据盖斯定律将方程式②×2-①得肼和N22H44 反应的热化学方程式:2N22H44(l)+N22O44(l)=3N22(g)+4H22O(g)△H=-1048.9kJ/mol,
故答案为:2N22H44(l)+N22O44(l)=3N22(g)+4H22O(g)△H=-1048.9kJ/mol;
(2)a、反应方程式两边气体的质量不相等,密度不变,说明达到了平衡状态,故a正确;
b、反应过程中,反应热不会变化,不是变量,无法判断是否达到平衡状态,故b错误;
c、根据图象,正反应速率还在减小,则说明未达到平衡状态,故c错误;
d、四氧化二氮的转化率不变,说明正逆反应速率相等,达到了平衡状态,故d正确;
故选ad;
(3)肼一空气燃料碱性电池中,负极上肼失电子和氢氧根离子反应生成水和氮气,电极反应式为:N22H44+4OH---4e--=4H22O+N22↑,
故答案为:N22H44+4OH---4e--=4H22O+N22↑;
(4)NH33与NaClO发生氧化还原反应可得到肼(N22H44)、氯化钠和水,所以该反应的离子方程式为:2NH33+ClO--=N22H44+Cl--+H22O,
故答案为:2NH33+ClO--=N22H44+Cl--+H22O.
①N22(g)+2O22(g)=N22O44(l)△H11=-19.5kJ•mol-1-1
②N22H44(l)+O22(g)=N22(g)+2H22O(g)△H22=-534.2kJ•mol-1-1
根据盖斯定律将方程式②×2-①得肼和N22H44 反应的热化学方程式:2N22H44(l)+N22O44(l)=3N22(g)+4H22O(g)△H=-1048.9kJ/mol,
故答案为:2N22H44(l)+N22O44(l)=3N22(g)+4H22O(g)△H=-1048.9kJ/mol;
(2)a、反应方程式两边气体的质量不相等,密度不变,说明达到了平衡状态,故a正确;
b、反应过程中,反应热不会变化,不是变量,无法判断是否达到平衡状态,故b错误;
c、根据图象,正反应速率还在减小,则说明未达到平衡状态,故c错误;
d、四氧化二氮的转化率不变,说明正逆反应速率相等,达到了平衡状态,故d正确;
故选ad;
(3)肼一空气燃料碱性电池中,负极上肼失电子和氢氧根离子反应生成水和氮气,电极反应式为:N22H44+4OH---4e--=4H22O+N22↑,
故答案为:N22H44+4OH---4e--=4H22O+N22↑;
(4)NH33与NaClO发生氧化还原反应可得到肼(N22H44)、氯化钠和水,所以该反应的离子方程式为:2NH33+ClO--=N22H44+Cl--+H22O,
故答案为:2NH33+ClO--=N22H44+Cl--+H22O.
看了 肼可作为火箭发动机的燃料,与...的网友还看了以下:
[N2O2]2-这个结构怎么写是[O=N-N=O]2-还是中心N与2个O和一个端基N相连 2020-04-06 …
椭圆的中心为原点O,离心率e=√2/2,一条准线的方程为x=2√2……椭圆的中心为原点O,离心率e 2020-05-16 …
1.(1)已知数轴上点M,O,N对应的数分别-3.0.1,点p为数轴上任意一点.如果点p到M,N距 2020-06-06 …
谁帮我做下下面的关于时间复杂度的习题?f(n)=100n^3+n^2+1000,g(n)=25n^ 2020-06-12 …
求给以下算法复杂度排序增长速度由慢到快1)O(n^(3/4))O(log(n)^5)O(2^n)O 2020-07-23 …
如图所示,在射线OM上有三点A、B、C.OA=20,AB=m,BC=n,m,n满足|m-6n|=- 2020-07-24 …
设算法的计算时间可用递推关系式T(n)=2T(n/2)+n表示,则该算法的时间复杂度为()A:O( 2020-08-01 …
总体X服从N(u,sigma^2).x1.xn为样本,u已知,sigma^2未知x为样本平均值s^ 2020-08-03 …
算法时间复杂度问题,谢谢!最好有解释假设算法A1和算法A2都可以解决规模为n的问题P,且时间复杂度都 2020-10-31 …
关于渐进时间复杂度题已知某一算法的时间复杂度上限函数满足递归关系T(n)=2(T/2)+n,那么该算 2021-01-14 …