下图是我校实验室化学试剂浓硫酸标签上的部分内容。现需要480mL1mol·L-1的稀硫酸。用该浓硫酸和蒸馏水配制,可供选用的仪器有:①胶头滴管;②玻璃棒;③烧杯;④量筒。请回
下图是我校实验室化学试剂浓硫酸标签上的部分内容。现需要480 mL 1 mol·L-1的稀硫酸。用该浓硫酸和蒸馏水配制,可供选用的仪器有:① 胶头滴管;②玻璃棒;③烧杯;④量筒。
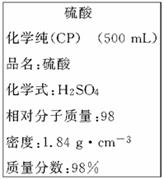
请回答下列问题:
(1)配制稀硫酸时,还缺少的仪器有______________(写仪器名称)。
(2)该硫酸的物质的量浓度为 mol/L;所需浓硫酸的体积 约为___________mL;若将该浓硫酸与等体积的水混合,所得溶液中溶质的质量分数____________49%(填“>” 、“<” 或“=”)。
(3)定容时 若加入的水超过刻度线 必须采取的措施是
(4)下列操作对H2SO4的物质的量浓度有什么影响(偏高、偏低或无影响)?
①转移溶液后,未洗涤烧杯: ;
②容量瓶用水洗净后未烘干: ;
③定容时俯视容量瓶的刻度线: 。
(5)在配置过程中,下列操作不正确的是(填序号) 。
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配液润洗
C.将准确量取的18.4mol·L-1的硫酸,注入已盛有100mL水的500mL的容量瓶中,加水至刻度线.
D.将硫酸溶于水后需冷却至室温再转移到容量瓶中
E.定容后塞好瓶塞,用食指顶住瓶塞,用另一只手的手掌托住瓶底,把容量瓶倒转摇匀
【答案】(11分)(1)—(4)题每空1分(5)题3分,漏选2分多选错选不给分
(1)500m L 容量瓶 (2)18.4 27.2 >
(3)重新配制 (4)偏低 无影响 偏高 (5)BCE
【解析】
试题分析:(1)配制顺序是:计算→量取→稀释、冷却→移液→洗涤→定容→摇匀→装瓶贴签,一般用量筒(用到胶头滴管)量取,在烧杯中稀释,冷却后转移到100mL容量瓶中,并用玻璃棒引流,转移完毕,用少量蒸馏水洗涤烧杯及玻璃棒2~3次并将洗涤液全部转移到容量瓶中,再加适量蒸馏水,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,使溶液的凹液面的最低点与刻线相平,塞好瓶塞,反复上下颠倒摇匀.所以需要的仪器为:量筒、胶头滴管、烧杯、玻璃棒、500mL容量瓶,缺少500 mL的容量瓶、玻璃棒;
(2)如图所示浓硫酸的浓度为![]() =18.4mol/L.稀释前后溶质的物质的量不发生变化,故18.4mol/LxV=500mlx1mol/L,解得V=27.2ml;若将该浓硫酸与等体积的水混合,硫酸溶质的质量不发生变化,质量分数为
=18.4mol/L.稀释前后溶质的物质的量不发生变化,故18.4mol/LxV=500mlx1mol/L,解得V=27.2ml;若将该浓硫酸与等体积的水混合,硫酸溶质的质量不发生变化,质量分数为![]() ,由于硫酸的密度大于水的密度,等体积混合硫酸的质量大于水的质量,故质量分数大于49%;
,由于硫酸的密度大于水的密度,等体积混合硫酸的质量大于水的质量,故质量分数大于49%;
(3)定容时 若加入的水超过刻度线,已经无法达到配制溶液所需要浓度,故必须重新配制;
(4)①转移溶液后,未洗涤烧杯,溶质未全部进入容量瓶,导致浓度偏低;②容量瓶用水洗净后未烘干,因配制过程中需要添加水,对浓度无影响;③定容时俯视容量瓶的刻度线,液面在刻度线以下,体积偏小,导致浓度偏高;
(5)容量瓶瓶口有活塞,使用容量瓶前应检查它是否漏水,A正确; 容量瓶用蒸馏水洗净后,不能用待配液润洗,否则导致浓度偏高,B错误;容量瓶只是定容容器,不可作溶解或稀释容器,C错误;浓硫酸溶解于水时溶液温度升高,需要冷却后再转移到容量瓶中,否则导致浓度偏高,D正确;定容后塞好瓶塞,用食指顶住瓶塞,用另一只手的四指托住瓶底,把容量瓶颠倒摇匀,E错误。
考点:配制一定物质的量浓度的溶液及误差分析
同学聚会约定中午12时准时到会早到的计为正迟到的计为负结果最早到的同学记为+2h最迟到的同学为—0 2020-04-07 …
设f(x)是定义在对称区间(-L,L)内的任何函数,证明……设f(x)是定义在对称区间(-L,L) 2020-05-16 …
写出下列算法的功能LinkListdemo(LinkListL){ListNode*q,*p;If 2020-05-17 …
设函数f(x)是定义在(-L,L)内的奇函数(L〉0),证明若f(x)在(-L,0)内单调增加,则 2020-06-09 …
先学离散数学还是先学高等数学(工本)?自考的,前面已经考了数据结构,概率论与数理统计,想知道离散数 2020-06-10 …
定义点P(x0,y0)到直线l:Ax+By+C=0(A2+B2≠0)的有向距离为d=Ax0+By0 2020-07-09 …
某学校为每个学生编排学籍号,如果设定末尾用1表示男生,用2表示女生,如:983012表示1998年入 2020-11-04 …
某学校为每个学生编排学籍号,如果设定末尾用1表示男生,用2表示女生,如:983012表示1998年入 2020-11-04 …
学校为每个新生编号,设定末位1表示男生,0表示女生,“199713321”表示“1997年入学的一年 2020-11-14 …
用L,l,m表示k某种弹簧秤原来的长度为l,悬挂重物后的长度L可用公式L=l+k分之m表示某种弹簧秤 2020-12-05 …