早教吧作业答案频道 -->化学-->
甲烷广泛存在于天然气、沼气、煤矿坑气之中,是优质的气体燃料,更是制造许多化工产品的重要原料.Ⅰ.制取氢气已知:CH4(g)+H2O(g)⇌CO(g)+3H2(g)△H=+206.2kJ•mol-1CH4(g)+CO2(g
题目详情
甲烷广泛存在于天然气、沼气、煤矿坑气之中,是优质的气体燃料,更是制造许多化工产品的重要原料.
Ⅰ.制取氢气
已知:CH4(g)+H2O(g)⇌CO(g)+3H2(g)△H=+206.2kJ•mol-1
CH4(g)+CO2(g)⇌2CO(g)+2H2(g)△H=+247.4kJ•mol-1
(1)请写出CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式___
(2)若将0.1mol CH4和0.1mol H2O(g)通入体积为10L的密闭容器里,在一定条件下发生反应:
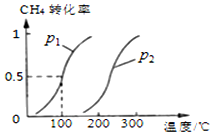
CH4(g)+H2O(g)⇌CO(g)+3H2(g),CH4的平衡转化率与温度、压强的关系如图
①已知100℃时达到平衡所需的时间为5min,则用H2表示的平均反应速率___;
②该反应的化学平衡常数___;
③图中的p1___p2(填“<”、“>”或“=”);
Ⅱ.制备甲醇
(3)在压强为0.1MPa条件下,将a mol CO与3amol H2的混合气体在催化剂作用下能自发反应生成甲醇:CO(g)+2H2(g)⇌CH3OH(g)△H<0.若容器容积不变,下列措施可增加甲醇产率的是___
A.升高温度 B.再充入1mol CO和3mol H2 C.将CH3OH(g)从体系中分离
D.充入He,使体系总压强增大 E.使用更高效的催化剂
Ⅲ.合成乙酸
(4)甲烷直接合成乙酸具有重要的理论意义和应用价值.光催化反应技术使用CH4和___(填化学式)直接合成乙酸,且符合“绿色化学”的要求(原子利用率100%).
Ⅰ.制取氢气
已知:CH4(g)+H2O(g)⇌CO(g)+3H2(g)△H=+206.2kJ•mol-1
CH4(g)+CO2(g)⇌2CO(g)+2H2(g)△H=+247.4kJ•mol-1

(1)请写出CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式___
(2)若将0.1mol CH4和0.1mol H2O(g)通入体积为10L的密闭容器里,在一定条件下发生反应:
CH4(g)+H2O(g)⇌CO(g)+3H2(g),CH4的平衡转化率与温度、压强的关系如图
①已知100℃时达到平衡所需的时间为5min,则用H2表示的平均反应速率___;
②该反应的化学平衡常数___;
③图中的p1___p2(填“<”、“>”或“=”);
Ⅱ.制备甲醇
(3)在压强为0.1MPa条件下,将a mol CO与3amol H2的混合气体在催化剂作用下能自发反应生成甲醇:CO(g)+2H2(g)⇌CH3OH(g)△H<0.若容器容积不变,下列措施可增加甲醇产率的是___
A.升高温度 B.再充入1mol CO和3mol H2 C.将CH3OH(g)从体系中分离
D.充入He,使体系总压强增大 E.使用更高效的催化剂
Ⅲ.合成乙酸
(4)甲烷直接合成乙酸具有重要的理论意义和应用价值.光催化反应技术使用CH4和___(填化学式)直接合成乙酸,且符合“绿色化学”的要求(原子利用率100%).
▼优质解答
答案和解析
(1)①CH4(g)+H2O(g)═CO(g)+3H2(g)△H=206.2kmol-1
②CH4(g)+CO2(g)═2CO(g)+2H2(g)△H=247.4kJmol-1
由盖斯定律,①×2-②得:CH4(g)+2H2O(g)═CO2(g)+4H2(g)△H=+165.0kmol-1,
故答案为:CH4(g)+2H2O(g)═CO2(g)+4H2(g)△H=+165.0kmol-1;
(2)将1.0mol CH4和2.0mol H2O ( g )通入容积固定为10L的反应室,在一定条件下发生反应I,由图象可知100℃甲烷转化率为50%,故参加反应的甲烷为1mol×50%=0.5mol,则:
CH4 (g)+H2O (g)=CO (g)+3H2 (g)
起始量(mol):1.0 2.0 0 0
变化量(mol):0.5 0.5 0.5 1.5
平衡量(mol):0.5 1.5 0.5 1.5
①假设100℃时达到平衡所需的时间为5min,则用H2表示该反应的平均反应速率=
=0.003 mol•L-1•min-1,
故答案为:0.0030mol•L-1•min-1;
②该反应的化学平衡常数K=
=
=6.75×10-4(mol/L)2,故答案为:6.75×10-4(mol/L)2;
③通过图表可知当温度相同时,p2→p1时,甲烷的转化率提高,平衡向正向移动,正向为气体系数增大的反应,根据减小压强平衡向系数增大的方向移动可知:p1<p2,故答案为:<;
(3)A.该反应是放热的,升高温度,平衡逆向进行,会减小甲醇产率,故A错误;
B.再充入1mol CO和3molH2,增大压强,平衡右移,有利提高甲醇的产率,故B正确;
C.将CH3OH(g)从体系中分离,会促使平衡正向移动,提高甲醇的产率,故C正确;
D.充入He,使体系总压强增大,体积不变,各组分浓度不变,所以平衡不会移动,不会改变甲醇产率,故D错误;
E.使用催化剂能改变反应速率,但平衡不移动,故E错误;
故选BC;
(4)利用加成反应可以使原子利用率100%,现有甲烷(CH4)与另一种化合物发生加成反应生成CH3COOH,根据原子守恒可知另一物质为CO2,故答案为:CO2.
②CH4(g)+CO2(g)═2CO(g)+2H2(g)△H=247.4kJmol-1
由盖斯定律,①×2-②得:CH4(g)+2H2O(g)═CO2(g)+4H2(g)△H=+165.0kmol-1,
故答案为:CH4(g)+2H2O(g)═CO2(g)+4H2(g)△H=+165.0kmol-1;
(2)将1.0mol CH4和2.0mol H2O ( g )通入容积固定为10L的反应室,在一定条件下发生反应I,由图象可知100℃甲烷转化率为50%,故参加反应的甲烷为1mol×50%=0.5mol,则:
CH4 (g)+H2O (g)=CO (g)+3H2 (g)
起始量(mol):1.0 2.0 0 0
变化量(mol):0.5 0.5 0.5 1.5
平衡量(mol):0.5 1.5 0.5 1.5
①假设100℃时达到平衡所需的时间为5min,则用H2表示该反应的平均反应速率=
| ||
| 5min |
故答案为:0.0030mol•L-1•min-1;
②该反应的化学平衡常数K=
| c(CO)×c3(H2) |
| c(CH4)×c(H2O) |
(
| ||||
(
|
③通过图表可知当温度相同时,p2→p1时,甲烷的转化率提高,平衡向正向移动,正向为气体系数增大的反应,根据减小压强平衡向系数增大的方向移动可知:p1<p2,故答案为:<;
(3)A.该反应是放热的,升高温度,平衡逆向进行,会减小甲醇产率,故A错误;
B.再充入1mol CO和3molH2,增大压强,平衡右移,有利提高甲醇的产率,故B正确;
C.将CH3OH(g)从体系中分离,会促使平衡正向移动,提高甲醇的产率,故C正确;
D.充入He,使体系总压强增大,体积不变,各组分浓度不变,所以平衡不会移动,不会改变甲醇产率,故D错误;
E.使用催化剂能改变反应速率,但平衡不移动,故E错误;
故选BC;
(4)利用加成反应可以使原子利用率100%,现有甲烷(CH4)与另一种化合物发生加成反应生成CH3COOH,根据原子守恒可知另一物质为CO2,故答案为:CO2.
看了 甲烷广泛存在于天然气、沼气、...的网友还看了以下:
1.裂化气2.裂解气3.电石气4.水煤气5.天然气6.石油气7.高炉煤气8.爆鸣气9.沼气10.坑 2020-05-16 …
(15分)甲烷是天然气、沼气、坑气及煤气的主要成分之一,可用作燃料及制造氢、一氧化碳、甲醛等物质的 2020-06-24 …
甲烷广泛存在于天然气、沼气、煤矿坑气之中,是优质的气体燃料,更是制造许多化工产品的重要原料Ⅰ.制取 2020-07-10 …
甲烷广泛存在于天然气、沼气、煤矿坑气之中,是优质的气体燃料,更是制造许多化工产品的重要原料.Ⅰ.制 2020-07-10 …
煤炭是目前我国的主要能源来源,不安全的煤炭开采会导致煤矿爆炸事故,其元凶是煤矿坑道气中含有的甲烷. 2020-07-22 …
据报道,每年都有一些煤矿发生“瓦斯”爆炸事故,原因是在采集原煤的坑道中有一种可燃性气体“坑气”.“坑 2020-11-02 …
3、煤矿坑道内的“瓦斯”爆炸往往造成重大矿难事故,“瓦斯”的主要成分是甲烷气体.以下措施不能防止煤矿 2020-11-11 …
煤矿坑道内的“瓦斯”爆炸往往造成重大矿难事故,“瓦斯”的主要成分是甲烷气体.以下措施不能防止煤矿坑道 2020-12-23 …
煤矿坑道内的“瓦斯”爆炸往往造成重大矿难事故,“瓦斯”的主要成分是甲烷气体.以下措施不能防止煤矿坑道 2020-12-23 …
为了提高煤燃烧的热效率并减少SO2和烟尘对大气的污染,适宜采取的措施是()A.通入大量的空气B.将煤 2021-01-09 …