早教吧作业答案频道 -->化学-->
航天员呼吸产生的CO2用下列反应处理,可实现空间站中O2的循环利用,Sabatier反应:CO2(g)+4H2(g)⇌CH4(g)+2H2O(g)水电解反应:2H2O(l)电解
题目详情
航天员呼吸产生的CO2用下列反应处理,可实现空间站中O2的循环利用,Sabatier反应:
CO2(g)+4H2(g)⇌CH4(g)+2H2O(g)
水电解反应:2H2O(l)
2H2(g)+O2(g)
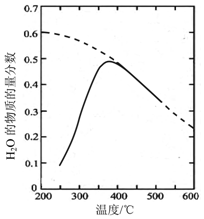
(1)将原料气按n(CO2):nH2=1:4置于密闭容器中发生Sabatier反应,测得H2O(g)的物质的量分数与温度的关系如图所示(虚线表示平衡曲线).
①该反应的平衡常数K随温度升高而___(填“增大”或“减小”).
②温度过高或过低均不利于该反应的进行,原因是___.
③200℃达到平衡时体系的总压强为p,该反应平衡常数Kp的计算式为___.(不必化简.用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
(2)Sabatier反应在空间站运行时,下列措施能提高CO2转化效率的是___(填标号).
A.适当减压
B.增大催化剂的比表面积
C.反应器前段加热,后段冷却
D.提高原料气中CO2所占比例
E.合理控制反应器中气体的流速
(3)一种新的循环利用方案是用Bosch反应CO2(g)+2H2(g)⇌C(s)+2H2O(g)代替Sabatier反应.
①已知CO2(g)、H2O(g)的生成焓分别为-394kJ•mol-1、-242kJ•mol-1,Bosch反应的△H=___kJ•mol-1.(生成焓指一定条件下由对应单质生成1mol化合物时的反应热)
②一定条件下Bosch反应必须在高温下才能启动,原因是___.
③新方案的优点是___.
CO2(g)+4H2(g)⇌CH4(g)+2H2O(g)
水电解反应:2H2O(l)
| ||

(1)将原料气按n(CO2):nH2=1:4置于密闭容器中发生Sabatier反应,测得H2O(g)的物质的量分数与温度的关系如图所示(虚线表示平衡曲线).
①该反应的平衡常数K随温度升高而___(填“增大”或“减小”).
②温度过高或过低均不利于该反应的进行,原因是___.
③200℃达到平衡时体系的总压强为p,该反应平衡常数Kp的计算式为___.(不必化简.用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
(2)Sabatier反应在空间站运行时,下列措施能提高CO2转化效率的是___(填标号).
A.适当减压
B.增大催化剂的比表面积
C.反应器前段加热,后段冷却
D.提高原料气中CO2所占比例
E.合理控制反应器中气体的流速
(3)一种新的循环利用方案是用Bosch反应CO2(g)+2H2(g)⇌C(s)+2H2O(g)代替Sabatier反应.
①已知CO2(g)、H2O(g)的生成焓分别为-394kJ•mol-1、-242kJ•mol-1,Bosch反应的△H=___kJ•mol-1.(生成焓指一定条件下由对应单质生成1mol化合物时的反应热)
②一定条件下Bosch反应必须在高温下才能启动,原因是___.
③新方案的优点是___.
▼优质解答
答案和解析
(1)①根据图知,当反应达到平衡状态后,升高温度,水的物质的量分数减小,说明平衡逆向移动,则生成物浓度减小、反应物浓度增大,所以化学平衡常数减小,故答案为:减小;
②温度过低,化学反应速率小;温度过高,平衡逆向移动,反应向右进行的程度减小,所以温度过高或过低均不利于该反应的进行,
故答案为:温度过低,反应速率小;温度过高,反应向右进行的程度小;
③设开始时n(CO2)为1mol、n(H2)=4mol,
设参加反应的n(CO2)为xmol,
该反应方程式CO2(g)+4H2(g)⇌CH4(g)+2H2O(g)
开始(mol)1 4 0 0
反应(mol)x 4x x 2x
平衡(mol)1-x 4-4x x 2x
水蒸气的物质的量分数=
=0.6,x=
P(CO2)=P×
=0.02P、P(H2)=
×P=0.08P、P(CH4)=
×P=0.3P、P(H2O)=
×P=0.6P,
压强平衡常数K=
=
,
故答案为:
;
(2)A.适当减压,平衡逆向移动,二氧化碳转化率减小,故A错误;
B.增大催化剂的比表面积,反应物浓度增大,平衡正向移动,二氧化碳转化率增大,故B正确;
C.反应器前段加热,后段冷却,平衡正向移动,二氧化碳转化率增大,故C正确;
D.提高原料气中CO2所占比例,平衡正向移动,但二氧化碳转化率减小,故D错误;
E.合理控制反应器中气体的流速,相当于增大浓度,平衡正向移动,二氧化碳转化率增大,故E正确;
故选BCE;
(3)①Bosch反应的△H=2(-242kJ•mol-1)-(-394kJ•mol-1)=-90kJ/mol,
故答案为:-90;
②断裂二氧化碳和氢气所需的能量较高,所以该反应所需的活化能较高,则一定条件下Bosch反应必须在高温下才能启动,故答案为:反应的活化能高;
③该反应中氢元素完全转化为水,氢原子利用率为100%,
故答案为:氢原子利用率为100%.
②温度过低,化学反应速率小;温度过高,平衡逆向移动,反应向右进行的程度减小,所以温度过高或过低均不利于该反应的进行,
故答案为:温度过低,反应速率小;温度过高,反应向右进行的程度小;
③设开始时n(CO2)为1mol、n(H2)=4mol,
设参加反应的n(CO2)为xmol,
该反应方程式CO2(g)+4H2(g)⇌CH4(g)+2H2O(g)
开始(mol)1 4 0 0
反应(mol)x 4x x 2x
平衡(mol)1-x 4-4x x 2x
水蒸气的物质的量分数=
| 2x |
| 1-x+4-4x+x+2x |
| 15 |
| 16 |
P(CO2)=P×
1-
| ||
5-2×
|
4×(1-
| ||
5-2×
|
| ||
5-2×
|
2×
| ||
2-5×
|
压强平衡常数K=
| P(CH4).P2(H2O) |
| P(CO2).P4(H2) |
| 0.3P×(0.6P)2 |
| 0.02P×(0.08P)4 |
故答案为:
| 0.3P×(0.6P)2 |
| 0.02P×(0.08P)4 |
(2)A.适当减压,平衡逆向移动,二氧化碳转化率减小,故A错误;
B.增大催化剂的比表面积,反应物浓度增大,平衡正向移动,二氧化碳转化率增大,故B正确;
C.反应器前段加热,后段冷却,平衡正向移动,二氧化碳转化率增大,故C正确;
D.提高原料气中CO2所占比例,平衡正向移动,但二氧化碳转化率减小,故D错误;
E.合理控制反应器中气体的流速,相当于增大浓度,平衡正向移动,二氧化碳转化率增大,故E正确;
故选BCE;
(3)①Bosch反应的△H=2(-242kJ•mol-1)-(-394kJ•mol-1)=-90kJ/mol,
故答案为:-90;
②断裂二氧化碳和氢气所需的能量较高,所以该反应所需的活化能较高,则一定条件下Bosch反应必须在高温下才能启动,故答案为:反应的活化能高;
③该反应中氢元素完全转化为水,氢原子利用率为100%,
故答案为:氢原子利用率为100%.
看了 航天员呼吸产生的CO2用下列...的网友还看了以下:
如果f(t)=t/(1+t),g(t)=t/(1-t),证明:证明:f(t)-g(t)=-2g(t 2020-05-23 …
2、构成双链DNA分子的四种碱基之间的关系,下列哪项因物种而异()A、(A+C)/(T+G)B、( 2020-06-03 …
关于微积分设f(x),g(x)在[a,b]上连续,在(a,b)内可微,证明存在t∈(a,b),使f 2020-06-10 …
∫(1,x^2)(x^2-t)g(t)dt这积分怎么求导?我有点奇怪我知道变上限积分,因为是对t求 2020-06-10 …
吊在大厅天花板上的电扇重力为G,静止时竖直固定杆对它的拉力为T;扇叶水平转动起来后,杆对它的拉力为 2020-06-12 …
假设一物体从飞机上扔下,t秒后物体的下落速度近似为:v(t)=g(1-e^-kt)/k,(g=9. 2020-06-16 …
如果下面的DNA双螺旋从左向右进行转录,指出那条链是编码链.并写出转录产物的顺序?5’-A-T-C 2020-06-26 …
matlab求解二阶导数方程,四个方程四个未知量>>symst>>E=32;G=10.81;b=2 2020-07-19 …
设f(x),g(x)在[a,b]上连续,在(a,b)内可导,且g(x)不等于0,f(a)g(b)= 2020-07-21 …
碱基计算的规律.①A等于T,G等于C,A+G=T+CA+G/T+C等1.②一条单链的A+G/T+C的 2020-11-27 …