早教吧作业答案频道 -->化学-->
某校化学小组对热水壶底部水垢的主要成分进行了如下探究,请完成以下活动并回答相关问题.查阅资料天然水中含有Ca2+、Mg2+、HCO3-等离子,在加热条件下,这些离子趋于生成溶解度更
题目详情
某校化学小组对热水壶底部水垢的主要成分进行了如下探究,请完成以下活动并回答相关问题.
【查阅资料】天然水中含有Ca2+、Mg2+、HCO3-等离子,在加热条件下,这些离子趋于生成溶解度更小的物质--水垢(主要成分为碳酸盐和碱).有关物质的溶解性见下表:
部分钙、镁化合物溶解性表(20℃)
【提出猜想】水垢的主要成分中一定含有
___和___,可能含有Ca(OH)2和MgCO3(填化学式).
【设计方案】
实验1:确定水垢中是否含Ca(OH)2和CaCO3
实验2:确定水垢中是否含MgCO3
利用下列实验装置,完成实验2探究.其主要实验步骤如下:
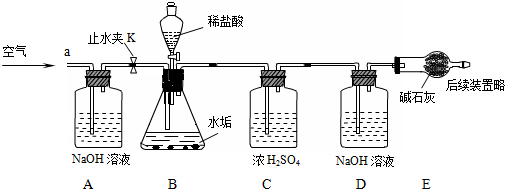
称量D、E装置总质量为200.0g,按上图组装后,将2.5g水垢试样放入锥形瓶中,加入足量稀盐酸溶液,待锥形瓶中不再产生气泡时,打开止水夹K,从导管a处缓缓鼓入空气,一段时间后称量装置D、E的总质量为201.25g(碱石灰主要成分为CaO和NaOH,不考虑装置内空气对实验的影响).
【实验讨论】
(1)加入样品前还应___,装置B中盛放稀盐酸的仪器名称为___,装置C的作用是___,反应结束后打开止水夹K,缓缓鼓入空气的目的是___,装置A的作用是___.A、B装置之间___设置干燥装置(填“要”、“不要”),其理由是___.
(2)装置B中生成气体的化学反应方程式为___(只要求写一种)
装置D中的化学反应方程式为___.
(3)装置B中生成CO2的质量为___ g.通过计算说明水垢中___含MgCO3(填字母).
A.一定 B.一定不 C.可能 D.无法确定
计算过程(已知CaCO3相对分子质量为100、MgCO3相对分子质量为84):
实验3:确定水垢中是否含有Mg(OH)2
另取质量为2.50g水垢,加3.65%稀盐酸与之反应,测得消耗稀盐酸w g.结合以上实验,判断当w的值满足___ 条件时,水垢中一定含有Mg(OH)2(请通过计算说明).
【查阅资料】天然水中含有Ca2+、Mg2+、HCO3-等离子,在加热条件下,这些离子趋于生成溶解度更小的物质--水垢(主要成分为碳酸盐和碱).有关物质的溶解性见下表:
部分钙、镁化合物溶解性表(20℃)
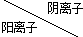 | OH- | CO32- | HCO3- |
| Ca2+ | 微溶 | 不溶 | 可溶 |
| Mg2+ | 不溶 | 微溶 | 可溶 |
___和___,可能含有Ca(OH)2和MgCO3(填化学式).
【设计方案】
实验1:确定水垢中是否含Ca(OH)2和CaCO3
| 实验步骤 | 实验现象 | 结论 |
| 在少量研碎的水垢中,加入适量的蒸馏水充分搅拌,过滤,在滤液里加入Na2CO3溶液. | 没有白色沉淀产生 | ___ |
利用下列实验装置,完成实验2探究.其主要实验步骤如下:

称量D、E装置总质量为200.0g,按上图组装后,将2.5g水垢试样放入锥形瓶中,加入足量稀盐酸溶液,待锥形瓶中不再产生气泡时,打开止水夹K,从导管a处缓缓鼓入空气,一段时间后称量装置D、E的总质量为201.25g(碱石灰主要成分为CaO和NaOH,不考虑装置内空气对实验的影响).
【实验讨论】
(1)加入样品前还应___,装置B中盛放稀盐酸的仪器名称为___,装置C的作用是___,反应结束后打开止水夹K,缓缓鼓入空气的目的是___,装置A的作用是___.A、B装置之间___设置干燥装置(填“要”、“不要”),其理由是___.
(2)装置B中生成气体的化学反应方程式为___(只要求写一种)
装置D中的化学反应方程式为___.
(3)装置B中生成CO2的质量为___ g.通过计算说明水垢中___含MgCO3(填字母).
A.一定 B.一定不 C.可能 D.无法确定
计算过程(已知CaCO3相对分子质量为100、MgCO3相对分子质量为84):
实验3:确定水垢中是否含有Mg(OH)2
另取质量为2.50g水垢,加3.65%稀盐酸与之反应,测得消耗稀盐酸w g.结合以上实验,判断当w的值满足___ 条件时,水垢中一定含有Mg(OH)2(请通过计算说明).
▼优质解答
答案和解析
【提出猜想】由题中溶解性表知碳酸钙和氢氧化镁不溶于水,其余的氢氧化钙、碳酸镁微溶,碳酸氢钙和碳酸氢镁都溶于水,故水垢的主要成分中一定含有:CaCO3、Mg(OH)2故填:CaCO3;Mg(OH)2;
【设计方案】
实验1:氢氧化钙溶液能和碳酸钠反应生成碳酸钙沉淀,所以
故填:没有氢氧化钙;
【实验讨论】:(1)因为实验需要测定生成的二氧化碳的质量,需要保证装置不漏气,所以需要检查装置的气密性;装置B中盛放稀盐酸的仪器名称为分液漏斗;浓硫酸具有吸水性,所以装置C的作用是除去二氧化碳中含有的水蒸气;反应结束后打开止水夹K,缓缓鼓入空气是为了将装置中的二氧化碳全部吸收;装置A的作用是吸收空气中的二氧化碳.A、B装置之间不要设置干燥装置,其理由是C装置可以除去二氧化碳的水蒸气;
故填:检查装置的气密性;分液漏斗;除去二氧化碳中含有的水蒸气;将残留在装置中的二氧化碳全部排入D、E装置中充分吸收;吸收空气中的二氧化碳;
C装置可以除去二氧化碳的水蒸气;
(2)装置B中是碳酸钙能与盐酸反应生成氯化钙、水和二氧化碳,而D中是二氧化碳和氢氧化钠溶液反应生成碳酸钠和水;故填:CaCO3+2HCl=CaCl2+H2O+CO2↑;CO2+2NaOH═Na2CO3+H2O;
(3)反应前后D、E装置的质量差为:604.4g-600g=4.4g,设生成4.4g二氧化碳需要碳酸钙的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 4.4g
=
解得x=10g,而水垢的质量为9.8g,故一定含有能生成二氧化碳的碳酸镁存在;故填:4.4;A;
实验3:由实验2可知:2.5g水垢与盐酸反应生成1.25g二氧化碳;据碳酸钙、碳酸镁与盐酸反应方程式可知生成1.25g二氧化碳恰好需要3.65%的稀盐酸的质量;
设需要稀盐酸的质量是x,由CaCO3+2HCl=CaCl2+H2O+CO2↑,MgCO3+2HCl=MgCl2+H2O+CO2↑可知:
2HCl~CO2
73 44
3.65%×x 1.25g
=
x=56.8g
由CaCO3+2HCl=CaCl2+H2O+CO2↑,MgCO3+2HCl=MgCl2+H2O+CO2↑,Mg(OH)2+2HCl=MgCl2+2H2O可知:
CaCO3~2HCl~MgCO3~Mg(OH)2;
100 73 84 58
可知:等质量的碳酸镁、碳酸钙、氢氧化镁,氢氧化镁消耗盐酸质量最多,所以当实际消耗盐酸质量大于56.8时,水垢中一定含有氢氧化镁.故填:w>56.8.
【设计方案】
实验1:氢氧化钙溶液能和碳酸钠反应生成碳酸钙沉淀,所以
| 实验步骤 | 实验现象 | 结论 |
| 在少量研碎的水垢中,加入适量的蒸馏水充分搅拌,过滤,在滤液里加入Na2CO3溶液. | 没有白色沉淀产生 | 没有氢氧化钙 |
【实验讨论】:(1)因为实验需要测定生成的二氧化碳的质量,需要保证装置不漏气,所以需要检查装置的气密性;装置B中盛放稀盐酸的仪器名称为分液漏斗;浓硫酸具有吸水性,所以装置C的作用是除去二氧化碳中含有的水蒸气;反应结束后打开止水夹K,缓缓鼓入空气是为了将装置中的二氧化碳全部吸收;装置A的作用是吸收空气中的二氧化碳.A、B装置之间不要设置干燥装置,其理由是C装置可以除去二氧化碳的水蒸气;
故填:检查装置的气密性;分液漏斗;除去二氧化碳中含有的水蒸气;将残留在装置中的二氧化碳全部排入D、E装置中充分吸收;吸收空气中的二氧化碳;
C装置可以除去二氧化碳的水蒸气;
(2)装置B中是碳酸钙能与盐酸反应生成氯化钙、水和二氧化碳,而D中是二氧化碳和氢氧化钠溶液反应生成碳酸钠和水;故填:CaCO3+2HCl=CaCl2+H2O+CO2↑;CO2+2NaOH═Na2CO3+H2O;
(3)反应前后D、E装置的质量差为:604.4g-600g=4.4g,设生成4.4g二氧化碳需要碳酸钙的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 4.4g
| 100 |
| x |
| 44 |
| 4.4g |
解得x=10g,而水垢的质量为9.8g,故一定含有能生成二氧化碳的碳酸镁存在;故填:4.4;A;
实验3:由实验2可知:2.5g水垢与盐酸反应生成1.25g二氧化碳;据碳酸钙、碳酸镁与盐酸反应方程式可知生成1.25g二氧化碳恰好需要3.65%的稀盐酸的质量;
设需要稀盐酸的质量是x,由CaCO3+2HCl=CaCl2+H2O+CO2↑,MgCO3+2HCl=MgCl2+H2O+CO2↑可知:
2HCl~CO2
73 44
3.65%×x 1.25g
| 73 |
| 3.65%×x |
| 44 |
| 1.25g |
x=56.8g
由CaCO3+2HCl=CaCl2+H2O+CO2↑,MgCO3+2HCl=MgCl2+H2O+CO2↑,Mg(OH)2+2HCl=MgCl2+2H2O可知:
CaCO3~2HCl~MgCO3~Mg(OH)2;
100 73 84 58
可知:等质量的碳酸镁、碳酸钙、氢氧化镁,氢氧化镁消耗盐酸质量最多,所以当实际消耗盐酸质量大于56.8时,水垢中一定含有氢氧化镁.故填:w>56.8.
看了 某校化学小组对热水壶底部水垢...的网友还看了以下:
英语翻译21世纪是一个数字化的世纪,网络化、全球化成为世界经济发展的必然趋势.在数字化时代里,谁先 2020-04-27 …
(2013•长清区二模)能源“非石油化”是战略目标,发展以CH4、CO2等为原料的“C1化学”成为 2020-06-15 …
氧化还原反应元素的化合价有没有趋向性?最稳定的价态是什么样的价态既然趋向性是趋向最稳定的价态,那为 2020-07-01 …
下列句子中加点成语使用不恰当的一项是()A.在全球经济一体化成为大趋势的今天,“与国际接轨”成为一 2020-07-23 …
英语翻译随着全球贸易的飞速发展和世界经济一体化趋势的不断加强,会计国际化已成为世界各国普遍关注的现 2020-07-25 …
a趋近于0,a/x也趋近于0吗?这是一个在导数的证明里看见的,先前是a趋近于0,但到后来令t=a/x 2020-11-11 …
据有关研究,汽车所用燃料的60%是消耗于汽车自身质量,汽车自身质量每降低100kg,每百公里油耗可减 2020-11-24 …
下列句子中加粗成语使用不恰当的一项是[]A.在全球经济一体化成为大趋势的今天,“与国际接轨”成为一个 2020-11-24 …
近年来,随着全球对能源需求的日益膨胀,由近海走向深海已成为发展海洋能源和经济的必然趋势和重大战略部署 2020-11-25 …
下列各句中加点成语使用不恰当的一句是()A.在经济一体化成为大趋势的今天,“与国际接轨”成为一个自强 2020-12-22 …