含有Ca2+、Mg2+、的水在加热过程中会发生如下反应而形成水垢:Ca(HCO3)2CaCO3↓+CO2↑+H2O,Mg(HCO3)2MgCO3↓+CO2↑+H2OMgCO3+H2OMg(OH)2+CO2↑某学生为研究水
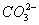 的水在加热过程中会发生如下反应而形成水垢:
的水在加热过程中会发生如下反应而形成水垢:
Ca(HCO 3 ) 2  CaCO 3 ↓+CO 2 ↑+H 2 O,
CaCO 3 ↓+CO 2 ↑+H 2 O,
Mg(HCO 3 ) 2 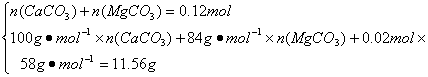 MgCO 3 ↓+CO 2 ↑+H 2 O
MgCO 3 ↓+CO 2 ↑+H 2 O
MgCO 3 +H 2 O 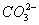 Mg(OH) 2 +CO 2 ↑
Mg(OH) 2 +CO 2 ↑
某学生为研究水垢的成分,取一定量水垢经加热使其失去结晶水并干燥后称得质量为
(1)通过计算确定水垢中是否含有碳酸镁。
(2)残留固体经冷却后称得质量为
解析:
(1)n()=n(CO2)=n(BaCO3)==0.12 mol。若水垢中不含MgCO3,则全部为CaCO3。m(CaCO3)=0.12 mol×100 g·mol-1=12.00 g>11.56 g。故一定含有MgCO3。(2)m(H2O)=11.56 g-5.92 g-0.12 mol×44 g·mol-1=0.36 gn(H2O)==0.02 mol所以
1)含2molNaCO3的溶液中含molNa+,有个CO2-..2)含有2.408×10*24个H 2020-04-13 …
1、有浓度24%的硫酸溶液72千克,要使硫酸溶液的浓度变为36%,需要加入硫酸多少千克?2、有含盐 2020-05-15 …
水果为什么能发电?醋也能发电吗?是不是所有含有酸性的物质都可以发电?我知道柠檬等水果可以发电,请问 2020-06-06 …
现有含酒精70%及含酒精98%的两种酒精,问各取多少可配成含酒精84%的酒精100千克?2.有含盐 2020-06-18 …
有一在空气中放置了一段时间的KOH固体,经分析测知其含水2.8%\含K2CO3取1克该样品投入25 2020-06-28 …
使372()既含有因数2,又含有因数5,括号中可以是()。同时是2,3和5使372()既含有因数2 2020-07-13 …
求助P(B|A)=1为什么不能推出B包含A?1、P(B|A)=1为什么不能推出B包含A?2、“当A 2020-07-14 …
求含元音字母且发元音的开音和闭音比如:A|ei|就是含有A且发|ei|的音的单词越多越好如:lat 2020-07-14 …
1mol/LBa(OH)2溶液的含义是[]A.1L水中含有1molBa(OH)2B.1L溶液中含有 2020-07-18 …
①有含药85%的农药5斤,应该加入多少斤水,才能配置成含药2%的农药?②有铜和银的合金200克,其中 2020-11-01 …