早教吧作业答案频道 -->化学-->
用黑钨矿[FeWO4、MnWO4(W为+6价)]结合其它化工生产高纯钨的化工流程如图1.已知H2WO4是不溶于水的弱酸,受热可分解生成氧化物.请回答下列有关问题:(1)上述流程中通入空气的目的是
题目详情
用黑钨矿[FeWO4、MnWO4(W为+6价)]结合其它化工生产高纯钨的化工流程如图1.已知H2WO4是不溶于水的弱酸,受热可分解生成氧化物.请回答下列有关问题:
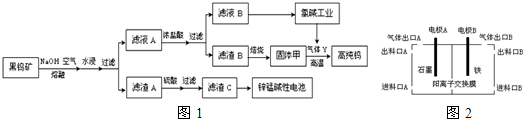
(1)上述流程中通入空气的目的是___;
(2)滤渣A为黑色,其与硫酸反应的离子方程式为___;
滤液A与浓盐酸反应的离子方程式为___;
(3)实验室用锌锰碱性电池做电源模拟氯碱工业的装置如图2:
已知:锌锰碱性电池的总反应为Zn+2MnO2+2H2O=Zn(OH)2+2MnOOH,写出锌锰碱性电池正极反应式___;则锌锰碱性电池的锌电极应与装置中电极___(填“A”或“B”)相接,进料口A的物质为___,若锌电极消耗6.5g时产生的气体Y理论上能还原固体甲得到___g纯钨(保留一位小数).[Mr(W)=184]
(4)已知单质碳也可与固体甲制得钨,用气体Y而不用单质碳的原因___;
(5)常温下,黑钨矿中FeWO4和MnWO4的溶度积常数分别为:Ksp(FeWO4)=2.5×10-12;Ksp(MnWO4)=7.5×10-16;欲将体积为1L含MnWO4物质的量为0.6mol悬浊液全部转化为FeWO4悬浊液,理论上可往MnWO4悬浊液加入等体积一定浓度的FeCl2溶液完成上述转化;请计算所加入FeCl2溶液浓度为___mol/L.(溶液混合体积变化可忽略)

(1)上述流程中通入空气的目的是___;
(2)滤渣A为黑色,其与硫酸反应的离子方程式为___;
滤液A与浓盐酸反应的离子方程式为___;
(3)实验室用锌锰碱性电池做电源模拟氯碱工业的装置如图2:
已知:锌锰碱性电池的总反应为Zn+2MnO2+2H2O=Zn(OH)2+2MnOOH,写出锌锰碱性电池正极反应式___;则锌锰碱性电池的锌电极应与装置中电极___(填“A”或“B”)相接,进料口A的物质为___,若锌电极消耗6.5g时产生的气体Y理论上能还原固体甲得到___g纯钨(保留一位小数).[Mr(W)=184]
(4)已知单质碳也可与固体甲制得钨,用气体Y而不用单质碳的原因___;
(5)常温下,黑钨矿中FeWO4和MnWO4的溶度积常数分别为:Ksp(FeWO4)=2.5×10-12;Ksp(MnWO4)=7.5×10-16;欲将体积为1L含MnWO4物质的量为0.6mol悬浊液全部转化为FeWO4悬浊液,理论上可往MnWO4悬浊液加入等体积一定浓度的FeCl2溶液完成上述转化;请计算所加入FeCl2溶液浓度为___mol/L.(溶液混合体积变化可忽略)
▼优质解答
答案和解析
黑钨矿通入空气与氢氧化钠在熔融状态下反应生成MnO2、Fe2O3、Fe3O4、Na2WO4,加水溶解、过滤,滤渣A含有MnO2、Fe3O4,加入硫酸,Fe3O4溶解,滤渣C为MnO2,可用于锌锰碱性电池,滤液A含有Na2WO4,加入盐酸可生成H2WO4沉淀,灼烧生成WO3,滤液B含有NaCl,电解饱和食盐水生成氢气,可用于高温下与WO3反应生成W,
(1)上述流程中通入空气可氧化Fe2+、Mn2+,故答案为:氧化Fe2+、Mn2+;
(2)滤渣A含有MnO2、Fe3O4,加入硫酸,Fe3O4溶解,反应的离子方程式为Fe3O4+8H+=2Fe3++Fe2+4H2O;滤液A中含有WO42-,与氢离子反应生成H2WO4沉淀,反应的离子方程式为:WO42-+2H+=H2WO4↓;
故答案为:Fe3O4+8H+=2Fe3++Fe2+4H2O;WO42-+2H+=H2WO4↓;
(3)锌锰碱性电池的正极上二氧化锰得电子生成MnOOH,则电池正极反应式为MnO2+e-+H2O=MnOOH+OH-,电解饱和食盐水,石墨为阳极,铁为阴极,锌锰碱性电池的锌电极应与装置中电极B相连,氢气在阴极生成,从出口B出来,且阴极生成氢氧化钠;从进料口A加入的物质为精制饱和食盐水,
根据电子守恒可知,Zn~2e-~H2~
WO3 ~
W
65
×184
6.5g m(W)
则m(W)=
=6.1g,
故答案为:MnO2+e-+H2O=MnOOH+OH-;B;精制饱和食盐水;6.1;
(4)单质碳也可与固体WO3制得钨,但易引入杂质碳,且生成碳化钨,故答案为:会引入杂质碳,会生成碳化钨;
(5)根据Ksp(FeWO4)=c(Fe2+)•c(WO42-)=2.5×10-12,Ksp(MnWO4)=7.5×10-16,体积为1L含MnWO4物质的量为0.6mol,则溶液中c(WO42-)=
=1.25×10-15,c(Fe2+)=
=
=2000mol/L,
故答案为:2000.
(1)上述流程中通入空气可氧化Fe2+、Mn2+,故答案为:氧化Fe2+、Mn2+;
(2)滤渣A含有MnO2、Fe3O4,加入硫酸,Fe3O4溶解,反应的离子方程式为Fe3O4+8H+=2Fe3++Fe2+4H2O;滤液A中含有WO42-,与氢离子反应生成H2WO4沉淀,反应的离子方程式为:WO42-+2H+=H2WO4↓;
故答案为:Fe3O4+8H+=2Fe3++Fe2+4H2O;WO42-+2H+=H2WO4↓;
(3)锌锰碱性电池的正极上二氧化锰得电子生成MnOOH,则电池正极反应式为MnO2+e-+H2O=MnOOH+OH-,电解饱和食盐水,石墨为阳极,铁为阴极,锌锰碱性电池的锌电极应与装置中电极B相连,氢气在阴极生成,从出口B出来,且阴极生成氢氧化钠;从进料口A加入的物质为精制饱和食盐水,
根据电子守恒可知,Zn~2e-~H2~
| 1 |
| 3 |
| 1 |
| 3 |
65
| 1 |
| 3 |
6.5g m(W)
则m(W)=
6.5g×
| ||
| 65 |
故答案为:MnO2+e-+H2O=MnOOH+OH-;B;精制饱和食盐水;6.1;
(4)单质碳也可与固体WO3制得钨,但易引入杂质碳,且生成碳化钨,故答案为:会引入杂质碳,会生成碳化钨;
(5)根据Ksp(FeWO4)=c(Fe2+)•c(WO42-)=2.5×10-12,Ksp(MnWO4)=7.5×10-16,体积为1L含MnWO4物质的量为0.6mol,则溶液中c(WO42-)=
| 7.5×10-16 |
| 0.6 |
| Ksp |
| c(WO42-) |
| 2.5×10-12 |
| 1.25×10-15 |
故答案为:2000.
看了 用黑钨矿[FeWO4、MnW...的网友还看了以下:
宇宙是真空的吗?书上说在一个完全没有任何空气的环境下就是真空,可是真空是不可能存在的,因为没有空气 2020-04-27 …
孙悟空师傅扫完金光塔后,师傅累得已是满头大汗,八戒见状,忙端上茶去献殷勤,并关心地问道:师傅,您这 2020-05-13 …
孙悟空师傅扫完金光塔后,师傅累得已是满头大汗,八戒见状,忙端上茶去献殷勤,并关心地问道:师傅,您这 2020-05-13 …
对诗不太了解.求助中.前天发来;眼里已是匆匆客,眉间却留一段情.青鸟殷勤飞云渡,莫做幽人寂寞吟.今 2020-05-13 …
这是什么修辞手法?1.“雨停了一会儿,又下一阵儿,比以前小了许多,祥子一口气跑回了家.”2.“茶从 2020-05-14 …
10.补写出下列句子中的空缺部分。(10分)(1)往事不堪回首,纵回首已是惘然,这是人类共有的情感 2020-06-09 …
两个集合并集是空集,这两个集合是空集么是不是只有两个集合都为空集的时候他们的并集才是空集,也就是两 2020-06-22 …
《拾穗的脚步》①迈着匆匆的脚步回到乡下,已是晌午时分,午后的阳光,火辣辣的,没有一丝阴凉。正是稻子 2020-06-28 …
《拾穗的脚步》(1)迈着匆匆的脚步回到乡下,已是晌午时分,午后的阳光,火辣辣的,没有一丝阴凉。正是 2020-06-28 …
英语翻译天天听都不知道是怎么写的,决心学会,它们是:您所拨打的用户已关机,请稍候再拨;您所拨打的用 2020-06-30 …