早教吧作业答案频道 -->化学-->
五种短周期元素的部分性质数据如下:元素TXYZW原子半径(nm)0.0370.0750.0990.1020.143最高或最低化合价+1+5,-3+7,-1+6,-2+3(1)Z离子的结构示
题目详情
五种短周期元素的部分性质数据如下:
(1)Z离子的结构示意图为___.
(2)关于Y、Z两种元素,下列叙述正确的是___(填序号)
a.简单离子的半径Y>Z b.气态氢化物的稳定性Y比Z强
c.最高价氧化物对应的水化物的酸性Z比Y强
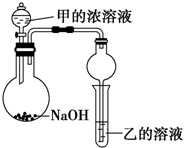
(3)甲是由T、X两种元素形成的10e-分子,乙是由Y、W两种元素形成的化合物.
某同学设计了如图所示装置(夹持仪器省略)进行实验,将甲的浓溶液逐滴加入到NaOH固体中,烧瓶中即有甲放出,原因是___.一段时间后,观察到试管中的现象是___,发生反应的离子方程式是___.
(4)XO2是导致光化学烟雾的“罪魁祸首”之一.它被氢氧化钠溶液吸收的化学方程式是:2XO2+2NaOH═M+NaXO3+H2O(已配平),产物M中元素X的化合价为___.
| 元素 | T | X | Y | Z | W |
| 原子半径(nm) | 0.037 | 0.075 | 0.099 | 0.102 | 0.143 |
| 最高或最低化合价 | +1 | +5,-3 | +7,-1 | +6,-2 | +3 |
(2)关于Y、Z两种元素,下列叙述正确的是___(填序号)
a.简单离子的半径Y>Z b.气态氢化物的稳定性Y比Z强
c.最高价氧化物对应的水化物的酸性Z比Y强
(3)甲是由T、X两种元素形成的10e-分子,乙是由Y、W两种元素形成的化合物.
某同学设计了如图所示装置(夹持仪器省略)进行实验,将甲的浓溶液逐滴加入到NaOH固体中,烧瓶中即有甲放出,原因是___.一段时间后,观察到试管中的现象是___,发生反应的离子方程式是___.
(4)XO2是导致光化学烟雾的“罪魁祸首”之一.它被氢氧化钠溶液吸收的化学方程式是:2XO2+2NaOH═M+NaXO3+H2O(已配平),产物M中元素X的化合价为___.

▼优质解答
答案和解析
五种短周期元素,Y有+7、-1价,则Y为Cl,Z有+6、-2价,则Z为S元素;X有+5、-3价,处于ⅤA族,原子半径小于Cl,故Y为N元素;W有最高正价+3,处于ⅢA族,原子半径大于Cl,故W为Al;T有最高正价+1,处于ⅠA族,原子半径小于N,故T为H元素,
(1)S2-离子的结构示意图为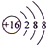 ,故答案为:
,故答案为: ;
;
(2)a.电子层结构相同,核电荷数越大离子半径越小,故离子半径Z(S2-)>Y(Cl-),故a错误;
b.因为Cl比S元素的非金属性强,故HCl比H2S稳定性强,故b正确;
c.因为Cl比S元素的非金属性强,故最高价氧化物对应的水化物的酸性:高氯酸>硫酸,故c错误;
故选:b;
(3)甲是由T、X两种元素形成的10e-分子,则甲为NH3,乙是由Y、W两种元素形成的化合物,乙为AlCl3,将氨水浓溶液逐滴加入到NaOH固体中,NaOH固体可吸收水,并且溶液中OH-浓度增大,可使平衡NH3+H2O⇌NH3•H2O⇌NH4++OH-向左移动,且过程中放热,故有利于NH3放出,一段时间后,试管中发生反应:3NH3.H2O+Al3+=Al(OH)3↓+3NH4+,生成氢氧化铝沉淀,溶液变溶液变浑浊,
故答案为:把浓氨水滴到NaOH固体上,NaOH固体可吸收水,并且溶液中OH-浓度增大,可使平衡NH3+H2O⇌NH3•H2O⇌NH4++OH-向左移动,且过程中放热,故有利于NH3放出;生成白色沉淀;3NH3.H2O+Al3+=Al(OH)3↓+3NH4+;
(4)由2NO2+2NaOH=M+NaNO3+H2O可知,NO2中N元素的化合价+4价,NaNO3中N元素的化合价为+5价,由氧化还原反应中得失电子守恒可知M中N元素的化合价为+3价,故答案为:+3.
(1)S2-离子的结构示意图为
 ,故答案为:
,故答案为: ;
;(2)a.电子层结构相同,核电荷数越大离子半径越小,故离子半径Z(S2-)>Y(Cl-),故a错误;
b.因为Cl比S元素的非金属性强,故HCl比H2S稳定性强,故b正确;
c.因为Cl比S元素的非金属性强,故最高价氧化物对应的水化物的酸性:高氯酸>硫酸,故c错误;
故选:b;
(3)甲是由T、X两种元素形成的10e-分子,则甲为NH3,乙是由Y、W两种元素形成的化合物,乙为AlCl3,将氨水浓溶液逐滴加入到NaOH固体中,NaOH固体可吸收水,并且溶液中OH-浓度增大,可使平衡NH3+H2O⇌NH3•H2O⇌NH4++OH-向左移动,且过程中放热,故有利于NH3放出,一段时间后,试管中发生反应:3NH3.H2O+Al3+=Al(OH)3↓+3NH4+,生成氢氧化铝沉淀,溶液变溶液变浑浊,
故答案为:把浓氨水滴到NaOH固体上,NaOH固体可吸收水,并且溶液中OH-浓度增大,可使平衡NH3+H2O⇌NH3•H2O⇌NH4++OH-向左移动,且过程中放热,故有利于NH3放出;生成白色沉淀;3NH3.H2O+Al3+=Al(OH)3↓+3NH4+;
(4)由2NO2+2NaOH=M+NaNO3+H2O可知,NO2中N元素的化合价+4价,NaNO3中N元素的化合价为+5价,由氧化还原反应中得失电子守恒可知M中N元素的化合价为+3价,故答案为:+3.
看了 五种短周期元素的部分性质数据...的网友还看了以下:
下表是元素周期表的短周期部分,表中字母分别表示一种元素。请回答下列问题:(1)f元素在周期表中的位 2020-04-08 …
(5分)元素周期表是化学学习和研究的重要工具。下图是元素周期表的一部分。(1)6~11号元素中属于 2020-05-13 …
当植物培养液里缺少镁元素,最先变黄的部位是……?以下几个选项可供选择(若有更佳答案,亦可直接给出) 2020-06-05 …
下表中,a、b、c、d、e为元素周期表中前四周期的一部分元素,下列有关叙述正确的是()abcdeA 2020-06-09 …
下表是元素周期表的短周期部分,表中字母分别表示一种元素.请回答下列问题:abcdefg(1)e与f 2020-06-09 …
下表为元素周期表的一部分,列出了10种元素在元素周期表中的位置.试回答下列问题:(1)②、③、④三 2020-06-09 …
一辆公共汽车共载客35人,有一部分人要买2元票,还有一部分买1元票,最后总结出2元票比1元票多收入 2020-07-25 …
小卖部最近进了一批圆规,每个八元,今天共卖出20个,实际卖出时每个10元为标准,超过的记为正,不足记 2020-12-01 …
下列有关元素周期表的说法正确的是()A.元素周期表含元素最多的族是第ⅢB族B.元素周期表有18个族C 2020-12-02 …
乱扔(v.);垃圾;废弃物(n.)底部;最下部(n.)煤;煤块(n.)丑陋的;难看的(adj.)优点 2021-01-01 …