早教吧作业答案频道 -->化学-->
氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点.已知:①CH4(g)+H2O(g)⇌CO(g)+3H2△H=+206.2kJ•mol-1;②CH4(g)+CO2(g)⇌2CO(g)+2H2△H=+247.4kJ•mol-1;③2H2S(g)
题目详情
氢气是一种清洁能源,氢气的制取与储存是氢能源利用领域的研究热点.
已知:①CH4(g)+H2O(g)⇌CO(g)+3H2△H=+206.2kJ•mol-1;
②CH4(g)+CO2(g)⇌2CO(g)+2H2△H=+247.4kJ•mol-1;
③2H2S(g)⇌2H2(g)+S2(g)△H=+169.8kJ•mol-1;
(1)以甲烷为原料制取氢气是工业上常用的制氢方法.CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为___.
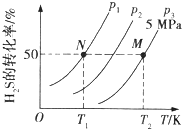
(2)在密闭容器中充入一定量的H2S,发生反应③.如图所示为H2S气体分解生成H2和S2(g)的平衡转化率与温度、压强的关系.
①图中压强(p1、p2、p3)的大小顺序为___,理由是___.
②该反应平衡常数的大小关系为K(T1)___(填“>”、“<”或“=”)K(T2),理由是___.
③图中M点的平衡常数Kp=___MPa-1(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
④如果想进一步提高H2S的转化率,除改变温度、压强外,还可以采取的措施有___.
(3)氢气燃料电池能大幅度提高能量的转化率.甲烷-空气碱性(KOH为电解质)燃料电池的负极反应式为___.相同条件下,甲烷燃料电池与氢气燃料电池的能量密度之比为___ (单位质量的输出电能叫能量密度,能量密度之比等于单位质量的可燃物转移电子数之比).
已知:①CH4(g)+H2O(g)⇌CO(g)+3H2△H=+206.2kJ•mol-1;
②CH4(g)+CO2(g)⇌2CO(g)+2H2△H=+247.4kJ•mol-1;
③2H2S(g)⇌2H2(g)+S2(g)△H=+169.8kJ•mol-1;

(1)以甲烷为原料制取氢气是工业上常用的制氢方法.CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为___.
(2)在密闭容器中充入一定量的H2S,发生反应③.如图所示为H2S气体分解生成H2和S2(g)的平衡转化率与温度、压强的关系.
①图中压强(p1、p2、p3)的大小顺序为___,理由是___.
②该反应平衡常数的大小关系为K(T1)___(填“>”、“<”或“=”)K(T2),理由是___.
③图中M点的平衡常数Kp=___MPa-1(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
④如果想进一步提高H2S的转化率,除改变温度、压强外,还可以采取的措施有___.
(3)氢气燃料电池能大幅度提高能量的转化率.甲烷-空气碱性(KOH为电解质)燃料电池的负极反应式为___.相同条件下,甲烷燃料电池与氢气燃料电池的能量密度之比为___ (单位质量的输出电能叫能量密度,能量密度之比等于单位质量的可燃物转移电子数之比).
▼优质解答
答案和解析
(1)①CH4(g)+H2O(g)═CO(g)+3H2(g)△H=206.2kmol-1
②CH4(g)+CO2(g)═2CO(g)+2H2(g)△H=247.4kJmol-1
据盖斯定律,①×2-②得:CH4(g)+2H2O(g)═CO2(g)+4H2(g)△H=165.0kmol-1,
故答案为:CH4(g)+2H2O(g)═CO2(g)+4H2(g)△H=+165.0kmol-1;
(2)①2H2S(g)⇌2H2(g)+S2(g)△H=+169.8kJ•mol-1,反应是气体体积增大的反应,温度不变,压强增大平衡逆向进行,H2S的转化率减小,则压强关系为:P123,
故答案为:P123,该可逆反应的正反应是气体分子数增大的反应,相同温度下,增大压强平衡逆向进行,H2S的转化率减小;
②反应是吸热反应,平衡移动原理可知,升温平衡正向进行,图分析可知升温H2S的转化率增大,说明升温平衡正向进行,平衡常数增大,K(T1)2),
故答案为:<,该可逆反应的正反应是吸热反应,升高温度,平衡常数增大;
③M点的H2S转化率为50%,总压为5MPa,设H2S起始量为2mol,
2H2S(g)⇌2H2(g)+S2(g)
起始量(mol) 2 0 0
变化量(mol) 1 1 0.5
平衡量(mol) 1 1 0.5
Kp=
=
=1,
故答案为:1;
④如果想进一步提高H2S的转化率,除改变温度、压强外,可以减少生成物浓度促进平衡正向进行,提高硫化氢的转化率,采取的措施有及时分离出产物,
故答案为:及时分离出产物;
(3)甲烷-空气碱性(KOH为电解质)燃料电池的负极反应式为CH4-8e一+10OH-=CO32-+7H20,设甲烷和氢气质量为16g,则预计电极反应计算电子转移总数计算得到能量密度之比,CH4-8e一+10OH-=CO32-+7H20,16g甲烷燃烧电子转移8mol,16g氢气物质的量8mol,电子转移16mol,H2-2e-=2H+,所以相同条件下,甲烷燃料电池与氢气燃料电池的能量密度之比为8:16=1:2,
故答案为:CH4-8e一+10OH-=CO32-+7H20; 1:2.
②CH4(g)+CO2(g)═2CO(g)+2H2(g)△H=247.4kJmol-1
据盖斯定律,①×2-②得:CH4(g)+2H2O(g)═CO2(g)+4H2(g)△H=165.0kmol-1,
故答案为:CH4(g)+2H2O(g)═CO2(g)+4H2(g)△H=+165.0kmol-1;
(2)①2H2S(g)⇌2H2(g)+S2(g)△H=+169.8kJ•mol-1,反应是气体体积增大的反应,温度不变,压强增大平衡逆向进行,H2S的转化率减小,则压强关系为:P1
故答案为:P1
②反应是吸热反应,平衡移动原理可知,升温平衡正向进行,图分析可知升温H2S的转化率增大,说明升温平衡正向进行,平衡常数增大,K(T1)
故答案为:<,该可逆反应的正反应是吸热反应,升高温度,平衡常数增大;
③M点的H2S转化率为50%,总压为5MPa,设H2S起始量为2mol,
2H2S(g)⇌2H2(g)+S2(g)
起始量(mol) 2 0 0
变化量(mol) 1 1 0.5
平衡量(mol) 1 1 0.5
Kp=
| Kp2(H2)Kp(S2) |
| Kp2(H2S) |
(5×
| ||||
(5×
|
故答案为:1;
④如果想进一步提高H2S的转化率,除改变温度、压强外,可以减少生成物浓度促进平衡正向进行,提高硫化氢的转化率,采取的措施有及时分离出产物,
故答案为:及时分离出产物;
(3)甲烷-空气碱性(KOH为电解质)燃料电池的负极反应式为CH4-8e一+10OH-=CO32-+7H20,设甲烷和氢气质量为16g,则预计电极反应计算电子转移总数计算得到能量密度之比,CH4-8e一+10OH-=CO32-+7H20,16g甲烷燃烧电子转移8mol,16g氢气物质的量8mol,电子转移16mol,H2-2e-=2H+,所以相同条件下,甲烷燃料电池与氢气燃料电池的能量密度之比为8:16=1:2,
故答案为:CH4-8e一+10OH-=CO32-+7H20; 1:2.
看了 氢气是一种清洁能源,氢气的制...的网友还看了以下:
小朋友齐打交2.5问题,急~~我才玩,想知道火神和水神,有没有地狱火/水龙这个招?怎么发?有人说是 2020-04-07 …
A.(C, B, D, A, P, E, I, J, G, H)B.(C, B, D, A, E, 2020-05-26 …
A.(A, B, D, C, F, E, I, J, H, G)B.(A, B, D, C, E, 2020-05-26 …
A.(A, B, D, C, P, E, I, J, H, G)B.(A, B, D, C, E, 2020-05-26 …
如图,已知A、B、C、D、E、F、G、H、J、K是10个互不相等的非零自然数,并且A=B+C,B= 2020-06-12 …
二叉树先序序列为E,F,H,I,G,J,K中序序列为H,F,I,E,J,K,G,那么这棵树是怎么排 2020-07-10 …
推断题:现有如下反应(反应条件均不给),推断物质⑴A→B+C+D⑵C+E→C+F+D⑶D+G→H⑷ 2020-07-30 …
如图,三角形ABC内接于圆O,弦AF垂直于BC于点H,G是BF的中点,求证AC=2OG 2020-08-03 …
三元一次方程组a*x+b*y+c*z+d=0,e*x+f*y+g*z+h=0,i*x+j*y+k* 2020-08-03 …
已知一棵二叉树的的中序和后序序列如下,求该二叉树的高度(假定空树的高度为0)和度为2,度为1及度为0 2020-12-05 …