已知H—H键能为436kJ·mol-1,H—N键能为391kJ·mol-1,根据化学方程式:N2+3H22NH3ΔH=-92.4kJ·mol-1,则N≡N键的键能是()A.431kJ·mol-1B.946kJ·mol-1C.649kJ·
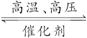 2NH 3 ΔH=-92.4 kJ·mol -1 ,则N≡N键的键能是( )
2NH 3 ΔH=-92.4 kJ·mol -1 ,则N≡N键的键能是( )
A.431 kJ·mol -1 B.946 kJ·mol
解析:
N2+3H22NH3 ΔH=-92.4 kJ·mol-1表示的意义是:1 mol N2与3 mol H2完全反应,生成2 mol NH3放出的热量是92.4 kJ·mol-1,断开1 mol N≡N吸收的能量为X,断开3 mol H—H吸收的能量为3×391 kJ·mol-1=1 173 kJ·mol-1,生成2 mol NH3即6 mol H—N键放出的能量为391 kJ·mol-1×6=2 346 kJ·mol-1,2 346 kJ·mol-1-(X+1 173 kJ·mol-1)=92.4 kJ·mol-1,解得X=946 kJ·mol-1。
谁帮我做下下面的关于时间复杂度的习题?f(n)=100n^3+n^2+1000,g(n)=25n^ 2020-06-12 …
设数列h0,h1,...,hn,...满足递推关系h(n)+h(n-1)-16h(n-2)+20h 2020-06-14 …
这个程序要求是输出m个数中任取n个数的所有组合,我要抓狂了==#include;#includei 2020-06-28 …
请教catalan数网上对catalan数的通项有两种说法一种说catalan数满足递归式:h(n 2020-06-28 …
规定:正整数n的“H运算”是①当n为奇数时,H=3n+13;②当n为偶数时,H=n×12×12×… 2020-07-20 …
已知H-H键键能为436kJ/mol,H-N键键能为391kJ/mol,根据化学方程式:N2+3H 2020-07-20 …
已知H-H键键能为436kJ/mol,H-N键键能为391kJ/mol,根据化学方程式:N2+3H 2020-07-20 …
我们可以通过计算求得:1+2+3+...+n=n*(n+1)除以2,其中n是正整数,现在我们来研究一 2020-12-04 …
按要求回答下列问题:(1)气态SeO3分子的立体构型为,SO32-离子的立体构型为;(2)H+可与N 2020-12-21 …
定义新运算..规定正整数n的“H运算”是:1、当n为奇数时,H=3n+13;2、当n为偶数时,H=n 2021-02-04 …