早教吧作业答案频道 -->化学-->
化学兴趣小组的同学对“影响金属与盐酸反应的剧烈程度的因素”进行了探究.提出问题金属与盐酸反应剧烈程度受哪些因素的影响?作出猜想a.可能与金属本身的性质有关b.可
题目详情
化学兴趣小组的同学对“影响金属与盐酸反应的剧烈程度的因素”进行了探究.
【提出问题】金属与盐酸反应剧烈程度受哪些因素的影响?
【作出猜想】a.可能与金属本身的性质有关
b.可能与盐酸的浓度有关
【设计探究】实验所用金属均已用砂纸打磨.
实验(1)为探究猜想a,小组同学分别在两支试管中放入相同质量的锌片和铁片,然后分别加入等质量、等浓度的稀盐酸,观察到放锌片的试管中立即产生大量气泡,放铁片的试管中只产生少量气泡.写出锌与盐酸发生反应的化学方程式为___.
从实验现象可判断:金属活动性Zn___Fe(填“<”、’“=”或“>”).
【得出结论】金属与盐酸发生反应的剧烈程度与金属本身性质有关,金属的活动性与反应的剧烈程度的关系是___.
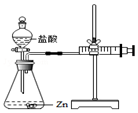
实验(2)为探究猜想b,小组同学设计如上图的装置进行实验,其中注射器的作用是___.
所用药品、实验数据如表:
【得出结论】金属与盐酸发生反应的剧烈程度与盐酸的浓度有关,其关系是___.
【反思评价】根据表中实验Ⅱ数据分析,请解释锌与盐酸发生反应由慢到快、再由快到慢的原因是___.
【拓展延伸】通过以上探究,你认为金属与盐酸反应的剧烈程度还可能与哪些因素有关?请你帮助他们继续探究.(只要求提出一种影响快慢的相关假设因素及实验方案)
【假设】___.
【实验方案】___.
【提出问题】金属与盐酸反应剧烈程度受哪些因素的影响?
【作出猜想】a.可能与金属本身的性质有关
b.可能与盐酸的浓度有关
【设计探究】实验所用金属均已用砂纸打磨.
实验(1)为探究猜想a,小组同学分别在两支试管中放入相同质量的锌片和铁片,然后分别加入等质量、等浓度的稀盐酸,观察到放锌片的试管中立即产生大量气泡,放铁片的试管中只产生少量气泡.写出锌与盐酸发生反应的化学方程式为___.
从实验现象可判断:金属活动性Zn___Fe(填“<”、’“=”或“>”).
【得出结论】金属与盐酸发生反应的剧烈程度与金属本身性质有关,金属的活动性与反应的剧烈程度的关系是___.
实验(2)为探究猜想b,小组同学设计如上图的装置进行实验,其中注射器的作用是___.
所用药品、实验数据如表:
| 实验编号 | 选用金属(均取2g) | 盐酸质量分数(均取50mL) | 每分钟产生氢气的体积/mL | |||||
| 1分钟 | 1-2分钟 | 2-3分钟 | 3-4分钟 | 4-5分钟 | 前5分钟共收集气体 | |||
| Ⅰ | 锌片 | 15% | 2.9 | 16.9 | 11.9 | 9.2 | 7.6 | 48.5 |
| Ⅱ | 锌片 | 5% | 1.6 | 8.4 | 5.9 | 4.8 | 3.7 | 24.4 |
【反思评价】根据表中实验Ⅱ数据分析,请解释锌与盐酸发生反应由慢到快、再由快到慢的原因是___.
【拓展延伸】通过以上探究,你认为金属与盐酸反应的剧烈程度还可能与哪些因素有关?请你帮助他们继续探究.(只要求提出一种影响快慢的相关假设因素及实验方案)
【假设】___.
【实验方案】___.

▼优质解答
答案和解析
【设计探究】由题意知:反应物、生成物,根据质量守恒定律,正确书写化学方程式,锌与盐酸反应的化学方程式为:Zn+2HCl=ZnCl2+H2↑;
放锌片的试管中立即产生大量气泡,放铁片的试管中只产生少量气泡,因此金属活动性强弱为:Zn>Fe;
得出结论:金属与盐酸反应的剧烈程度与金属本身性质有关(金属活动性越强,反应越剧烈);
实验(2)注射器的作用是通过注射器往右移动的体积判断生成氢气的体积;
得出结论:根据表格信息可知,其他条件相同时,盐酸浓度越大,反应越剧烈;
【反思评价】锌与盐酸反应产生气体的速度先加快后变慢,因为锌与盐酸是放热反应,所以开始时温度升高,产生气体速度加快,随着反应的进行,盐酸不断被消耗,浓度降低,产生气体速度变慢;
金属与盐酸反应的剧烈程度可能受温度、金属的颗粒大小、金属的纯度等因素的影响;可以利用控制变量法设计实验为:分别取等质量的锌片和锌粉于试管中,分别加入等体积等浓度的稀盐酸,观察产生气泡的快慢.(假设与方案要对应合理即可);
故答案为:实验(1):Zn+2HCl=ZnCl2+H2↑;>;金属活动性越强,反应越剧烈;
实验(2):通过注射器往右移动的体积测得生成氢气的体积;
其他条件相同时,盐酸浓度越大,反应越剧烈;
【反思评价】原因:锌与稀盐酸反应放热,随着反应的进行,温度升高,所以速度越来越快,一段时间后,盐酸被消耗,盐酸浓度变小,反应速率减慢;
【假设】金属与盐酸反应的剧烈程度与金属表面积大小有关
【实验方案】分别取等质量的锌片和锌粉于试管中,分别加入等体积等浓度的稀盐酸,观察产生气泡的快慢.(假设与方案要对应合理即可)
放锌片的试管中立即产生大量气泡,放铁片的试管中只产生少量气泡,因此金属活动性强弱为:Zn>Fe;
得出结论:金属与盐酸反应的剧烈程度与金属本身性质有关(金属活动性越强,反应越剧烈);
实验(2)注射器的作用是通过注射器往右移动的体积判断生成氢气的体积;
得出结论:根据表格信息可知,其他条件相同时,盐酸浓度越大,反应越剧烈;
【反思评价】锌与盐酸反应产生气体的速度先加快后变慢,因为锌与盐酸是放热反应,所以开始时温度升高,产生气体速度加快,随着反应的进行,盐酸不断被消耗,浓度降低,产生气体速度变慢;
金属与盐酸反应的剧烈程度可能受温度、金属的颗粒大小、金属的纯度等因素的影响;可以利用控制变量法设计实验为:分别取等质量的锌片和锌粉于试管中,分别加入等体积等浓度的稀盐酸,观察产生气泡的快慢.(假设与方案要对应合理即可);
故答案为:实验(1):Zn+2HCl=ZnCl2+H2↑;>;金属活动性越强,反应越剧烈;
实验(2):通过注射器往右移动的体积测得生成氢气的体积;
其他条件相同时,盐酸浓度越大,反应越剧烈;
【反思评价】原因:锌与稀盐酸反应放热,随着反应的进行,温度升高,所以速度越来越快,一段时间后,盐酸被消耗,盐酸浓度变小,反应速率减慢;
【假设】金属与盐酸反应的剧烈程度与金属表面积大小有关
【实验方案】分别取等质量的锌片和锌粉于试管中,分别加入等体积等浓度的稀盐酸,观察产生气泡的快慢.(假设与方案要对应合理即可)
看了 化学兴趣小组的同学对“影响金...的网友还看了以下:
病句周谷城先生早年就投身于轰轰烈烈的"五·四"运动,所以最终成为蜚声海内外的学者我知道前后无关联, 2020-04-06 …
1924~1927年轰轰烈烈的国民革命运动震惊了中国大地,也给当时的北洋军阀以沉重打击,但最后的结 2020-04-06 …
仿写句子人生的价值不在于成就了轰轰烈烈的事业,而在于具体做好什么.所以,见到茂密的森林,你只要无愧 2020-04-06 …
轰轰烈烈的国民大革命兴起了,但革命也潜伏着隐患,据此回答14题:1.北伐战争的历史背景是①革命统一 2020-04-06 …
1航天飞机在升空过程中所穿过大气温度变化是A降升降升B降升降2与火星相比,地球具备生命存在的基本条 2020-04-11 …
关于求逆的.设方阵A满足方程A的平方-A-2E=O(opq的o欧),证明:A及A+2E均可逆,并求 2020-04-27 …
根据以下材料,选取角度,自拟题目,写一篇不少于800字的记叙文。生活是浓烈的,它可以是激烈的比赛、 2020-05-13 …
氢氧化钠具有强烈的腐蚀性,因此它的俗名叫、或.在空气中它可以跟反应,生成,其反应的化学方程式为. 2020-05-15 …
16.已知方程x的方程1/4ax+5/2=7x-3/4的解释正整数,求正整数a的值17.某学校组织 2020-06-03 …
“最强烈的光可以使世界解体.”英文怎么译呢谢谢全句是:“最强烈的光可以使世界解体.在弱的眼睛前面, 2020-06-04 …