早教吧作业答案频道 -->化学-->
以硅孔雀石[主要成分为CuCO3•Cu(OH)2、CuSiO3•2H2O,含SiO2、FeCO3、Fe2O3等杂质]为原料制备CuCl2的工艺流程如图:已知:SOCl2+H2O△.
题目详情
以硅孔雀石[主要成分为CuCO3•Cu(OH)2、CuSiO3•2H2O,含SiO2、FeCO3、Fe2O3等杂质]为原料制备CuCl2的工艺流程如图:
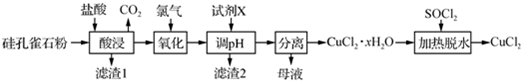
已知:SOCl2+H2O
SO2↑+2HCl↑
(1)“酸浸”时盐酸与CuCO3•Cu(OH)2反应的化学方程式为___.检验“酸浸”后浸出液中的Fe3+可用___溶液.
(2)“氧化”时发生反应的离子方程式为___.
(3)“滤渣2”的主要成分为___(填化学式);“调pH”时,pH不能过高,其原因是___.
(4)“加热脱水”时,加入SOCl2的目的是___.

已知:SOCl2+H2O
| ||
(1)“酸浸”时盐酸与CuCO3•Cu(OH)2反应的化学方程式为___.检验“酸浸”后浸出液中的Fe3+可用___溶液.
(2)“氧化”时发生反应的离子方程式为___.
(3)“滤渣2”的主要成分为___(填化学式);“调pH”时,pH不能过高,其原因是___.
(4)“加热脱水”时,加入SOCl2的目的是___.
▼优质解答
答案和解析
(1)“酸浸”时盐酸与CuCO3•Cu(OH)2反应为复分解反应,由此确定产物配平得化学方程式为CuCO3•Cu(OH)2+4HCl═2CuCl2+CO2↑+3H2O,检验“酸浸”后浸出液中的Fe3+可用KSCN溶液,
故答案为:CuCO3•Cu(OH)2+4HCl═2CuCl2+CO2↑+3H2O;KSCN;
(2)硅孔雀石主要成分为CuCO3•Cu(OH)2、CuSiO3•2H2O,含SiO2、FeCO3、Fe2O3等杂质,根据流程图,加盐酸“酸浸”后溶液中只有Fe2+可被氯气氧化,“氧化”时发生反应的离子方程式为Cl2+2Fe2+═2Fe3++2Cl-,
故答案为:Cl2+2Fe2+═2Fe3++2Cl-;
(3)根据流程图,经氧化后溶液中阳离子主要为Cu2+和Fe3+,加试剂X调节pH使Fe3+完全沉淀而除去,Cu2+仍留在溶液中,实现Cu2+和Fe3+的分离,最终制备CuCl2;“调pH”时,pH不能过高,否则Cu2+转化为Cu(OH)2沉淀,
故答案为:Fe(OH)3 ;防止Cu2+转化为Cu(OH)2沉淀;
(4)由已知:SOCl2+H2O
SO2↑+2HCl↑,“加热脱水”时,加入SOCl2的目的是生成的HCl抑制CuCl2的水解.
故答案为:生成的HCl抑制CuCl2的水解.
故答案为:CuCO3•Cu(OH)2+4HCl═2CuCl2+CO2↑+3H2O;KSCN;
(2)硅孔雀石主要成分为CuCO3•Cu(OH)2、CuSiO3•2H2O,含SiO2、FeCO3、Fe2O3等杂质,根据流程图,加盐酸“酸浸”后溶液中只有Fe2+可被氯气氧化,“氧化”时发生反应的离子方程式为Cl2+2Fe2+═2Fe3++2Cl-,
故答案为:Cl2+2Fe2+═2Fe3++2Cl-;
(3)根据流程图,经氧化后溶液中阳离子主要为Cu2+和Fe3+,加试剂X调节pH使Fe3+完全沉淀而除去,Cu2+仍留在溶液中,实现Cu2+和Fe3+的分离,最终制备CuCl2;“调pH”时,pH不能过高,否则Cu2+转化为Cu(OH)2沉淀,
故答案为:Fe(OH)3 ;防止Cu2+转化为Cu(OH)2沉淀;
(4)由已知:SOCl2+H2O
| ||
故答案为:生成的HCl抑制CuCl2的水解.
看了 以硅孔雀石[主要成分为CuC...的网友还看了以下:
已知球O的球面有四点S,A,B,C,其中O,A,B,C,四点共面,△ABC是边长为2的已知球O的球 2020-04-26 …
已知-1小于等于x小于等于1,n大于等于2,且n属于N正,求证:(1-x)的n次方+(1+x)的n 2020-05-13 …
已知常温下Ca(OH)2的KSP为5.6×10-6,在常温下将适量Ca(OH)2固体溶于100mL 2020-05-13 …
在0.2mol/L Nh4cl和 0.5mol/L氨水混合溶液中 Mg(OH)2的溶解度是多少已知 2020-05-16 …
已知P是抛物线y=2倍(x-2)的平方的对称轴上的一个动点,直线x=t平行于y轴,分别与直线y=x 2020-05-16 …
Cu(NO3)2到Cu(OH)2Cu(OH)2到Cu(NO3)2CuSO4到Cu(OH)2Cu(O 2020-05-17 …
几种常见强碱、中强碱、弱碱的电离平衡常数强碱:NaOH、KOH、CsOH、Ba(OH)2、Tl(O 2020-05-17 …
提问一道电动势的问题(无机化学)已知电对Fe3+/Fe2+的电极电位为0.77V.请用Fe(OH) 2020-05-24 …
化学电池在通讯、交通及日常生活中有着广泛的应用。(1)目前常用的镍镉(NiCd)电池,其电池总反应 2020-06-17 …
化学电源在通讯、交通及日常生活中有着广泛的应用.(1)目前常用的镍(Ni)镉(Cd)电池,其电池总 2020-06-17 …