早教吧作业答案频道 -->化学-->
铜及其化合物在工业上有许多用途.回答下列问题:(1)某工厂以辉铜矿(主要成分为Cu2S,含少量Fe2O3、SiO2等杂质)为原料制备不溶于水的碱式碳酸铜的流程如图1:①浸取反应中氧化剂的
题目详情
铜及其化合物在工业上有许多用途.回答下列问题:
(1)某工厂以辉铜矿(主要成分为Cu2S,含少量Fe2O3、SiO2等杂质)为原料制备不溶于水的碱式碳酸铜的流程如图1:
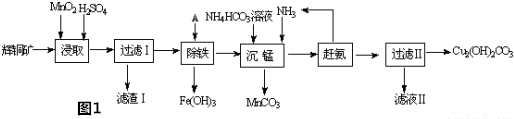
①浸取反应中氧化剂的化学式为___;滤渣Ⅰ的成分为MnO2、S和___(写化学式)
②“除铁”这一步反应在25℃进行,加入试剂A调节溶液PH为4后,溶液中铜离子最大浓度不超过___mol/L.(已知Ksp[Cu(OH)2]=2.2×10-20)
③“沉锰”(除Mn2+)过程中反应的离子方程式___.
④滤液Ⅱ经蒸发结晶得到的盐主要是___(写化学式).
(2)某实验小组同学用电化学原理模拟湿法炼铜,进行了一系列探究活动.
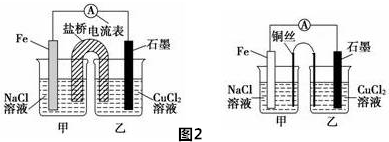
①如图2为某实验小组设计的原电池装置,盐桥内装载的是足量用饱和氯化钾溶液浸泡的琼脂,反应前,电极质量相等,一段时间后,两电极质量相差6.00 g,则导线中通过了___mol电子,若不考虑甲、乙两池电解质溶液中的离子向盐桥中移动,则甲、乙两池电解质溶液的总质量与实验开始前的电解质溶液的总质量相差___g
②其他条件不变,若将盐桥换成光亮的U形弯铜丝浸入甲池与乙池,如图2所示,电流计指针偏转方向与先前一样,但偏转角度明显减小.一段时间后,乙池石墨棒浸入液面以下部分也析出了一层紫红色固体,则甲池铜丝附近溶液的pH___(填“减小”、“增大”或“不变”),乙池中石墨为___极(填“正”、“负”、“阴”或“阳”)
(1)某工厂以辉铜矿(主要成分为Cu2S,含少量Fe2O3、SiO2等杂质)为原料制备不溶于水的碱式碳酸铜的流程如图1:

①浸取反应中氧化剂的化学式为___;滤渣Ⅰ的成分为MnO2、S和___(写化学式)
②“除铁”这一步反应在25℃进行,加入试剂A调节溶液PH为4后,溶液中铜离子最大浓度不超过___mol/L.(已知Ksp[Cu(OH)2]=2.2×10-20)
③“沉锰”(除Mn2+)过程中反应的离子方程式___.
④滤液Ⅱ经蒸发结晶得到的盐主要是___(写化学式).
(2)某实验小组同学用电化学原理模拟湿法炼铜,进行了一系列探究活动.
①如图2为某实验小组设计的原电池装置,盐桥内装载的是足量用饱和氯化钾溶液浸泡的琼脂,反应前,电极质量相等,一段时间后,两电极质量相差6.00 g,则导线中通过了___mol电子,若不考虑甲、乙两池电解质溶液中的离子向盐桥中移动,则甲、乙两池电解质溶液的总质量与实验开始前的电解质溶液的总质量相差___g
②其他条件不变,若将盐桥换成光亮的U形弯铜丝浸入甲池与乙池,如图2所示,电流计指针偏转方向与先前一样,但偏转角度明显减小.一段时间后,乙池石墨棒浸入液面以下部分也析出了一层紫红色固体,则甲池铜丝附近溶液的pH___(填“减小”、“增大”或“不变”),乙池中石墨为___极(填“正”、“负”、“阴”或“阳”)

▼优质解答
答案和解析
(1)①由滤渣1的成份可知反应的化学方程式是:2MnO2+Cu2S+4H2SO4=S↓+2CuSO4+2MnSO4+4H2O,反应中Mn元素化合价降低,被还原,MnO2为氧化剂,因二氧化硅与酸不反应,则滤渣Ⅰ的成分为MnO2、S和SiO2,
故答案为:MnO2;SiO2;
②溶液pH=4,c(OH-)=10-10mol/L,则稀释后的溶液中铜离子浓度最大不能超过
mol/L=2.2 mol/L,
故答案为:2.2 mol/L;
③“沉锰”(除Mn2+)过程中,加入碳酸氢铵和氨气,生成碳酸锰沉淀,反应的离子方程式为Mn2++HCO3-+NH3•H2O=MnCO3↓+NH4++H2O,
故答案为:Mn2++HCO3-+NH3•H2O=MnCO3↓+NH4++H2O;
④滤液Ⅱ主要是硫酸铵溶液通过蒸发浓缩,冷却结晶,过滤洗涤得到硫酸铵晶体,
故答案为:(NH4)2SO4;
(2)①图2为原电池反应,Fe为负极,发生:Fe-2e-=Fe2-,石墨为正极,发生Cu2++2e-=Cu,总反应式为Fe+Cu2+═Fe2++Cu,一段时间后,两电极质量相差6g,
则 Fe+Cu2+═Fe2++Cu 两极质量差△m 转移电子
56g 64g 56g+64g=120g 2mol
6g n
则:n=0.1mol,转移0.1mol,甲池:溶解铁为
×56g/mol=2.8g,溶液增加2.8g,乙池:析出铜
×64g/mol=3.2g,溶液减少3.2g,则甲、乙两池电解质溶液的总质量与实验开始前的电解质溶液的总质量相差3.2g-2.8g=0.4g,
故答案为:0.1;0.4g;
②其他条件不变,若将盐桥换成弯铜导线与石墨相连成n型,则乙装置是电解池,甲装置是原电池,Fe是负极,发生:Fe-2e-=Fe2-,Cu丝是正极,正极发生 O2+2H2O+4e-═4OH-,呈碱性,则甲池铜丝附近溶液的pH增大,乙池中与铜线相连石墨电极是阳极,该极上发生的反应式为2Cl--2e-=Cl2↑,与铁丝相连石墨电极是阴极,发生反应:Cu2++2e-=Cu,
故答案为:增大;阴.
故答案为:MnO2;SiO2;
②溶液pH=4,c(OH-)=10-10mol/L,则稀释后的溶液中铜离子浓度最大不能超过
| 2.2×10-20 |
| (10-10)2 |
故答案为:2.2 mol/L;
③“沉锰”(除Mn2+)过程中,加入碳酸氢铵和氨气,生成碳酸锰沉淀,反应的离子方程式为Mn2++HCO3-+NH3•H2O=MnCO3↓+NH4++H2O,
故答案为:Mn2++HCO3-+NH3•H2O=MnCO3↓+NH4++H2O;
④滤液Ⅱ主要是硫酸铵溶液通过蒸发浓缩,冷却结晶,过滤洗涤得到硫酸铵晶体,
故答案为:(NH4)2SO4;
(2)①图2为原电池反应,Fe为负极,发生:Fe-2e-=Fe2-,石墨为正极,发生Cu2++2e-=Cu,总反应式为Fe+Cu2+═Fe2++Cu,一段时间后,两电极质量相差6g,
则 Fe+Cu2+═Fe2++Cu 两极质量差△m 转移电子
56g 64g 56g+64g=120g 2mol
6g n
则:n=0.1mol,转移0.1mol,甲池:溶解铁为
| 0.1mol |
| 2 |
| 0.1mol |
| 2 |
故答案为:0.1;0.4g;
②其他条件不变,若将盐桥换成弯铜导线与石墨相连成n型,则乙装置是电解池,甲装置是原电池,Fe是负极,发生:Fe-2e-=Fe2-,Cu丝是正极,正极发生 O2+2H2O+4e-═4OH-,呈碱性,则甲池铜丝附近溶液的pH增大,乙池中与铜线相连石墨电极是阳极,该极上发生的反应式为2Cl--2e-=Cl2↑,与铁丝相连石墨电极是阴极,发生反应:Cu2++2e-=Cu,
故答案为:增大;阴.
看了 铜及其化合物在工业上有许多用...的网友还看了以下:
澳大利亚属经济发达国家,也是世界上著名的矿产出口国.澳大利亚大量出口矿产,这能说明该国()A.单一 2020-04-06 …
某科学小组决定测量一块鹅卵石的密度,但是手边的测量工具只有量筒.他们设计了如图所示的实验装置,先把 2020-05-13 …
共同的秘密矿工下井刨煤时,一镐刨在哑炮上.哑炮响了,矿工当场被炸死.因为矿工是临时工,所以矿上只发 2020-05-23 …
共同的秘密》,回答问题矿工队长在安抚完矿工妻子后会对其它十一个矿工会说些什么矿工下井刨煤时,一镐刨 2020-05-23 …
共同的秘密矿工下井刨煤时,一镐刨在哑炮上.哑炮响了,矿工当场被炸死.因为矿工是临时工,所以矿上共同 2020-05-23 …
工程应用题前进矿现有一定量的锡矿,并且每天都挖掘出相同数量的锡矿.如果27辆汽车来运输,6天全部运 2020-06-26 …
共同的秘密1、从此以后指()这个女人指()联系全文看,者不多不少的12个人是()矿工下井刨煤时,一 2020-06-28 …
共同的秘密矿工下井刨煤时,一镐刨在哑炮上,矿工当场被炸死,因为矿工是临时工,所以矿上只发放了一笔抚 2020-07-14 …
阅读理解①矿工下井刨煤时,一镐刨在哑炮上。矿工当场被炸死。因为矿工是临时工,所以矿上只发放了一笔抚 2020-07-14 …
以下为1893-1930年出口原料按经济类别分类比重(百分比),从表中可以看出()年份原料农产品矿产 2020-12-16 …