甲酸(HCOOH)易挥发,熔点为8.6℃,电离常数K=1.8×10-4。某化学兴趣小组进行以下实验。I制取一氧化碳(1)用A图所示装置进行实验。利用浓硫酸的脱水性,将甲酸与浓硫酸混合,甲
甲酸( HCOOH)易挥发,熔点为8.6℃,电离常数K=1.8×10-4。某化学兴趣小组进行以下实验。
I制取一氧化碳
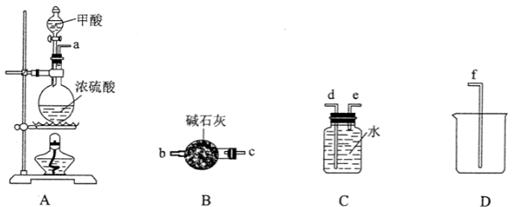
(1)用A图所示装置进行实验。利用浓硫酸的脱水性,将甲酸与浓硫酸混合,甲酸发生分解反应生成CO,反应的化学方程式是____ ;
实验时,不需加热也能产生CO,其原因是 。
(2)欲收集CO气体,连接上图中的装置,其连接顺序为:a→ (按气流方向,用小写字母表示)。
Ⅱ一氧化碳性质的探究
资料:i常温下,CO与PdC12溶液反应,有金属Pd和CO2生成,可用于检验CO;
ii一定条件下,CO能与NaOH固体发生反应:CO+NaOH ![]() HCOONa
HCOONa
利用下列装置进行实验,验证CO具有上述两个性质

(3)打开k2,F装置中发生反应的化学方程式为 ;
为了使气囊收集到纯净的CO,以便循环使用,G装置的作用是 ,
H装置中盛放的试剂是 。
(4)某同学为了证明“E装置中CO与NaOH固体发生了反应”,设计下列实验方案:
取固体产物,配成溶液,常温下测溶液的pH,若pH>7,证明CO与NaOH固体
生了反应。
![]() 经小组讨论,该方案不可行,理由是 。
经小组讨论,该方案不可行,理由是 。
(5)测定产物中甲酸钠(HCOONa)的纯度
准确称取固体产物m g配成100 mL溶液,取20.00 mL溶液,加入指示剂,用
c mol•![]() L-1的盐酸标准溶液平行滴定剩余的NaOH三
L-1的盐酸标准溶液平行滴定剩余的NaOH三![]() 次,平均消耗的体积为νmL。
次,平均消耗的体积为νmL。
已知:三种指示剂的变色范围如下所示。
![]()
甲基橙 酚酞 甲基红
指示剂应选用 ;产物中甲酸钠的纯度为 (用含m、c、v的代数式表示)。
![]() (1)HCOOH CO↑+ H2O (2分)
(1)HCOOH CO↑+ H2O (2分)
(说明:反应条件未写“△”不扣分,“=”写成“→”不扣分)
浓硫酸与甲酸混合时放出大量的热 (2分)
(说明:写“浓硫酸吸水放热”或“浓硫酸脱水放热”等合理答案也得2分)
(2)c b e d f (2分)
(说明:字母顺序完全正确才得分)
(3)PdCl2 + CO + H2O = Pd↓+ CO2 + 2HCl (2分)
除去酸性气体 (1分)
(说明:写“除去CO2、HCl等气体”也得2分)
浓硫酸 (1分)
(4)无论CO与NaOH是否发生反应,溶液的pH均大于7(或其他合理答案) (2分)
(5)酚酞 (2分)
![]() (2分)
(2分)
![]()
![]() (说明:写“ ”“ ”等合理答案也得2分
(说明:写“ ”“ ”等合理答案也得2分![]() )
)
硫酸1.2升和水1.8升混合成稀溶液,硫酸0.9升和水0.3升混合成浓溶液,现在要混合成硫酸和水各 2020-04-12 …
浓度问题(1)硫酸1.2公升和水1.8公升混合成稀溶液,硫酸0.9公升和水0.3公升混合成浓溶液, 2020-04-12 …
硫酸1.2升和水1.8升混合成稀溶液,硫酸0.9升和水0.3升混合成浓溶液,现在要混合成硫酸和水各 2020-06-27 …
用0.1000mol.L-NaOH溶液滴定20.00ml0.1000mol/LHCOOH溶液,计算 2020-07-24 …
甲酸(HCOOH)易挥发,熔点为8.6℃,电离常数K=1.8×10-4。某化学兴趣小组进行以下实验 2020-07-24 …
下列物质(均为0.1mol/L),不能用NaOH标准溶液直接滴定的是A.一氯醋酸(Ka=1.4´1 2020-07-24 …
看下这两个氧化还原反应配平的区别反应物:高锰酸钾,硫酸亚铁,硫酸生成物:硫酸铁,硫酸2价锰,硫酸钾 2020-07-25 …
(8分)已知在25℃时,醋酸、碳酸和亚硫酸的电离平衡常数分别为:醋酸Ka=1.75×10-5碳酸Ka 2020-11-29 …
这是某学校实验室从化学试剂商店买回的硫酸试剂,问题如下:欲配制500克溶质质量分数为百分之19.6的 2020-12-06 …
如表是某硫酸试剂瓶标签上的部分文字说明,苏老师需要将10mL的该硫酸稀释成浓度为9.8%的稀硫酸ag 2021-02-01 …