早教吧作业答案频道 -->化学-->
(1)25℃,吸收液Na2SO3溶液在吸收SO2的过程中,pH随n(SO32-):n(HSO3-)变化关系如下表:n(SO32-):n(HSO3-)91:91:11:91pH8.27.26.2①当吸收液呈中性时,溶液中离
题目详情
(1)25℃,吸收液Na2SO3溶液在吸收SO2的过程中,pH随n(SO32-):n(HSO3-)变化关系如下表:
①当吸收液呈中性时,溶液中离子浓度关系正确的是:___(选填字母)
A.c(Na+)=2c(SO32-)+c(HSO3-)
B.c(Na+)>c(HSO3-)>c(SO32-)>c(H+)=c(OH-)
C.c(Na+)+c(H+)=c(SO32-)+c(HSO3-)+c(OH-)
②当吸收液的pH降至约为6时,需送至电解槽再生.再生示意图如下:
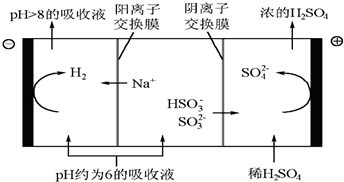
请写出HSO3-在阳极放电的电极反应式是___.
(2)已知:CH4(g)+2O2(g)=CO2 (g)+2H2O (l)△H=-Q1 kJ/mol
2H2(g)+O2(g)=2H2 O (g)△H=-Q2 kJ/mol
2H2(g)+O2(g)=2H2 O (l)△H=-Q3 kJ/mol,
常温下,取体积比4:1的甲烷和氢气的混合气体11.2L(标况),经完全燃烧恢复常温,放出的热为___.
| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 1:91 |
| pH | 8.2 | 7.2 | 6.2 |
A.c(Na+)=2c(SO32-)+c(HSO3-)
B.c(Na+)>c(HSO3-)>c(SO32-)>c(H+)=c(OH-)
C.c(Na+)+c(H+)=c(SO32-)+c(HSO3-)+c(OH-)
②当吸收液的pH降至约为6时,需送至电解槽再生.再生示意图如下:

请写出HSO3-在阳极放电的电极反应式是___.
(2)已知:CH4(g)+2O2(g)=CO2 (g)+2H2O (l)△H=-Q1 kJ/mol
2H2(g)+O2(g)=2H2 O (g)△H=-Q2 kJ/mol
2H2(g)+O2(g)=2H2 O (l)△H=-Q3 kJ/mol,
常温下,取体积比4:1的甲烷和氢气的混合气体11.2L(标况),经完全燃烧恢复常温,放出的热为___.
▼优质解答
答案和解析
(1)①当溶液呈中性时,溶液中氢离子浓度等于氢氧根离子浓度,亚硫酸氢根离子浓度大于亚硫酸根离子浓度.
A、溶液呈电中性,溶液中阴阳离子所带电荷相等,溶液呈中性时,溶液中氢离子浓度等于氢氧根离子浓度,所以c(Na+)=2c(SO32-)+c(HSO3-),故A正确.
B、溶液呈中性时,溶液中氢离子浓度等于氢氧根离子浓度,亚硫酸氢根离子浓度大于亚硫酸根离子浓度,溶液中阴阳离子所带电荷相等,所以得c(Na+)>c(HSO3-)>c(SO32-)>c(H-)=c(OH-),故B正确.
C、溶液呈电中性,溶液中阴阳离子所带电荷相等,得c(Na+)+c(H-)=2c(SO32-)+c(HSO3-)+c(OH-),故C错误.
故答案为:AB;
②当吸收液的pH降至约为6时,吸收液中阴离子主要是亚硫酸氢根离子,亚硫酸氢根离子在阳极上失电子和水反应生成硫酸根离子和氢离子,电极反应式为:HSO3-+H2O-2e-=SO42-+3H+.
故答案为:HSO3-+H2O-2e-=SO42-+3H+;
(2)甲烷和氢气的混合气体11.2L(已折合成标准状况),所以甲烷和氢气的混合气体的总的物质的量为
=0.5mol,
甲烷和氢气的体积比为4:1,所以甲烷的物质的量为0.5mol×
=0.4mol,氢气的物质的量为0.5mol-0.4mol=0.1mol.
由CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-Q1kJ/mol可知,
0.4mol甲烷燃烧放出的热量为0.4mol×Q1kJ/mol=0.4Q1kJ;
由2H2(g)+O2(g)═2H2O(l)△H=-Q3kJ/mol可知,
0.1mol氢气燃烧生成液态水放出的热量为0.1mol×
×Q3kJ/mol=0.05Q3kJ.
所以放出的热量为0.4Q1+0.05Q3,
故答案为:0.4 Q1+0.05Q3.
A、溶液呈电中性,溶液中阴阳离子所带电荷相等,溶液呈中性时,溶液中氢离子浓度等于氢氧根离子浓度,所以c(Na+)=2c(SO32-)+c(HSO3-),故A正确.
B、溶液呈中性时,溶液中氢离子浓度等于氢氧根离子浓度,亚硫酸氢根离子浓度大于亚硫酸根离子浓度,溶液中阴阳离子所带电荷相等,所以得c(Na+)>c(HSO3-)>c(SO32-)>c(H-)=c(OH-),故B正确.
C、溶液呈电中性,溶液中阴阳离子所带电荷相等,得c(Na+)+c(H-)=2c(SO32-)+c(HSO3-)+c(OH-),故C错误.
故答案为:AB;
②当吸收液的pH降至约为6时,吸收液中阴离子主要是亚硫酸氢根离子,亚硫酸氢根离子在阳极上失电子和水反应生成硫酸根离子和氢离子,电极反应式为:HSO3-+H2O-2e-=SO42-+3H+.
故答案为:HSO3-+H2O-2e-=SO42-+3H+;
(2)甲烷和氢气的混合气体11.2L(已折合成标准状况),所以甲烷和氢气的混合气体的总的物质的量为
| 11.2 |
| 22.4 |
甲烷和氢气的体积比为4:1,所以甲烷的物质的量为0.5mol×
| 4 |
| 5 |
由CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-Q1kJ/mol可知,
0.4mol甲烷燃烧放出的热量为0.4mol×Q1kJ/mol=0.4Q1kJ;
由2H2(g)+O2(g)═2H2O(l)△H=-Q3kJ/mol可知,
0.1mol氢气燃烧生成液态水放出的热量为0.1mol×
| 1 |
| 2 |
所以放出的热量为0.4Q1+0.05Q3,
故答案为:0.4 Q1+0.05Q3.
看了 (1)25℃,吸收液Na2S...的网友还看了以下:
图1表示萌发小麦种子中发生的相关生理过程,A~E表示物质,①~④表示过程.图2表示测定消过毒的萌发 2020-05-14 …
图1曲线表示某植物在恒温30℃、CO2浓度一定时光合速率与光照强度的关系,图2表示测定消毒过的萌发 2020-05-15 …
(11分)图1为某植物所在密闭大棚内一昼夜二氧化碳浓度的变化,图2表示该植物在温度为A时光照强度分 2020-05-15 …
假如我们约定正整数a和b中,如果a除以b中,如果a除以b的商的整数部分记作Z(a/b),而它的余数 2020-06-17 …
六年级求下列各式中x的值(1)x:11/5=61/4:2(2)6:x=22/5:1(3)60/x= 2020-07-18 …
(1)25℃,吸收液Na2SO3溶液在吸收SO2的过程中,pH随n(SO32-):n(HSO3-) 2020-07-25 …
c(11,2)表示什么? 2020-11-23 …
(11分,每空1分)图1为某植物所在密闭大棚内一昼夜二氧化碳浓度的变化,图2表示该植物在温度为A时光 2020-11-30 …
高中数学1.一个凸n边形的内角成等差数列,最小角为40°,公差为20°,求n.2.观察下列数表,求第 2020-12-24 …
(1)在钠碱循环法吸收尾气中的SO2时,Na2SO3溶液作为吸收液.写出吸收时发生的有关离子方程式: 2021-01-12 …