早教吧作业答案频道 -->化学-->
已知A、B、C、D四种元素均为短周期元素,原子序数依次递增,E为前30号元素.5种元素的部分特点:元素特点A其气态氢化物呈三角锥形,水溶液显碱性B基态原子核外有
题目详情
已知A、B、C、D四种元素均为短周期元素,原子序数依次递增,E为前30号元素.5种元素的部分特点:
(1)AF3分子中A的杂化类型为___,该分子的空间构型为___.
(2)基态C原子的电子排布式为___.第一电离能:A___B(填“>”或“<”“=”).
(3)A、B、D电负性由大到小的顺序为___(用元素符号表示).
(4)D和A形成的化合物常用作高温耐火材料,化学性质稳定,据此推测它应属于___晶体.
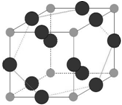
(5)E元素与A元素形成某种化合物的晶胞结构如图所示(黑球代表E原子),若该晶体的密度为ρg•cm-3,则该晶胞的体积是___cm3.
| 元素 | 特 点 |
| A | 其气态氢化物呈三角锥形,水溶液显碱性 |
| B | 基态原子核外有三个能级,其中最外层电子数等于次外层电子数的3倍 |
| C | 基态原子占据两种形状的原子轨道,且最外层电子数等于最内层电子数 |
| D | 元素原子的外围电子层排布式为nsn-1npn-1 |
| E | 原子M能级层为全充满状态且核外的未成对电子只有一个 |
(2)基态C原子的电子排布式为___.第一电离能:A___B(填“>”或“<”“=”).
(3)A、B、D电负性由大到小的顺序为___(用元素符号表示).
(4)D和A形成的化合物常用作高温耐火材料,化学性质稳定,据此推测它应属于___晶体.
(5)E元素与A元素形成某种化合物的晶胞结构如图所示(黑球代表E原子),若该晶体的密度为ρg•cm-3,则该晶胞的体积是___cm3.

▼优质解答
答案和解析
(1)NF3分子中N形成三个σ键,和一对孤对电子对,所以中心原子氮的杂化类型为sp3;该分子的空间构型为三角锥形,故答案为:sp3;三角锥形;
(2)镁的基态原子的电子式为:1s22s22p63s2,氮的价电子排布为:1s22s22p3,而氧元素的价电子排布为:1s22s22p4,氮的价电子排布式2p轨道是半满的稳定状态,所以第一电离能:A>B,故答案为:1s22s22p63s2;>;
(3)非金属性越强电负性越大,非金属性:O>N>Si,所以电负性:O>N>Si,故答案为:O>N>Si;
(4)硅和氮形成的化合物氮化硅,由于熔点高,化学性质稳定,所以氮化硅是原子,故答案为:原子;
(5)A为N元素,E为Cu元素,该晶胞中,Cu原子个数=12×
=3,N原子个数=8×
=1,该晶胞的化学式为Cu3N,该晶胞的体积为:
=
cm=
cm,故答案为:
.
(2)镁的基态原子的电子式为:1s22s22p63s2,氮的价电子排布为:1s22s22p3,而氧元素的价电子排布为:1s22s22p4,氮的价电子排布式2p轨道是半满的稳定状态,所以第一电离能:A>B,故答案为:1s22s22p63s2;>;
(3)非金属性越强电负性越大,非金属性:O>N>Si,所以电负性:O>N>Si,故答案为:O>N>Si;
(4)硅和氮形成的化合物氮化硅,由于熔点高,化学性质稳定,所以氮化硅是原子,故答案为:原子;
(5)A为N元素,E为Cu元素,该晶胞中,Cu原子个数=12×
| 1 |
| 4 |
| 1 |
| 8 |
| m |
| ρ |
| ||
| ρ |
| 206 |
| ρNA |
| 206 |
| ρNA |
看了 已知A、B、C、D四种元素均...的网友还看了以下:
送快递的人可能在早上6:30-7:30之间把快递送到张老师家里,张老师离开家去工作的时间在早上7: 2020-04-08 …
3的m次方=2,则3的m+1次方=?2的a次方=14 2的b次方=7 则2的a-b次方=?已知5的 2020-05-13 …
对有理数a,b定义运算★:a ★b=a的b次方.例如(-5)★3=(-5)的3次方=-125.对有 2020-05-16 …
整式的乘法的比赛题.第一题:已知,2的a次方=5,2的b次方=6,求2的3a+2b次方?第二题:已 2020-05-19 …
一套五卷百科全书按递增顺序摆放在书架上,即从左到右由第1卷依次排到第5卷.现想把它们改换成按递减顺 2020-06-22 …
C语言一些题目问题?1.C语言程序的三种基础结构是()结构、抉择结构跟轮回构造。A.次序B.递归C 2020-06-27 …
已知(a+b)的a次方乘(b+a)的b次方=(a+b)的5次方,且(a-b)的a+5次方乘(a-b 2020-07-21 …
递增公式举例:100为基数,每次递增2.5%到150次第150次得多少-------------- 2020-07-22 …
每隔5年递增一次,递增幅度为5%,30年如何计算. 2020-11-27 …
比重不同的药物制备散剂时,采用()的混合方法最佳A.等量递加法B.多次过筛C.将轻者加在重者比重不同 2020-12-17 …