早教吧作业答案频道 -->化学-->
某化学小组同学用下列装置和试剂进行实验,探究O2与KI溶液发生反应的条件.供选试剂:30%H2O2溶液、0.1mol/LH2SO4溶液、MnO2固体、KMnO4固体(1)小组同学设计甲、乙、丙三组实验,记录如表
题目详情
某化学小组同学用下列装置和试剂进行实验,探究O2与KI溶液发生反应的条件.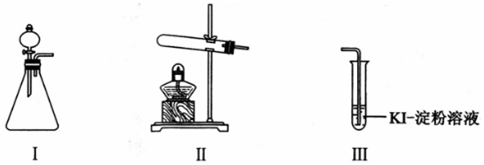
供选试剂:30% H2O2溶液、0.1mol/L H2SO4溶液、MnO2固体、KMnO4固体
(1)小组同学设计甲、乙、丙三组实验,记录如表:
(2)丙实验中O2与KI溶液反应的离子方程式是___.
(3)对比乙、丙实验可知,O2与KI溶液发生反应的适宜条件是___.为进一步探究该条件对反应速率的影响,可采取的实验措施是___.
(4)由甲、乙、丙三实验推测,甲实验可能是I中的白雾使溶液变蓝.学生将I中产生的气体直接通入下列___溶液(填序号),证明了白雾中含有H2O2.
A.酸性 KMnO4 B.FeCl2 C.Na2S D.品红
(5)资料显示:KI溶液在空气中久置过程中会被缓慢氧化:4KI+O2+2H2O=2I2+4KOH.该小组同学取20mL久置的KI溶液,向其中加入几滴淀粉溶液,结果没有观察到溶液颜色变蓝,他们猜想可能是发生了反应(写离子方程式)___造成的,请设计实验证明他们的猜想是否正确___.

供选试剂:30% H2O2溶液、0.1mol/L H2SO4溶液、MnO2固体、KMnO4固体
(1)小组同学设计甲、乙、丙三组实验,记录如表:
| 操作 | 现象 | |
| 甲 | 向I的锥形瓶中加入 ___,.向I的 ___中加入30% H2O2溶液,连接I、Ⅲ,打开活塞 | I中产生无色气体并伴随大量白雾;Ⅲ中有气泡冒出,溶液迅速变蓝 |
| 乙 | 向Ⅱ中加入KMnO4固体,连接Ⅱ、Ⅲ,点燃酒精灯 | Ⅲ中有气泡冒出,溶液不变蓝 |
| 丙 | 向Ⅱ中加入KMnO4固体,Ⅲ中加入适量0.1mol/L H2SO4溶液,连接Ⅱ、Ⅲ,点燃酒精灯 | Ⅲ中有气泡冒出,溶液变蓝 |
(3)对比乙、丙实验可知,O2与KI溶液发生反应的适宜条件是___.为进一步探究该条件对反应速率的影响,可采取的实验措施是___.
(4)由甲、乙、丙三实验推测,甲实验可能是I中的白雾使溶液变蓝.学生将I中产生的气体直接通入下列___溶液(填序号),证明了白雾中含有H2O2.
A.酸性 KMnO4 B.FeCl2 C.Na2S D.品红
(5)资料显示:KI溶液在空气中久置过程中会被缓慢氧化:4KI+O2+2H2O=2I2+4KOH.该小组同学取20mL久置的KI溶液,向其中加入几滴淀粉溶液,结果没有观察到溶液颜色变蓝,他们猜想可能是发生了反应(写离子方程式)___造成的,请设计实验证明他们的猜想是否正确___.
▼优质解答
答案和解析
(1)甲实验:根据装置Ⅰ不需要加热制取氧气可知利用的是双氧水的分解,过氧化氢在二氧化锰催化作用下分解生成氧气,向I的锥形瓶中加入MnO2固体,向I的分液漏斗中加入30% H2O2溶液,连接I、Ⅲ,打开活塞,I中产生无色气体并伴随大量白雾;Ⅲ中有气泡冒出,溶液迅速变蓝说明生成碘单质,
故答案为:MnO2固体;分液漏斗;
(2)碘离子具有还原性,在酸性条件下能够被氧化氧化成碘单质,据此写出反应的离子方程式为:O2+4I-+4H+=2I2+2H2O,
故答案为:O2+4I-+4H+=2I2+2H2O;
(3)向Ⅱ中加入KMnO4固体,连接Ⅱ、Ⅲ,点燃酒精灯,Ⅲ中有气泡冒出,溶液不变蓝,向Ⅱ中加入KMnO4固体,Ⅲ中加入适量0.1mol/L H2SO4溶液,连接Ⅱ、Ⅲ,点燃酒精灯,Ⅲ中有气泡冒出,溶液变蓝对比乙、丙实验可知,O2与KI溶液发生反应的适宜条件是:酸性环境;为进一步探究该条件对反应速率的影响,可采取的实验措施是:使用不同浓度的稀硫酸作对比实验,
故答案为:酸性环境;使用不同浓度的稀硫酸作对比实验;
(4)A.KMnO4,高锰酸钾溶液能够将双氧水氧化,导致高锰酸钾溶液褪色,而氧气不与高锰酸钾溶液反应,如果高锰酸钾溶液褪色可证明混合气体中含有双氧水,故A正确;
B.FeCl2,氧气和高锰酸钾溶液都能够氧化亚铁离子,无法证明混合气体中含有双氧水,故B错误;
C.Na2S,高锰酸钾和氧气都能够氧化硫化钠,无法用硫化钠检验混合气体中是否含有双氧水,故C错误;
D.品红遇到过氧化氢会被氧化红色褪去,证明混合气体中含有双氧水,故D正确;
故答案为:AD;
(5)KI溶液在空气中久置过程中会被缓慢氧化:4KI+O2+2H2O=2I2+4KOH.该小组同学取20mL久置的KI溶液,向其中加入几滴淀粉溶液,结果没有观察到溶液颜色变蓝,他们猜想可能是发生了反应的离子方程式为:3I2+6OH-=5I-+IO3-+3H2O,设计实验证明他们的猜想是否正确升温方案为:在上述未变蓝的溶液中滴入0.1mol/LH2SO4溶液观察现象,若溶液变蓝则猜想正确,否则错误,
故答案为:3I2+6OH-=5I-+IO3-+3H2O;在上述未变蓝的溶液中滴入0.1mol/LH2SO4溶液观察现象,若溶液变蓝则猜想正确,否则错误.
故答案为:MnO2固体;分液漏斗;
(2)碘离子具有还原性,在酸性条件下能够被氧化氧化成碘单质,据此写出反应的离子方程式为:O2+4I-+4H+=2I2+2H2O,
故答案为:O2+4I-+4H+=2I2+2H2O;
(3)向Ⅱ中加入KMnO4固体,连接Ⅱ、Ⅲ,点燃酒精灯,Ⅲ中有气泡冒出,溶液不变蓝,向Ⅱ中加入KMnO4固体,Ⅲ中加入适量0.1mol/L H2SO4溶液,连接Ⅱ、Ⅲ,点燃酒精灯,Ⅲ中有气泡冒出,溶液变蓝对比乙、丙实验可知,O2与KI溶液发生反应的适宜条件是:酸性环境;为进一步探究该条件对反应速率的影响,可采取的实验措施是:使用不同浓度的稀硫酸作对比实验,
故答案为:酸性环境;使用不同浓度的稀硫酸作对比实验;
(4)A.KMnO4,高锰酸钾溶液能够将双氧水氧化,导致高锰酸钾溶液褪色,而氧气不与高锰酸钾溶液反应,如果高锰酸钾溶液褪色可证明混合气体中含有双氧水,故A正确;
B.FeCl2,氧气和高锰酸钾溶液都能够氧化亚铁离子,无法证明混合气体中含有双氧水,故B错误;
C.Na2S,高锰酸钾和氧气都能够氧化硫化钠,无法用硫化钠检验混合气体中是否含有双氧水,故C错误;
D.品红遇到过氧化氢会被氧化红色褪去,证明混合气体中含有双氧水,故D正确;
故答案为:AD;
(5)KI溶液在空气中久置过程中会被缓慢氧化:4KI+O2+2H2O=2I2+4KOH.该小组同学取20mL久置的KI溶液,向其中加入几滴淀粉溶液,结果没有观察到溶液颜色变蓝,他们猜想可能是发生了反应的离子方程式为:3I2+6OH-=5I-+IO3-+3H2O,设计实验证明他们的猜想是否正确升温方案为:在上述未变蓝的溶液中滴入0.1mol/LH2SO4溶液观察现象,若溶液变蓝则猜想正确,否则错误,
故答案为:3I2+6OH-=5I-+IO3-+3H2O;在上述未变蓝的溶液中滴入0.1mol/LH2SO4溶液观察现象,若溶液变蓝则猜想正确,否则错误.
看了 某化学小组同学用下列装置和试...的网友还看了以下:
如图甲、乙两图都是电解水的简易装置.回答下列问题:(1)装置甲比装置乙有一个明显的优点,这个优点是 2020-05-05 …
(1)装置甲与装置乙相比,有一个明显的优点是(2)装置乙与装置甲相比,有一个明显的优点是(3)电解 2020-05-05 …
(1)装置甲与装置乙相比,有一个明显的优点是(2)装置乙与装置甲相比,有一个明显的优点是(3)电解 2020-05-05 …
1:甲有40元,乙比甲的4分之1多2元,乙有几元?2:甲有40元,乙比甲的4分之1少2元,乙有几元 2020-06-15 …
请老师再帮我看看下列说法对不对.1,甲是乙的3倍=甲比乙多2倍=乙比甲少2倍=乙是甲的1/3.2,甲 2020-11-03 …
如图,甲、乙两图都是电解水的简易装置.回答下列问题.(1)装置甲比装置乙有一个明显的优点,这个优点是 2020-11-25 …
六人站成一排,求(1)甲、乙即不再排头也不在排尾数(2)甲不在排头,乙不在排尾且甲乙不相邻(1)4* 2020-11-30 …
图2-4中甲、乙两图都是使用电磁打点计时器测量重力加速度g的装置示意图,已知该打点计时器的打点频率为 2020-12-07 …
为了响应“足球进校园”的号召,某校计划为校足球队购置一批足球.已知购买2个甲型足球和3个乙型足球共需 2021-01-09 …
甲地(位置见图2)气温年较差较小,5~8月降水稀少。据此完成4~5题。4、甲地气温年较差较小的主要原 2021-01-18 …