氢气、一氧化碳、辛烷、甲烷燃烧的热化学方程式分别为:H2(g)+O2(g)=H2O(l)△H=﹣285.8kJ/molCO(g)+O2(g)=CO2(g)△H=﹣282.6kJ/molC8H18(l)
氢气、一氧化碳、辛烷、甲烷燃烧的热化学方程式分别为:
H 2 (g)+ 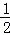 O 2 (g)=H 2 O(l)△H=﹣285.8kJ/mol
O 2 (g)=H 2 O(l)△H=﹣285.8kJ/mol
CO(g)+ 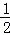 O 2 (g)=CO 2 (g)△H=﹣282.6kJ/mol
O 2 (g)=CO 2 (g)△H=﹣282.6kJ/mol
C 8 H 18 (l)+ 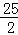 O 2 (g)=8CO 2 (g)+9H 2 O(l)△H=﹣5472kJ/mol
O 2 (g)=8CO 2 (g)+9H 2 O(l)△H=﹣5472kJ/mol
CH 4 (g)+2O 2 (g)=CO 2 (g)+2H 2 O(l);△H=﹣889.6kJ/mol
相同质量的氢气、一氧化碳、辛烷、甲烷完全燃烧时,放出热量最少的是( )
|
| A. | H 2 (g) | B. | CO(g) | C. | C 8 H 18 (l) | D. | CH 4 (g) |
考点:
| 热化学方程式. | |
| | 化学反应中的能量变化. |
| | △H是焓变,其值为负值时,反应放热,负号后面的数字越大,放出的热量就越大;负号后面的数字越小,放出的热量就越小,并利用物质的物质的量与热量成正比来计算. |
| | H 2 、CO、C 8 H 18 、CH 4 的相对分子质量分别为2、28、114、16, 所以相同质量(假设均是1g)四种物质的物质的量之比为57:4.07:1:7.125, 燃烧放出热量之比为(57×285.8):(4.07×282.6):(1×5472):(7.125×889.6)=16256.4:1150.182:5472:6362.4, 所以相同质量的氢气、一氧化碳、辛烷、甲烷完全燃烧时,放出热量最多的是氢气,最少的为CO. 故选B. |
| | 本题考查学生有关热化学方程式的计算,熟悉物质的相对分子质量及物质的量与热量的关系即可解答,难度不大. |
已知:①C(s)+O2(g)=CO2(g);△H=-393.5kJ•mol1②2CO(g)+O2 2020-04-07 …
氢气、一氧化碳、辛烷、甲烷的热化学方程式分别为:H2(g)+O2(g)=H2O(l)△H=-285 2020-05-13 …
氢气、一氧化碳、辛烷、甲烷的热化学方程式分别为:H2(g)+O2(g)=H2O(l)△H=-285 2020-05-13 …
比较下列各组热化学方程式中△H的大小关系.(1)S(s)+O2(g)═SO2(g)△H1S(g)+ 2020-07-12 …
I.已知:反应4HCl(g)+O2(g)CuO/CuCI400℃2Cl2(g)+2H2O(g)△H 2020-07-17 …
已知:反应4HCl(g)+O2(g)⇌2Cl2(g)+2H2O(g)△H=-115.6kJ/mol 2020-07-18 …
根据下列热化学方程式:(1)C(s)+O2(g)=CO2(g)ΔH1=-393.5kJ·mol-1 2020-07-19 …
下列各组热化学方程式中,化学反应的△H前者大于后者的是①C(s)+O2(g)====CO2(g);△ 2020-12-14 …
已知:2SO2(g)+O2(g)2SO3(g)△H=-196.6kJ•mol-12NO(g)+O2( 2021-02-16 …
书写热化学方程式:A.1molN2(g)与适量O2(g)起反应,生成NO2(g),吸收68kJ热量. 2021-02-16 …