早教吧作业答案频道 -->化学-->
甲乙两同学对保存已久的Na2SO3试剂进行试验探究.取适量Na2SO3样品于洁净烧杯中,加入适量蒸馏水,充分搅拌全部溶解.(1)测上述溶液的PH值,其PH值>7,原因是(用离子方程式表示)
题目详情
甲乙两同学对保存已久的Na2SO3试剂进行试验探究.
取适量Na2SO3样品于洁净烧杯中,加入适量蒸馏水,充分搅拌全部溶解.
(1)测上述溶液的PH值,其PH值>7,原因是(用离子方程式表示)___
(2)取少量上述溶液于试管中,加入硝酸钡溶液生成白色沉淀,再加入盐酸,白色沉淀不溶解,甲认为已变质,乙认为他的结论不科学,理由是___
(3)假设试剂由Na2SO3和Na2SO4组成,设计试验方案,进行成分检验,他们决定继续探究,请在答题卡上写出实验步骤、预期现象和结论.
限选试剂及仪器:稀盐酸、稀硝酸、氯化钡溶液,品红溶液,酸性高锰酸溶液,NaOH溶液、澄清石灰水、pH计、烧杯、试管、带塞导气管、滴管
(4)经实验检验后,确实已变质,现准确测定其中Na2SO3的含量.实验如下:
①配制250ml 约0.2mol•L-1 Na2SO3溶液:准确称取w克试样,置于烧杯中,加适量蒸馏水溶解,将溶液转入___,洗涤,定容,摇匀.
②滴定:准确量取25.00ml Na2SO3所配制溶液于锥形瓶中,将 0.05mol•L-1酸性高锰酸钾装入50ml___(填酸式或碱式)滴定管,滴定至终点,记录数据.重复滴定2次.平均消耗KMnO4VmL.
③计算Na2SO3的质量分数=___(只列出计算式,不要求算出结果)
取适量Na2SO3样品于洁净烧杯中,加入适量蒸馏水,充分搅拌全部溶解.
(1)测上述溶液的PH值,其PH值>7,原因是(用离子方程式表示)___
(2)取少量上述溶液于试管中,加入硝酸钡溶液生成白色沉淀,再加入盐酸,白色沉淀不溶解,甲认为已变质,乙认为他的结论不科学,理由是___
(3)假设试剂由Na2SO3和Na2SO4组成,设计试验方案,进行成分检验,他们决定继续探究,请在答题卡上写出实验步骤、预期现象和结论.
限选试剂及仪器:稀盐酸、稀硝酸、氯化钡溶液,品红溶液,酸性高锰酸溶液,NaOH溶液、澄清石灰水、pH计、烧杯、试管、带塞导气管、滴管
| 实验步骤 | 预期现象和结论 |
| 步骤1:取适量试剂于洁净烧杯中,加入足量蒸馏水,充分搅拌,静置. | |
| 步骤2:取适量步骤1所得溶液于试管中,加入少量的 ___溶液. | 若溶液褪色,说明其有 ___ 若溶液不褪色,说明其中没有 ___ |
| 步骤3:再取适量步骤1所得溶液于另一试管中,先加入足量的稀盐酸,再滴加 ___溶液. | 如果有白色沉淀生成,则说明其中有 ___,已经变质. 如果没有白色沉淀生成,则说明其中没有 ___ |
①配制250ml 约0.2mol•L-1 Na2SO3溶液:准确称取w克试样,置于烧杯中,加适量蒸馏水溶解,将溶液转入___,洗涤,定容,摇匀.
②滴定:准确量取25.00ml Na2SO3所配制溶液于锥形瓶中,将 0.05mol•L-1酸性高锰酸钾装入50ml___(填酸式或碱式)滴定管,滴定至终点,记录数据.重复滴定2次.平均消耗KMnO4VmL.
③计算Na2SO3的质量分数=___(只列出计算式,不要求算出结果)
▼优质解答
答案和解析
(1)Na2SO3溶液PH值>7,因为其为强碱弱酸盐,SO32-水解呈碱性,水解的离子方程式为SO32-+H2O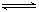 HSO3-+OH-,
HSO3-+OH-,
故答案为:SO32-+H2O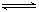 HSO3-+OH-;
HSO3-+OH-;
(2)检验Na2SO3样品是否变质,实质是检验是否生成Na2SO4,即检验样品溶液中是否存在SO42-的,但加入硝酸钡溶液,溶液中的NO3-和H+在一起有强氧化性,会把亚硫酸钡氧化成硫酸钡,无法确定样品是否变质生成Na2SO4,
故答案为:溶液中的NO3-和H+在一起有强氧化性,会把亚硫酸钡氧化成硫酸钡;
(3)假设试剂由Na2SO3和Na2SO4组成,进行成分检验实质是检验SO32-和SO42-,SO32-具有强还原性,根据提供的试剂,可用酸性高锰酸钾溶液检验,若酸性高锰酸溶液褪色,说明中有Na2SO3,若酸性高锰酸溶液不褪色,说明中没有Na2SO3,SO42-检验方法为先加入足量的稀盐酸,再滴加氯化钡溶液看是否有白色沉淀生成,如果有白色沉淀生成,则说明其中有Na2SO4,已经变质,如果没有白色沉淀生成,则说明没有Na2SO4;
故答案为:酸性高锰酸钾;Na2SO3;Na2SO3;氯化钡;Na2SO4;Na2SO4;
(4)①配制250ml 约0.2mol•L-1 Na2SO3溶液,准确称取w克试样,置于烧杯中,加适量蒸馏水溶解,将溶液转入250mL容量瓶洗涤,定容,摇匀;
故答案为:250mL容量瓶;
②酸性高锰酸钾溶液具有强氧化性会腐蚀橡胶,应装入酸式滴定管,
故答案为:酸式;
③根据氧化还原反应得失电子守恒,设25.00ml Na2SO3溶液中Na2SO3物质的量为n,则有
5Na2SO3~2KMnO4
5 2
n 0.05V×10-3
则n=
mol,则w克试样中m(Na2SO3)=n×
×126=
g,
则Na2SO3的质量分数=
×100%,
故答案为:
×100%.
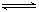 HSO3-+OH-,
HSO3-+OH-,故答案为:SO32-+H2O
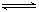 HSO3-+OH-;
HSO3-+OH-;(2)检验Na2SO3样品是否变质,实质是检验是否生成Na2SO4,即检验样品溶液中是否存在SO42-的,但加入硝酸钡溶液,溶液中的NO3-和H+在一起有强氧化性,会把亚硫酸钡氧化成硫酸钡,无法确定样品是否变质生成Na2SO4,
故答案为:溶液中的NO3-和H+在一起有强氧化性,会把亚硫酸钡氧化成硫酸钡;
(3)假设试剂由Na2SO3和Na2SO4组成,进行成分检验实质是检验SO32-和SO42-,SO32-具有强还原性,根据提供的试剂,可用酸性高锰酸钾溶液检验,若酸性高锰酸溶液褪色,说明中有Na2SO3,若酸性高锰酸溶液不褪色,说明中没有Na2SO3,SO42-检验方法为先加入足量的稀盐酸,再滴加氯化钡溶液看是否有白色沉淀生成,如果有白色沉淀生成,则说明其中有Na2SO4,已经变质,如果没有白色沉淀生成,则说明没有Na2SO4;
故答案为:酸性高锰酸钾;Na2SO3;Na2SO3;氯化钡;Na2SO4;Na2SO4;
(4)①配制250ml 约0.2mol•L-1 Na2SO3溶液,准确称取w克试样,置于烧杯中,加适量蒸馏水溶解,将溶液转入250mL容量瓶洗涤,定容,摇匀;
故答案为:250mL容量瓶;
②酸性高锰酸钾溶液具有强氧化性会腐蚀橡胶,应装入酸式滴定管,
故答案为:酸式;
③根据氧化还原反应得失电子守恒,设25.00ml Na2SO3溶液中Na2SO3物质的量为n,则有
5Na2SO3~2KMnO4
5 2
n 0.05V×10-3
则n=
| 5×0.05V |
| 2000 |
| 250 |
| 25 |
| 2.5V×126 |
| 2000 |
则Na2SO3的质量分数=
| 2.5V×126 |
| 2000w |
故答案为:
| 2.5V×126 |
| 2000w |
看了 甲乙两同学对保存已久的Na2...的网友还看了以下:
真正挑战高智商 因事分解设常系数多项式p(x)=x^4+ax^3+bx^2+cx+d满足:p(1) 2020-05-13 …
若有以下定义,则值为4的表达式是 A)p+=3,*(p++) B)p+=3,*++p C)p+=4 2020-05-13 …
如图,抛物线y=ax2+bx+c(a≠0)过点(-1,0)和点(0,-3),且顶点在第四象限,设P 2020-05-17 …
小明在探究“馒头在口腔中的变化”时,进行了三种处理:1.将馒头碎屑与唾液放入1号试管中充分搅拌;2 2020-06-03 …
为什么我做的鲜奶炖蛋,表面光滑,中间却有气泡?我做的步骤是这样的:1、把小半碗牛奶隔水加热,加冰糖 2020-06-17 …
三相功率P=根号3*U*I*COSφ=660*U*I*COSφ,单相p=U*I*COSφ=220* 2020-07-19 …
指针问题设intx[]={1,2,3,4,5,6},*p=x;则数值为3的表达式是(B)。(A)p 2020-07-30 …
A(1,3).B(-3,1).C(-1,-4).D(5,-2).P(3,4)为平面直角坐标系内五个 2020-07-31 …
英语翻译牛奶味果冻:1.将鱼胶粉撒在热水(约80℃)里,搅拌至全部溶化后,倒入温牛奶(约50℃)和砂 2020-11-01 …
用逻辑联结词“且”、“或”联结命题p,q,并判断复合命题“p且q”、“p或q”的真假:1、p:6是3 2020-12-07 …