早教吧作业答案频道 -->化学-->
锂元素被誉为“能源元素”.锂及锂盐具有的优异性能和特殊功能,在化工、电子、宇航、核能、能源等领域都得到广泛应用.Ⅰ锂的原子结构示意图为;锂暴露在湿空气中时,会迅速地
题目详情
锂元素被誉为“能源元素”.锂及锂盐具有的优异性能和特殊功能,在化工、电子、宇航、核能、能源等领域都得到广泛应用.
Ⅰ锂的原子结构示意图为___;锂暴露在湿空气中时,会迅速地失去金属光泽、表面开始变黑,更长时间则变成白色.生成的化合物是氮化锂、氢氧化锂,最终生成碳酸锂.写出生成氮化锂的化学方程式___.
Ⅱ下面是从锂辉石(Li2O•Al2O3•SiO2)中提出锂的工业流程示意图.
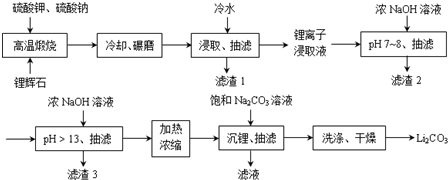
①高温煅烧时的反应原理为:
Li2O•Al2O3•SiO2+K2SO4=K2O•Al2O3•SiO2+Li2SO4
Li2O•Al2O3•SiO2+Na2SO4=Na2O•Al2O3•SiO2+Li2SO4
②锂离子浸取液中含有的金属离子为:K+、Na+、Li+、Fe3+、Fe2+、Al3+、Mn2+.
③几种金属离子沉淀完全的pH
④Li2SO4、Li2CO3在不同温度下的溶解度(g/100g水)
(1)浸取时使用冷水的原因是___.
(2)滤渣2的主要成分为___.
(3)流程中分2次调节pH(pH7~8和pH>13),有研究者尝试只加一次浓NaOH溶液使pH>13,结果发现在加饱和碳酸钠溶液沉锂后,随着放置时间延长,白色沉淀增加,最后得到的Li2CO3产品中杂质增多.Li2CO3产品中的杂质可能是___,用离子方程式表示其产生的原因___.
(4)加热浓缩的作用是___.
(5)洗涤Li2CO3晶体使用___.
Ⅰ锂的原子结构示意图为___;锂暴露在湿空气中时,会迅速地失去金属光泽、表面开始变黑,更长时间则变成白色.生成的化合物是氮化锂、氢氧化锂,最终生成碳酸锂.写出生成氮化锂的化学方程式___.
Ⅱ下面是从锂辉石(Li2O•Al2O3•SiO2)中提出锂的工业流程示意图.

①高温煅烧时的反应原理为:
Li2O•Al2O3•SiO2+K2SO4=K2O•Al2O3•SiO2+Li2SO4
Li2O•Al2O3•SiO2+Na2SO4=Na2O•Al2O3•SiO2+Li2SO4
②锂离子浸取液中含有的金属离子为:K+、Na+、Li+、Fe3+、Fe2+、Al3+、Mn2+.
③几种金属离子沉淀完全的pH
| 金属离子 | Al(OH)3 | Fe(OH)2 | Fe(OH)3 | Mn(OH)2 |
| 沉淀完全的pH | 4.7 | 9.0 | 3.2 | 10.1 |
| 温度 溶解度 | 10℃ | 20℃ | 50℃ | 80℃ |
| Li2SO4 | 35.4 | 34.7 | 33.1 | 31.7 |
| Li2CO3 | 1.43 | 1.33 | 1.08 | 0.85 |
(2)滤渣2的主要成分为___.
(3)流程中分2次调节pH(pH7~8和pH>13),有研究者尝试只加一次浓NaOH溶液使pH>13,结果发现在加饱和碳酸钠溶液沉锂后,随着放置时间延长,白色沉淀增加,最后得到的Li2CO3产品中杂质增多.Li2CO3产品中的杂质可能是___,用离子方程式表示其产生的原因___.
(4)加热浓缩的作用是___.
(5)洗涤Li2CO3晶体使用___.
▼优质解答
答案和解析
I.锂的原子核外有2个电子层,各层电子数为2、1,原子结构示意图为:,Li与氮气反应生成Li3N,反应方程式为:6Li+N2=2Li3N,故答案为:;6Li+N2=2Li3N;Ⅱ.锂辉石(Li2O•Al2O3•4SiO2)煅烧后,冷却、研磨,有利于...
看了 锂元素被誉为“能源元素”.锂...的网友还看了以下:
对于物体的惯性,下列正确说法是()A.物体在静止时难于推动,说明静止物体的惯性大B.运动速度大的物体 2020-11-02 …
材料一土地退化是指土地受到人为因素或自然因素或人为、自然综合因素的干扰、破坏而改变土地原有的内部结构 2020-11-04 …
地方性法规、规章不一致的问题法律规定有这样一句话“部门规章之间、部门规章与地方政府规章之间具有同等效 2020-11-07 …
某农场有60公顷土地临近麦收,计划等小麦收获后,种植25公顷玉米和35公顷大豆.这些土地中,20公顷 2020-11-23 …
如图所示,从地面上A点发射一枚远程弹道导弹,在引力作用下沿ACB椭圆轨道飞行击中地面目标B,C为轨道 2020-12-05 …
如图所示,从地面上A点发射一枚远程弹道导弹,在引力作用下沿ACB椭圆轨道飞行击中地面目标B,C为轨道 2021-01-12 …
如图所示,从地面上A点发射一枚中远程导弹,只在引力作用下沿ACB椭圆轨道飞行击中地面目标B,C为轨道 2021-01-12 …
表面活性剂是指分子由亲油基和亲水基构成的一类物质。由于其分子结构的特殊性,致使表面活性剂具有一些独特 2021-01-13 …
读“沿北纬32°线我国地形剖面图”,完成下列要求:(1)图中字母表示的范围,分别代表我国地势的阶梯等 2021-01-14 …
读如图“沿北纬32°线我国地形剖面图,完成下列要求:(1)图中字母表示的范围,分别代表我国地势的阶梯 2021-01-14 …