以硼镁矿(2Mg·B2O3·H2O·SiO2)及少量Fe3O4、CaCO3、Al2O3)为原料生产硼酸的工艺流程如下:(1)由于矿粉中含CaCO3,“浸取”时容易产生大量泡沫使物
以硼镁矿(2Mg·B 2 O 3 ·H 2 O·SiO 2 )及少量Fe 3 O 4 、CaCO 3 、Al 2 O 3 )为原料生产硼酸的工艺流程如下:
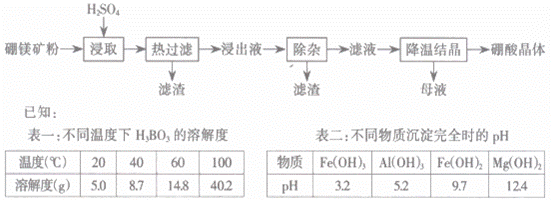
(1)由于矿粉中含CaCO 3 ,“浸取”时容易产生大量泡沫使物料从反应器中溢出,应采取的措施为_____。
(2) “浸出液”显酸性,含有H 3 BO 3 、Mg 2 + 和 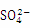 ,还含有Fe 2 + 、Fe 3 + 、Ca 2 + 、Al 3 + 等杂质。“除杂”时,向浸出液中依次加入适量目H 2 O 2 和MgO,可以除去的杂质离子为_________,H 2 O 2 的作用为_________(用离子方程式表示)。
,还含有Fe 2 + 、Fe 3 + 、Ca 2 + 、Al 3 + 等杂质。“除杂”时,向浸出液中依次加入适量目H 2 O 2 和MgO,可以除去的杂质离子为_________,H 2 O 2 的作用为_________(用离子方程式表示)。
(3) “浸取”后,采用“热过滤”的目的为_______。
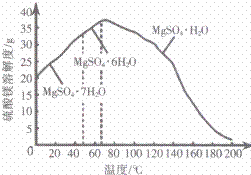
(4) “母液”可用于回收硫酸镁,已知硫酸镁的溶解度随温度变化的曲线如图所示,且溶液的沸点随压强增大而升高。为了从“母液”中充分回收 MgSO 4 ·H 2 O,应采取的措施是将“母液”蒸发浓缩,____。
(5)已知25 ℃时,硼酸( H 3 BO 3 )溶液中存在如下平衡:
H 3 BO 3 (aq)+H 2 O(l)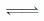 [B(OH) 4 ] - (aq)+H + (aq) K =5.7×10 -10 ;
[B(OH) 4 ] - (aq)+H + (aq) K =5.7×10 -10 ;
25℃时,0.7 mol·L -1 硼酸溶液中 c (H + )≈mol·L -1 。
(6)已知25 ℃时:
| 化学式 | H 2 CO 3 | CH 3 COOH |
| 电离常数 | K 1 =4.4×10 -7 K 2 =4.7×10 -11 | K =1.75×10 -5 |
下列说法正确的是_____________(填选项字母)。
A.碳酸钠溶液滴入硼酸溶液中能观察到有气泡产生
B.碳酸钠溶液滴入醋酸溶液中能观察到有气泡产生
C.等浓度碳酸溶液和硼酸溶液的pH:前者>后者
D.等浓度碳酸钠溶液和醋酸钠溶液的pH:前者>后者
本题考查了工业生产硼酸的工艺流程分析及有关问题。(1)浸取矿粉时,矿粉中含有石灰石,如果一次加入硫酸,会导致碳酸钙分解产生大量气泡,为防止大量气泡产生,可以控制加入硫酸的量来控制反应,故可以分批慢慢加入硫酸。(2)由于铁离子和铝离子能够水解,即Fe3++3H2OFe(OH)3+3H+、Al3++3H2OAl(OH)3+3H+,用稀硫酸浸取及浸出液呈酸性时,能抑制铁离子和铝离子的水解,加入过氧化氢和氧化镁时,能消耗氢离子、生成水且不引入新的杂质阳离子,即MgO+2H+Mg2++H2O,减小氢离子浓度,增大溶液pH至3.2时,促进铁离子水解彻底,即亚铁离子转化为铁离子,铁离子完全沉淀为氢氧化铁,增大溶液pH至5.2时,促进铝离子水解彻底,即铝离子完全沉淀为氢氧化铝沉淀,因此加入适量过氧化氢和氧化镁除去的杂质离子是Fe3+、Fe2+、Al3+。双氧水是常用的绿色氧化剂,所含氧元素由-1价降低为-2价,杂质阳离子中只有亚铁离子能被其氧化为铁离子,根据化合价升降,电荷守恒、质量守恒可得离子方程式为H2O2+2H++2Fe2+2Fe3++2H2O。 (3)浸取时二氧化硅不溶于稀硫酸,浸取反应生成硫酸钙微溶于水,其余物质溶解后变为硼酸、硫酸亚铁、硫酸铁、硫酸镁,根据已知信息,H3BO3在20℃、40℃、60℃、100℃时的溶解度依次为5.0g、8.7g、14.8g、40.2g,为了除去固液混合物中的二氧化硅和硫酸钙,且不能损失硼酸,因此应选择硼酸溶解度最大时的温度,进行趁热过滤,防止温度下降时H3BO3从溶液中析出。(4)除杂时,所得滤渣的主要成分是氢氧化铁、氢氧化铝,而母液的主要成分是硼酸、硫酸镁;为了从“母液”中充分回收MgSO4•H2O,根据硫酸镁的溶解度随温度变化的曲线的已知信息推断,若蒸发浓缩、冷却结晶得到的是MgSO4•7H2O晶体,因此应该蒸发浓缩,升温结晶;根据溶液的沸点随压强增大而升高的已知条件,为了防止蒸发时液体沸腾,影响结晶,还要加压结晶,防止蒸发浓缩时溶液沸腾,从而得到MgSO4•H2O晶体。(5)25℃时,0.7 mol·L-1硼酸溶液中c(H+)===2×10-5mol/L。(6)根据平衡常数可知,酸性为H2CO3H3BO3,所以碳酸钠溶液滴入硼酸溶液中不能观察到有气泡产生,故A错。根据平衡常数可知,酸性CH3COOHH3CO3,则碳酸钠溶液滴入醋酸溶液可生成二氧化碳气体,所以能观察到有气泡产生,故B正确。根据平衡常数可知,酸性H2CO3H3BO3,所以碳酸的电离常数大于硼酸,等浓度碳酸溶液和硼酸溶液比较,酸性碳酸大于硼酸, pH:前者小于后者,故C错。根据平衡常数可知,酸性CH3COOHH3CO3,所以碳酸根离子的水解程度大于醋酸根离子的水解程度,则等浓度碳酸钠溶液和醋酸钠溶液的pH:前者>后者,故D正确。
我国将于2012年10月逐步使用高效照明产品(如:LED节能型灯)替代白炽灯.灯泡中充入氮气是利用 2020-05-13 …
英语翻译摘要:随着电子商务的日益成熟,使对外贸易出现网络化趋势.与传统贸易方式相比,电子商务具有无 2020-05-13 …
台灯灯泡我家用的25W白炽灯泡.调灯泡亮度和灯泡的使用寿命有没有关系?什么关系?也就是说,25W的 2020-05-16 …
下列对网络层次化设计理解,不正确的是()。A.层次化设计易于扩展B.可以使故障排除更容易C.使网络容 2020-05-26 …
二手车交易后,原为运营车辆,交易后改为私家车,其规定使用年限按( )执行。A.私家车规定的使用年限B 2020-05-31 …
一宿舍楼的走廊有10盏“220V40W”的电灯,所有灯每天要开10小时,很容易损坏,于是小明同学给 2020-06-04 …
小杨家里走廊的路灯使用200V5W灯泡,厨房使用220V40W灯泡,试问:两灯泡正常工作的电阻各是 2020-06-06 …
写出下列化学方程式1、为延长白炽灯泡的使用时间,灯泡内放有极少量红磷,以减少灯丝写出下列化学方程式 2020-06-07 …
设有两种型号的灯泡(A和B),A的使用寿命从均值为100小时,方差为16的正态分布.B的使用寿命服 2020-06-10 …
求救啊一到简单数学题啊!灯泡的使用寿命时间服从正态分布,现测10个灯泡得平均寿命为1500小时,s 2020-06-10 …