早教吧作业答案频道 -->化学-->
高碘酸钾(KIO4)为无色晶体,在分析化学中常用作氧化剂.Ⅰ.高碘酸钾的制备步骤①称取1.270g碘溶于适量的水中,通入足量氯气将I2氧化为高碘酸(HIO4).步骤②向步骤①所得溶液中加入
题目详情
高碘酸钾(KIO4)为无色晶体,在分析化学中常用作氧化剂.
Ⅰ.高碘酸钾的制备
步骤①称取1.270g碘溶于适量的水中,通入足量氯气将I2氧化为高碘酸(HIO4).
步骤②向步骤①所得溶液中加入适量氢氧化钾溶液中和.
步骤③将步骤②所得溶液进行蒸发浓缩、冷却结晶等操作得KIO4晶体.
(1)步骤①将I2氧化为HIO4,至少需要消耗___L(标准状况)Cl2.
(2)步骤①所得溶液用0.200mol•L-1KOH溶液中和至中性时(HIO4为强酸,假定溶液中不含Cl2和HClO),则消耗0.200mol•L-1KOH溶液的体积为___mL.
Ⅱ.用高碘酸钾测定甘油的含量
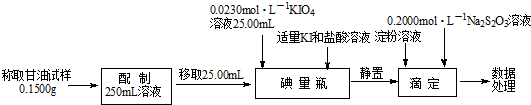
相关反应:C3H8O3(甘油)+2HIO4=2HCHO+HCOOH+2HIO3+H2O
HIO3+5KI+5HCl=3I2+5KCl+3H2O
HIO4+7KI+7HCl=4I2+7KCl+4H2O
I2+2Na2S2O3=2NaI+Na2S4O6
(3)用0.2000mol•L-1Na2S2O3标准溶液滴定时,判断达到滴定终点的现象是___.
(4)已知滴定至终点时消耗Na2S2O3溶液20.00mL,计算甘油样品的纯度(请给出计算过程).
Ⅰ.高碘酸钾的制备
步骤①称取1.270g碘溶于适量的水中,通入足量氯气将I2氧化为高碘酸(HIO4).
步骤②向步骤①所得溶液中加入适量氢氧化钾溶液中和.
步骤③将步骤②所得溶液进行蒸发浓缩、冷却结晶等操作得KIO4晶体.
(1)步骤①将I2氧化为HIO4,至少需要消耗___L(标准状况)Cl2.
(2)步骤①所得溶液用0.200mol•L-1KOH溶液中和至中性时(HIO4为强酸,假定溶液中不含Cl2和HClO),则消耗0.200mol•L-1KOH溶液的体积为___mL.
Ⅱ.用高碘酸钾测定甘油的含量

相关反应:C3H8O3(甘油)+2HIO4=2HCHO+HCOOH+2HIO3+H2O
HIO3+5KI+5HCl=3I2+5KCl+3H2O
HIO4+7KI+7HCl=4I2+7KCl+4H2O
I2+2Na2S2O3=2NaI+Na2S4O6
(3)用0.2000mol•L-1Na2S2O3标准溶液滴定时,判断达到滴定终点的现象是___.
(4)已知滴定至终点时消耗Na2S2O3溶液20.00mL,计算甘油样品的纯度(请给出计算过程).
▼优质解答
答案和解析
Ⅰ.(1)根据电子得失守恒可知,将I2氧化为HIO4时,有关系式I2~7Cl2,1.270g 碘的质量为
=0.005mol,所以消耗的氯气的物质的量为0.035mol,其体积为0.035mol×22.4L/mol=0.784L,
故答案为:0.784;
(2)根据碘元素守恒可知,1.270g I2氧化为高碘酸时,HIO4的物质的量为
×2=0.01mol,同时生成氯化氢的物质的量为0.07mol,与氢氧化钾反应的关系式为7HCl~HIO4~KOH,所以氢氧化钾溶液的体积为
×8=0.05L×8=400mL,
故答案为:400;
Ⅱ.(3)碘溶液中有淀粉,所以溶液呈蓝色,所以用Na2S2O3标准溶液滴定,判断达到滴定终点的现象是滴入最后一滴标准液时,溶液蓝色刚好褪去,且保持30秒不恢复原来的颜色,
故答案为:滴入最后一滴标准液时,溶液蓝色刚好褪去,且保持30秒不恢复原来的颜色;
(4)根据题中的反应方程式可得关系式C3H8O3~
HIO3,I2~2Na2S2O3,3n(HIO3)+4n(HIO4)=n(I2),
碘量瓶中n(HIO3)+n(HIO4)=n(KIO4)=0.0230 mol•L×25.00mL×10-3 L•mL=5.750×10-4 mol…①
滴定时:3n(HIO3)+4n(HIO4)=n(I2)=
n(Na2S2O3)=
×0.2000 mol•L×20.00mL×10-3 L•mL-1=2.000×10-3 mol…②
①×4-②得 n(HIO3)=3.000×10-4 mol
n(C3H8O3)=
n(HIO3)=1.500×10-4 mol
w(C3H8O3)=
×100%=92.00%,
答:甘油样品的纯度为92.00%.
| 1.270g |
| 254g/mol |
故答案为:0.784;
(2)根据碘元素守恒可知,1.270g I2氧化为高碘酸时,HIO4的物质的量为
| 1.270g |
| 254g/mol |
| 0.01mol |
| 0.200mol•L-1 |
故答案为:400;
Ⅱ.(3)碘溶液中有淀粉,所以溶液呈蓝色,所以用Na2S2O3标准溶液滴定,判断达到滴定终点的现象是滴入最后一滴标准液时,溶液蓝色刚好褪去,且保持30秒不恢复原来的颜色,
故答案为:滴入最后一滴标准液时,溶液蓝色刚好褪去,且保持30秒不恢复原来的颜色;
(4)根据题中的反应方程式可得关系式C3H8O3~
| 1 |
| 2 |
碘量瓶中n(HIO3)+n(HIO4)=n(KIO4)=0.0230 mol•L×25.00mL×10-3 L•mL=5.750×10-4 mol…①
滴定时:3n(HIO3)+4n(HIO4)=n(I2)=
| 1 |
| 2 |
| 1 |
| 2 |
①×4-②得 n(HIO3)=3.000×10-4 mol
n(C3H8O3)=
| 1 |
| 2 |
w(C3H8O3)=
| 1.5×10-4×92×10 |
| 0.150 |
答:甘油样品的纯度为92.00%.
看了 高碘酸钾(KIO4)为无色晶...的网友还看了以下:
测定废干电池酸浸液中Mn2+浓度的主要步骤如下:(1)配制硫酸亚铁铵[(NH4)2Fe(SO4)2 2020-04-12 …
要除去锰酸钾中混有的少量高锰酸钾.有如下几步操作(填化学式):第一步:加热,目的是使分解而除去;第 2020-05-14 …
要除去锰酸钾中混有的少量高锰酸钾.有如下几步操作(填化学式):第一步:加热,目的是使分解而除去;第 2020-05-14 …
有关化学离子反应的一些题目1、(1)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性,请写出发 2020-05-16 …
⑴向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性,请写出发生反应的离子方程式:,在以上中性溶 2020-07-20 …
(1)向硫酸氢钠溶液中,逐滴加入Ba(OH)2溶液至中性.请写出发生反应的化学方程式:;(2)在以上 2020-11-02 …
(1)写出NaHSO4在熔融状态的电离方程式(2)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中 2020-11-11 …
有一杯主要含有MgCl2和CaCl2的硬水某兴趣小组设计出软化水的部分实验方案.可供选用的物质有:C 2020-12-03 …
高氯酸是很强的酸,沸点是130℃.质量分数为60%的溶液加热不分解,浓度增高就不稳定,受热易分解,热 2020-12-20 …
SO2是硫酸工业尾气的主要成分。实验室中,拟用如图所示流程,测定标准状况下体积为VL的硫酸工业尾气中 2021-02-01 …