将煤转化为水煤气是通过化学方法将煤转化为洁净燃料的方法之一。煤转化为水煤气的主要化学反应为C(s)H2O(g)CO(g)+H2(g)。C(s)、CO(g)和H2(g)完全燃烧的热化学方程
将煤转化为水煤气是通过化学方法将煤转化为洁净燃料的方法之一。煤转化为水煤气的主要化学反应为 C(s)H 2 O(g) ![]() CO(g) + H 2 (g) 。
CO(g) + H 2 (g) 。
C(s) 、 CO(g) 和 H 2 (g) 完全燃烧的热化学方程式分别为
C(s) + O 2 (g) == =CO 2 (g) Δ H =- 393.5 kJ·mol - 1
H 2 (g) + 1/2O 2 (g) == =H 2 O(g) Δ H 2 =- 242.0 kJ·mol - 1
CO(g) + 1/2O 2 (g) == =CO 2 (g) Δ H 3 =- 283.0 kJ·mol - 1
请回答:
(1) 请你根据以上数据,写出 C(s) 与水蒸气反应生成 CO 和 H 2 的热化学方程式: ________________________________________________________________________ 。
(2) 比较反应热数据可知, 1 mol CO(g) 和 1 mol H 2 (g) 完全燃烧放出的热量之和,比 1 mol C(s) 完全燃烧放出的热量 ________( 填 “ 多 ” 或 “ 少 ”) 。
甲同学据此认为: “ 煤炭燃烧时加少量水,可以使煤炭燃烧放出更多的热量。 ”
乙同学根据盖斯定律作出了下列循环图:
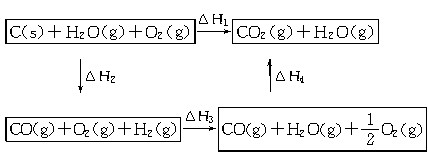
请你写出 Δ H 1 、 Δ H 2 、 Δ H 3 、 Δ H 4 之间存在的关系式 __________________________ 。
乙同学据此认为: “ 将煤转化为水煤气再燃烧放出的热量,最多与直接燃烧煤放出的热量相同。 ” 请分析:甲、乙两同学观点正确的是 ________( 填 “ 甲 ” 或 “ 乙 ”) 同学,另一同学出现错误观点的原因是 ________________________________________ 。
答案 (1)C(s) + H 2 O(g) == =CO(g) + H 2 (g)
Δ H =+ 131.5 kJ·mol - 1
(2) 多 Δ H 1 = Δ H 2 + Δ H 3 + Δ H 4 乙 甲同学忽视了生成水煤气的反应为吸热反应
解析 (2) 由于 C(s) 与水蒸气反应要吸热,所以 1 mol CO 和 1 mol H 2 的能量比 1 mol C(s) 和 1 mol H 2 O(g) 的能量多,燃烧后放出的能量同样也多;反应的总能量是守恒的,所以甲同学的说法不正确的,原因是他忽视了反应 C(s) + H 2 O(g) ![]() CO(g) + H 2 (g) 为吸热反应,已经从环境中吸收了能量,而能量在转化过程中往往会有损失,所以乙同学说得对,即使没有损失也只能与直接燃烧煤放出的热量相同。
CO(g) + H 2 (g) 为吸热反应,已经从环境中吸收了能量,而能量在转化过程中往往会有损失,所以乙同学说得对,即使没有损失也只能与直接燃烧煤放出的热量相同。
冶炼金属一般有下列四种方法:①焦炭法②水煤气(或H2或CO)法③活泼金属置换法④电解法以上四种方法 2020-05-13 …
羰基硫(OCS)是一种有臭鸡蛋气味的无色气体,分子结构与CO2相似,高温下分解为CO和S.下列有关 2020-05-13 …
羰基硫(OCS)是一种有臭鸡蛋气味的无色气体,分子结构与CO2相似,高温下分解为CO和S.下列有关 2020-05-14 …
根据右图,可判断出下列离子方程式中错误的是()A.2Ag(s)+Cd2+(aq)=2Ag+(aq) 2020-06-15 …
(2011•惠州模拟)(1)纳米级Cu2O具有优良的催化性能,下列为制取Cu2O的三种方法;方法1 2020-07-18 …
如图,在长方形ACDF中,AC=DF,点B在CD上,点E在DF上,BC=DE=a,AC=BD=b, 2020-07-21 …
新型锂离子电池材料Li2MSiO4(M为Fe,Co,Mn,Cu等)是一种发展潜力很大的电池电极材料。 2020-12-01 …
新型锂离子电池材料Li2MSiO4(M为Fe,Co,Mn,Cu等)是一种发展潜力很大的电池电极材料。 2020-12-01 …
区分下列各组物质的两种方法都合理的是()选项需区分的物质方法一方法二A硬水和软水取样,蒸干加肥皂水搅 2020-12-03 …
下列有关说法或方程式正确的是()A.用催化法处理汽车尾气中的CO和NO:CO+NOC+NO2B.NO 2021-01-12 …