早教吧作业答案频道 -->化学-->
氨是合成硝酸、铵盐和氮肥的基本原料,回答下列问题:(1)请写出氨气的电子式;(2)0.1mol•L-1的氨水中加入少量NH4Cl固体,溶液的pH(填“升高”或“降低”);若升温,溶液中NH4+
题目详情
氨是合成硝酸、铵盐和氮肥的基本原料,回答下列问题:
(1)请写出氨气的电子式___;
(2)0.1mol•L-1的氨水中加入少量NH4Cl固体,溶液的pH___(填“升高”或“降低”);若升温,溶液中NH4+的浓度___(填“增大”或“减小”);(不考虑氨气受热挥发)
(3)硝酸铵加热分解可得到N2O和H2O,250℃时,硝酸铵在密闭容器中分解达到平衡,该分解反应的化学方程式为___平衡常数表达式为___.
(1)请写出氨气的电子式___;
(2)0.1mol•L-1的氨水中加入少量NH4Cl固体,溶液的pH___(填“升高”或“降低”);若升温,溶液中NH4+的浓度___(填“增大”或“减小”);(不考虑氨气受热挥发)
(3)硝酸铵加热分解可得到N2O和H2O,250℃时,硝酸铵在密闭容器中分解达到平衡,该分解反应的化学方程式为___平衡常数表达式为___.
▼优质解答
答案和解析
(1)N原子的最外层有5个电子,其中3个未成对电子和1对成对电子,3个未成对电子分别和3个H原子形成3对共用电子对,故氨气的电子式为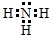 ,
,
故答案为: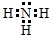 ;
;
(2)一水合氨为弱碱,在水溶液中存在部分电离,电离出氢氧根离子使溶液显碱性,方程式为:NH3•H2O⇌NH4++OH-,向氨水中加入少量NH4Cl固体,铵根浓度增大,平衡左移,即氢氧根浓度减小,pH值降低,升高温度,促进电离,NH4+浓度增大,
故答案为:降低;增大;
(3)硝酸铵分解生成N2O和H2O,达到平衡,说明为可逆反应,化学反应方程式为:NH4NO3
N2O+2H2O,250℃时,水为气体状态,NH4NO3为固态,
则平衡常数K=c(N2O)×c2(H2O),
故答案为:NH4NO3
N2O+2H2O;K=c(N2O)×c2(H2O).
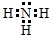 ,
,故答案为:
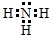 ;
;(2)一水合氨为弱碱,在水溶液中存在部分电离,电离出氢氧根离子使溶液显碱性,方程式为:NH3•H2O⇌NH4++OH-,向氨水中加入少量NH4Cl固体,铵根浓度增大,平衡左移,即氢氧根浓度减小,pH值降低,升高温度,促进电离,NH4+浓度增大,
故答案为:降低;增大;
(3)硝酸铵分解生成N2O和H2O,达到平衡,说明为可逆反应,化学反应方程式为:NH4NO3
| △ |
则平衡常数K=c(N2O)×c2(H2O),
故答案为:NH4NO3
| △ |
看了 氨是合成硝酸、铵盐和氮肥的基...的网友还看了以下:
原电池的问题(高一),析氢吸氧,困惑ing一般的盐溶液里面有H+吧,水应该电离了一些.那么在一个原 2020-04-25 …
氨是合成硝酸、铵盐和氮肥的基本原料,回答下列问题:(1)请写出氨气的电子式;(2)0.1mol•L 2020-05-13 …
在0.1摩尔每升的氯化铵溶液中,怎样使其电离(注意只是氯化铵电离的)的氯离子和铵根离子浓度相等.答 2020-05-13 …
但是题目要求就是使氯化铵电离出的氯离子和铵根离子相等啊,答案的意...但是题目要求就是使氯化铵电离 2020-05-13 …
下列对光反应描述不正确的是A.叶绿素吸收光能并将光能转化为ATP中的化学能B.电子传递链到达最终的 2020-05-15 …
电解H2O和D2O的混合物,通电一段时间后,两极共产生气体18.5g,其体积在标准状况下是33.6 2020-07-09 …
头都大了,哪位大虾帮忙翻译一下!每生产1.5Nm3氢氧混合燃气耗电4KW.h,而氧乙炔是由高耗电能 2020-07-11 …
氯气和氨气生成氯化铵和氮气的电子转移用双线桥法如何表示 2020-07-22 …
用初中电解水的实验装置电解水和重水(D2O)组成的混合液,通电一段时间后,在两极共收集到33.6L( 2020-12-17 …
下列关于铵盐的叙述中正确的是()①所有铵盐都有氨的刺激性气味②所有铵盐都溶于水③铵盐不稳定,受热易分 2020-12-20 …