早教吧作业答案频道 -->化学-->
I.碱性锌锰干电池的总反应为Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2.该电池中,负极材料是,正极反应式为.Ⅱ.以废旧锌锰干电池处理得到的混合物为原料制备锰锌铁氧体的主要流程如图1所示.
题目详情
I.碱性锌锰干电池的总反应为Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2.该电池中,负极材料是___,正极反应式为___.
Ⅱ.以废旧锌锰干电池处理得到的混合物为原料制备锰锌铁氧体的主要流程如图1所示.
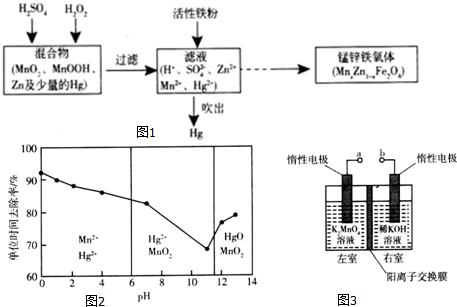
请回答下列问题:
(1)MnxZn1-xFe2O4中铁元素化合价为+3,则锰元素的化合价为___.
(2)活性铁粉除汞时,铁粉的作用是___(填“氧化剂”或“还原剂”).
(3)除汞是以氮气为载气吹入滤液中,带出汞蒸气经KMnO4溶液进行吸收而实现的.在恒温下不同pH时,KMnO4溶液对Hg的单位时间去除率及主要产物如图2所示.
①写出pH=2时KMnO4溶液吸收汞蒸气的离子方程式___.
②在强酸性环境中汞的单位时间去除率高,其原因除氢离子浓度增大使KMnO4溶液的氧化性增强外,还可能是___.
(4)用惰性电极电解K2MnO4溶液制备KMnO4的装置如图3所示.
①a应接直流电源的___(填“正”或“负”)极.
②已知25℃,两室溶液的体积均为100mL,电解一段时间后,右室溶液的pH由10变为14,则理论上可制得___mol KMnO4 (忽略溶液的体积和温度变化).
Ⅱ.以废旧锌锰干电池处理得到的混合物为原料制备锰锌铁氧体的主要流程如图1所示.

请回答下列问题:
(1)MnxZn1-xFe2O4中铁元素化合价为+3,则锰元素的化合价为___.
(2)活性铁粉除汞时,铁粉的作用是___(填“氧化剂”或“还原剂”).
(3)除汞是以氮气为载气吹入滤液中,带出汞蒸气经KMnO4溶液进行吸收而实现的.在恒温下不同pH时,KMnO4溶液对Hg的单位时间去除率及主要产物如图2所示.
①写出pH=2时KMnO4溶液吸收汞蒸气的离子方程式___.
②在强酸性环境中汞的单位时间去除率高,其原因除氢离子浓度增大使KMnO4溶液的氧化性增强外,还可能是___.
(4)用惰性电极电解K2MnO4溶液制备KMnO4的装置如图3所示.
①a应接直流电源的___(填“正”或“负”)极.
②已知25℃,两室溶液的体积均为100mL,电解一段时间后,右室溶液的pH由10变为14,则理论上可制得___mol KMnO4 (忽略溶液的体积和温度变化).
▼优质解答
答案和解析
Ⅰ、碱性锌锰电池的总反应是:Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2,Zn为负极,Zn失电子生成锌离子,正极MnO2得电子被还原生成MnOOH,反应式为MnO2+H2O+e-═MnOOH+OH-,故答案为:Zn;MnO2+e-+H2O=MnOOH+OH-;Ⅱ、(1)...
看了 I.碱性锌锰干电池的总反应为...的网友还看了以下:
已知曲线C1的参数方程为x=4+5cost,y=5+5sint,以坐标原点为极点,x轴的正半轴为极 2020-06-14 …
在直角坐标系xOy中,以O为极点,x轴正半轴为极轴建立极坐标系.已知圆C的极坐标方程为ρ2-42ρ 2020-07-31 …
在平面直角坐标系中、以坐标原点O为极点、x轴的正半轴为极轴建立极坐标系、已知曲线c的极坐标方程ps 2020-07-31 …
已知圆的参数方程为(为参数),以坐标原点为极点,x轴的正半轴为极轴建立极坐标系,圆的极坐标方程为. 2020-07-31 …
已知直线l的参数方程为x=−10+ty=t(t为参数),以坐标原点为极点,x轴的正半轴为极轴建立极 2020-07-31 …
已知圆C1的参数方程为(φ为参数),以坐标原点O为极点,x轴的正半轴为极轴建立极坐标系,圆C2的极 2020-07-31 …
曲线C1的参数方程为x=2+2cosαy=2sinα(α为参数)在以原点O为极点,x轴的非负半轴为 2020-07-31 …
已知曲线C1的方程为x2+y2-8x-10y+16=0.以坐标原点为极点,x轴的正半轴为极轴建立极坐 2020-10-31 …
已知测定锰的一种方法是:锰离子转化为高锰酸根离子,反应体系中有H+、Mn2+、H2O、IO3-、Mn 2020-12-25 …
已知圆的参数方程为(为参数),以坐标原点O为极点,x轴的正半轴为极轴建立极坐标系,圆的极坐标方程为. 2021-02-10 …