早教吧作业答案频道 -->化学-->
面对日益严重的资源短缺及环境污染问题,“变废为宝”成为化学发展的新方向.废旧酸性锌锰干电池经分离破碎后的锰粉含Mn02、Mn0(0H)、Zn(NH3)CL2、Fe、NH4C1和炭黑等,可用于制取Mn02高
题目详情
面对日益严重的资源短缺及环境污染问题,“变废为宝”成为化学发展的新方向.废旧酸性锌锰干电池经分离破碎后的锰粉含Mn02、Mn0(0H)、Zn(NH3)CL2、Fe、NH4C1和炭黑等,可用于制取Mn02高性能磁性材料MnC03,其工艺流程如下:
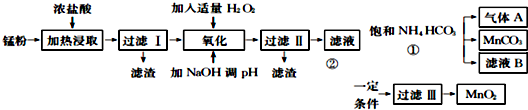
已知几种氢氧化物开始沉淀和完全沉淀的pH如表:
回答下列问题:
(1)过滤工得到的滤渣主要成分是___.
(2)滤液经氧化后加入NaOH溶液调节pH至8.5〜8.8,其目的是___.
(3)过滤Ⅱ得到的滤液中含有的阳离子主要是___(填离子符号).
(4)过程①中发生反应的离子方程式为___,对气体A和滤液B应采取的处理方法分别是___.
(5)过程②得到MnO2.将MnO2成悬浊液,通S02还原可得MnSO4,再加入Na2CO3或NaHCO3,也可制备MnCO3.SO2还原MnO2的化学方程式为___,向MnS04溶液中加入Na2C03或NaHC03制备MnC03时应注意的问题是___.

已知几种氢氧化物开始沉淀和完全沉淀的pH如表:
| 氢氧化物 | Fe(OH) | Fe(OH) | Mn0H)2 | Zn(OH)2 |
| 开始沉淀的pH | 7.5 | 2.2 | 8.8 | 6.4 |
| 沉淀完全的pH | 9.5 | 3.7 | 10.8 | 8.5 |
(1)过滤工得到的滤渣主要成分是___.
(2)滤液经氧化后加入NaOH溶液调节pH至8.5〜8.8,其目的是___.
(3)过滤Ⅱ得到的滤液中含有的阳离子主要是___(填离子符号).
(4)过程①中发生反应的离子方程式为___,对气体A和滤液B应采取的处理方法分别是___.
(5)过程②得到MnO2.将MnO2成悬浊液,通S02还原可得MnSO4,再加入Na2CO3或NaHCO3,也可制备MnCO3.SO2还原MnO2的化学方程式为___,向MnS04溶液中加入Na2C03或NaHC03制备MnC03时应注意的问题是___.
▼优质解答
答案和解析
锰粉[含MnO2、MnO(OH)、Zn(NH3)2Cl2、Fe、NH4Cl和炭黑等]在浓盐酸中加热、浸取,发生MnO2+4HCl
MnCl2+Cl2↑+2H2O、2MnO(OH)+6HCl=2MnCl2+Cl2↑+3H2O、Fe+2HCl=FeCl2+H2↑等反应,过滤后所得滤渣为碳黑,滤液中含有Mn2+、Fe2+、NH4+、Zn2+等离子,在滤液中加入适量过氧化氢和氢氧化钠,可将Fe2+转化为Fe3+,并生成Fe(OH)3,控制溶液pH在8.5<pH<8.8之间可以除去Fe3+、Zn2+,过滤后所得滤液Ⅱ主要为Mn2+,滤液Ⅱ中H2O2溶液,在一定条件下使Mn2+转化成MnO2,经过滤、洗涤、干燥可得MnO2,滤液Ⅱ中加入碳酸氢铵饱和溶液,发生反应Mn2++2HCO3-=MnCO3+CO2↑+H2O,得到碳酸锰沉淀、氯化铵溶液和气体A为CO2,
(1)根据上面的分析可知,过滤Ⅰ得到的滤渣主要成分是碳黑,
故答案为:碳黑;
(2)流程中氧化后加入NaOH溶液调节pH的范围为8.5<pH<8.8,其作用是除去Fe3+、Zn2+,
故答案为:除去Fe3+、Zn2+;
(3)过滤Ⅱ后滤液中阳离子主要是Mn2+、NH4+、Na+,
故答案为:Mn2+、NH4+、Na+;
(4)滤液Ⅱ中加入碳酸氢铵饱和溶液,发生反应Mn2++2HCO3-=MnCO3+CO2↑+H2O;气体A是 CO2,CO2循环利用,可以用于生产NH4HCO3;滤液B中含有NH4Cl,可分离用作氮肥;
故答案为:Mn2++2HCO3-=MnCO3+CO2↑+H2O;CO2循环利用,用于生产NH4HCO3;滤液B中含有NH4Cl,可分离用作氮肥;
(5)过程②得到MnO2.将MnO2成悬浊液,通S02还原可得MnSO4,其反应方程式为:MnO2+S02=MnSO4;向MnS04溶液中加入Na2C03或NaHC03制备MnC03,边加边搅拌,为了防止锰离子水解生成沉淀,溶液的pH要小于8.8;
故答案为:MnO2+S02=MnSO4;边搅拌边加入Na2C03或NaHC03,并控制溶液的pH<8.8.
| ||
(1)根据上面的分析可知,过滤Ⅰ得到的滤渣主要成分是碳黑,
故答案为:碳黑;
(2)流程中氧化后加入NaOH溶液调节pH的范围为8.5<pH<8.8,其作用是除去Fe3+、Zn2+,
故答案为:除去Fe3+、Zn2+;
(3)过滤Ⅱ后滤液中阳离子主要是Mn2+、NH4+、Na+,
故答案为:Mn2+、NH4+、Na+;
(4)滤液Ⅱ中加入碳酸氢铵饱和溶液,发生反应Mn2++2HCO3-=MnCO3+CO2↑+H2O;气体A是 CO2,CO2循环利用,可以用于生产NH4HCO3;滤液B中含有NH4Cl,可分离用作氮肥;
故答案为:Mn2++2HCO3-=MnCO3+CO2↑+H2O;CO2循环利用,用于生产NH4HCO3;滤液B中含有NH4Cl,可分离用作氮肥;
(5)过程②得到MnO2.将MnO2成悬浊液,通S02还原可得MnSO4,其反应方程式为:MnO2+S02=MnSO4;向MnS04溶液中加入Na2C03或NaHC03制备MnC03,边加边搅拌,为了防止锰离子水解生成沉淀,溶液的pH要小于8.8;
故答案为:MnO2+S02=MnSO4;边搅拌边加入Na2C03或NaHC03,并控制溶液的pH<8.8.
看了 面对日益严重的资源短缺及环境...的网友还看了以下:
近几十年随着森林不断遭到砍伐,马鹿的栖息环境受到了很大的破坏.为了更好的保护马鹿,科研人员进行了研 2020-06-11 …
刚捕了几只头上有束长长的毛的鸟,圆圆的头弯弯的嘴和短短的脚黑色羽毛翅膀有点白色和肚子白色像鹰... 2020-06-15 …
植物的开花受光周期的影响,短日照植物的花诱导要求长夜,而长日照植物则要求短夜.若以短暂的黑夜中断其 2020-06-27 …
你一定和同学们一起寻找过鼠妇,一般在哪种环境里最容易找到?()A.黑暗干燥的沙土环境B.黑暗潮湿的 2020-07-02 …
你一定和同学们一起寻找过鼠妇,一般在哪种环境里最容易找到?()A.黑暗干燥的沙土环境B.黑暗潮湿的 2020-07-02 …
2.资源枯竭和环境破坏都有哪些表现?资源枯竭环境破坏(1)减少(2)土地荒漠化(3)短缺(4)能源匮 2020-11-04 …
短跑名将博尔特在北京奥运会100和200米短跑破记录,所用时间为9.69s和19.30s.假定他在一 2020-11-26 …
环保英语作文,去了一个公园去公园的目的(对环境好的事)人们在干什么发现有人破坏环境告诉他不该破坏环境 2020-12-10 …
人口增长慢带来的问题是()A.社会抚养老年人的负担加重,国防兵源不足B.就业困难、交通拥挤、住房紧张 2020-12-18 …
下列问题中与人口增长过快无关的是()A.环境破坏,资源短B.人口出现老龄化C.交通拥挤,污染严重D. 2020-12-18 …