早教吧作业答案频道 -->化学-->
现向含6molKI的硫酸溶液中逐滴加入KBrO3溶液,整个过程中含碘物质的物质的量与所加入KBrO3的物质的量的关系如图所示.已知①BrO3-+6I一+6H+=3I2+Br-+3H2O;②2BrO3-+I2=2IO3-+Br2;请回答下列问题:
题目详情
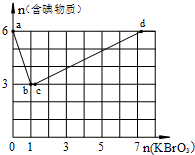
现向含6mol KI的硫酸溶液中逐滴加入KBrO3溶液,整个过程中含碘物质的物质的量与所加入KBrO3的物质的量的关系如图所示.
已知①BrO3-+6I一+6H+=3I2+Br-+3H2O;
②2BrO3-+I2=2IO3-+Br2;
请回答下列问题:
(1)由反应②有同学由此得出氧化性:I2>Br2的结论,你认为是否正确___(填是或否),并说明理由___
(2)b点时,KI反应完全,则消耗的氧化剂与还原剂物质的量之比为___,还原产物是___.
(3)b→c过程中只有一种元素的化合价发生变化,写出该过程的离子反应方程式___.
(4)含6mol KI的硫酸溶液所能消耗n(KBrO3)的最大值为___mol.
(5)n(KBrO3)=4mol时,对应含碘物质的化学式为___.
(6)若实验室需要6mol•L-1的KI溶液480mL,根据配制情况回答下列问题:
①实验室中除了托盘天平、烧杯、药匙、量筒外还需要的其它仪器有___.
②下列操作使所配溶液浓度偏低的有___(填字母);
A.容量瓶未干燥就用来配制溶液B.定容时,加蒸馏水超过刻度线,又用胶头滴管吸出
C.往容量瓶转移时有少量液体溅出 D.定容时仰视刻度线.
已知①BrO3-+6I一+6H+=3I2+Br-+3H2O;
②2BrO3-+I2=2IO3-+Br2;
请回答下列问题:

(1)由反应②有同学由此得出氧化性:I2>Br2的结论,你认为是否正确___(填是或否),并说明理由___
(2)b点时,KI反应完全,则消耗的氧化剂与还原剂物质的量之比为___,还原产物是___.
(3)b→c过程中只有一种元素的化合价发生变化,写出该过程的离子反应方程式___.
(4)含6mol KI的硫酸溶液所能消耗n(KBrO3)的最大值为___mol.
(5)n(KBrO3)=4mol时,对应含碘物质的化学式为___.
(6)若实验室需要6mol•L-1的KI溶液480mL,根据配制情况回答下列问题:
①实验室中除了托盘天平、烧杯、药匙、量筒外还需要的其它仪器有___.
②下列操作使所配溶液浓度偏低的有___(填字母);
A.容量瓶未干燥就用来配制溶液B.定容时,加蒸馏水超过刻度线,又用胶头滴管吸出
C.往容量瓶转移时有少量液体溅出 D.定容时仰视刻度线.
▼优质解答
答案和解析
(1)根据反应:2BrO3-+I2═2IO3-+Br2,还原剂的还原性强于还原产物的氧化性,所以得出还原性I2>Br2,
故答案为:否;该反应中I2作还原剂,Br2为还原产物,应得出还原性I2>Br2结论;
(2)b点时,KI反应完全,有图象可知参加反应的KI为6mol,KBrO3为1mol,则消耗的氧化剂与还原剂物质的量之比为1:6,
发生反应为6I-+BrO3-=Br-+3I2,还原产物是KBr,
故答案为:1:6;KBr;
(3)b→c过程中,仅有一种元素发生化合价变化,应是BrO3-与Br-之间的氧化还原反应,反应的离子方程式为BrO3-+5Br-+6H+=3Br2+3H2O,
故答案为:BrO3-+5Br-+6H+=3Br2+3H2O;
(4)发生的反应依次有6I-+6H++BrO3-=Br-+3I2+3H2O,BrO3-+5Br-+6H+=3Br2+3H2O,2BrO3-+I2=2IO3-+Br2,
总反应为5I-+6H++6BrO3-=5IO3-+3Br2+3H2O,则含6molKI的硫酸溶液所能消耗n(KBrO3)的最大值为1.2×6mol=7.2mol,
故答案为:7.2;
(5)n(KBrO3)=4时,发生的反应依次有6I-+BrO3-=Br-+3I2,BrO3-+5Br-+6H+=3Br2+3H2O,2BrO3-+I2=2IO3-+Br2,6molKI生成I2,需要1molKBrO3,同时生成1molKBr,发生BrO3-+5Br-+6H+=3Br2+3H2O,需要0.2molKBrO3,如I2完全被氧化生成KIO3,还应需要6molKBrO3,
则n(KBrO3)=4时,对应含碘物质的化学式为I2,KIO3,
故答案为:I2,KIO3;
(6)①6mol•L-1的KI溶液480mL,托盘天平、烧杯、药匙、量筒外还需要的其它仪器有:玻璃棒、胶头滴管、500ml 容量瓶,故答案为:玻璃棒、胶头滴管、500ml 容量瓶;
②A.容量瓶未干燥就用来配制溶液,无影响,故不选;
B.定容时,加蒸馏水超过刻度线,又用胶头滴管吸出,溶质的量减少,浓度偏低,故选;
C.往容量瓶转移时有少量液体溅出,溶质的量减少,浓度偏低,故选;
D.定容时仰视刻度线,体积变大,浓度偏低,故选,
故选:BCD.
故答案为:否;该反应中I2作还原剂,Br2为还原产物,应得出还原性I2>Br2结论;
(2)b点时,KI反应完全,有图象可知参加反应的KI为6mol,KBrO3为1mol,则消耗的氧化剂与还原剂物质的量之比为1:6,
发生反应为6I-+BrO3-=Br-+3I2,还原产物是KBr,
故答案为:1:6;KBr;
(3)b→c过程中,仅有一种元素发生化合价变化,应是BrO3-与Br-之间的氧化还原反应,反应的离子方程式为BrO3-+5Br-+6H+=3Br2+3H2O,
故答案为:BrO3-+5Br-+6H+=3Br2+3H2O;
(4)发生的反应依次有6I-+6H++BrO3-=Br-+3I2+3H2O,BrO3-+5Br-+6H+=3Br2+3H2O,2BrO3-+I2=2IO3-+Br2,
总反应为5I-+6H++6BrO3-=5IO3-+3Br2+3H2O,则含6molKI的硫酸溶液所能消耗n(KBrO3)的最大值为1.2×6mol=7.2mol,
故答案为:7.2;
(5)n(KBrO3)=4时,发生的反应依次有6I-+BrO3-=Br-+3I2,BrO3-+5Br-+6H+=3Br2+3H2O,2BrO3-+I2=2IO3-+Br2,6molKI生成I2,需要1molKBrO3,同时生成1molKBr,发生BrO3-+5Br-+6H+=3Br2+3H2O,需要0.2molKBrO3,如I2完全被氧化生成KIO3,还应需要6molKBrO3,
则n(KBrO3)=4时,对应含碘物质的化学式为I2,KIO3,
故答案为:I2,KIO3;
(6)①6mol•L-1的KI溶液480mL,托盘天平、烧杯、药匙、量筒外还需要的其它仪器有:玻璃棒、胶头滴管、500ml 容量瓶,故答案为:玻璃棒、胶头滴管、500ml 容量瓶;
②A.容量瓶未干燥就用来配制溶液,无影响,故不选;
B.定容时,加蒸馏水超过刻度线,又用胶头滴管吸出,溶质的量减少,浓度偏低,故选;
C.往容量瓶转移时有少量液体溅出,溶质的量减少,浓度偏低,故选;
D.定容时仰视刻度线,体积变大,浓度偏低,故选,
故选:BCD.
看了现向含6molKI的硫酸溶液中...的网友还看了以下:
已知:I2+2S2O2-3=S4O2-6+2I-.相关物质的溶度积常数见下表:物质Cu(OH)2Fe 2020-03-30 …
已知A²-B²=6,A-B=3.求4AB等于多少?一 :(A-B)²=A²-B²-2AB已知 A² 2020-05-15 …
下列是水体污染过程中的一系列现象,(1)溶解氧下降(2)鱼类难以生存(3)水中有机物浓度增加(4) 2020-05-17 …
(2/3)6克,B管质量增加了9.24克,已知该有机物相对分子质量为108.(1)燃烧此化合物3. 2020-05-23 …
如图,密度为0.6*10^3/m^3,的正方体木块,放入盛有水的柱形容器中静止时,木块的下表面距水 2020-05-23 …
已知一串分数1/3,2/3,1/6,2/6,3/6,4/6,5/6,1/9,2/9,3/9,9/4 2020-06-05 …
已知抛物线y=x2-2x+3经过点B(3,6),与y轴交于点A(0,3),若点M是直线AB:y=x 2020-07-10 …
科学家认为,在宇宙的构成中,人类已知物质仅占4%左右,而暗物质几乎是已知物质的6倍,但人类一点未找到 2020-12-29 …
化成最简整数比:(1)3分之2:6分之5:9分之8=(2)已知x:2y=3:4,则x:y为()A.3 2021-01-12 …
常温时,已知:I2+2S2O2−3=S4O2−6+2I-.相关物质的溶度积常数见下表:物质Cu(OH 2021-01-12 …