早教吧作业答案频道 -->化学-->
某小组欲探究Cl2与KI溶液的反应,设计实验装置如下图.已知:I2在水中溶解度很小,在KI溶液中溶解度显著增大,I2(S)+I-⇌I3-(aq).容器中盛放的试剂分别为:A.MnO2C.0.5000mol/L的KI溶液D
题目详情
某小组欲探究Cl2与KI溶液的反应,设计实验装置如下图.
已知:I2在水中溶解度很小,在KI溶液中溶解度显著增大,I2(S)+I-⇌I3-(aq).
容器中盛放的试剂分别为:
A.MnO2
C.0.5000mol/L的KI溶液
D.AgNO3溶液
E.NaOH溶液
F.浓盐酸
完成下列填空:
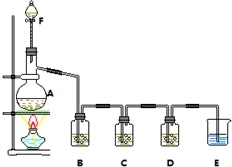
(1)仪器A的名称___,B中的试剂是___.
(2)当D装置中出现___ 时,停止加热;E的作用是___.
(3)当氯气开始进入C时,C中看到的现象是___;不断向C中通入氯气,看到溶液颜色逐渐加深,后来出现深褐色沉淀,试运用平衡移动原理分析产生这些现象的原因___.
(4)持续不断地向C中通入氯气,看到C中液体逐渐澄清,最终呈无色.推测此时C中无色溶液里含碘物质的化学式___(此时溶液中只有一种含碘微粒).
为确定含碘物质中碘元素的化合价,进行如下实验:
①取反应后C中溶液5.00mL(均匀)于锥形瓶中,加入KI(过量)和足量稀硫酸.
②向上述锥形瓶中滴加淀粉指示剂,溶液变蓝,用0.6250mol/L的Na2S2O3溶液滴定至蓝色刚好褪去,耗Na2S2O3溶液24.00mL.
已知:I2+2S2O32-→2I-+S4O62-
计算:碘元素的化合价为___.
(5)欲检验某溶液中是否含有I-,可使用的试剂为氯水和淀粉溶液.合理的实验操作为___.
已知:I2在水中溶解度很小,在KI溶液中溶解度显著增大,I2(S)+I-⇌I3-(aq).
容器中盛放的试剂分别为:
A.MnO2
C.0.5000mol/L的KI溶液
D.AgNO3溶液
E.NaOH溶液
F.浓盐酸
完成下列填空:

(1)仪器A的名称___,B中的试剂是___.
(2)当D装置中出现___ 时,停止加热;E的作用是___.
(3)当氯气开始进入C时,C中看到的现象是___;不断向C中通入氯气,看到溶液颜色逐渐加深,后来出现深褐色沉淀,试运用平衡移动原理分析产生这些现象的原因___.
(4)持续不断地向C中通入氯气,看到C中液体逐渐澄清,最终呈无色.推测此时C中无色溶液里含碘物质的化学式___(此时溶液中只有一种含碘微粒).
为确定含碘物质中碘元素的化合价,进行如下实验:
①取反应后C中溶液5.00mL(均匀)于锥形瓶中,加入KI(过量)和足量稀硫酸.
②向上述锥形瓶中滴加淀粉指示剂,溶液变蓝,用0.6250mol/L的Na2S2O3溶液滴定至蓝色刚好褪去,耗Na2S2O3溶液24.00mL.
已知:I2+2S2O32-→2I-+S4O62-
计算:碘元素的化合价为___.
(5)欲检验某溶液中是否含有I-,可使用的试剂为氯水和淀粉溶液.合理的实验操作为___.
▼优质解答
答案和解析
(1)A中是制备氯气的装置,依据仪器图形和用途可知A是蒸馏烧瓶,B中是用来除去氯气中的氯化氢气体,所以用饱和食盐水,
故答案为:蒸馏烧瓶,饱和食盐水;
(2)氯气的KI溶液反应之后,剩余的氯气进入硝酸银溶液,装置D中生成氯化银白色沉淀;未反应的氯气进入装置E中的氢氧化钠溶液被吸收,
故答案为:白色沉淀,吸收未反应的氯气;
(3)氯气开始进入C时,将碘离子氧化成单质碘,所以开始溶液变棕黄色;不断向C中通入氯气,看到溶液颜色逐渐加深,后来出现深褐色沉淀,因为被置换出来的I2在KI溶液中溶解度、较大,所以溶液颜色逐渐加深,但随着反应KI被消耗,平衡I2(S)+I-⇌I3-(aq)向左移动,碘在水中的溶解度较小,所以部分碘以沉淀的形式析出,
故答案为:溶液变棕黄色,被置换出来的I2在KI溶液中溶解度、较大,所以溶液颜色逐渐加深,但随着反应KI被消耗,平衡I2(S)+I-⇌I3-(aq)向左移动,碘在水中的溶解度较小,所以部分碘以沉淀的形式析出;
(4)氯气过量时会将碘继续氧化成HIO3;Na2S2O3的物质的量=0.625×0.024=0.015mol,C中原I-的物质的量=0.005×0.5=0.0025mol,
设被氯气氧化为x价,据反应I2+2S2O32-→2I-+S4O62-,得反应的碘单质物质的量=0.015mol×
=0.0075mol,碘原子共0.015mol,
x价碘生成的占0.0025mol,则碘离子生成的为0.015-0.0025=0.0125mol,
据化合价升降相等得:0.0025x=0.0125,x=5,
所以碘元素的化合价为+5价,
故答案为:HIO3,+5;
(5)检验某溶液中是否含有I-,取样,滴加淀粉溶液,振荡均匀后再逐滴加入氯水并振荡,
故答案为:取样滴加淀粉溶液,振荡均匀后再逐滴加入氯水并振荡;
故答案为:蒸馏烧瓶,饱和食盐水;
(2)氯气的KI溶液反应之后,剩余的氯气进入硝酸银溶液,装置D中生成氯化银白色沉淀;未反应的氯气进入装置E中的氢氧化钠溶液被吸收,
故答案为:白色沉淀,吸收未反应的氯气;
(3)氯气开始进入C时,将碘离子氧化成单质碘,所以开始溶液变棕黄色;不断向C中通入氯气,看到溶液颜色逐渐加深,后来出现深褐色沉淀,因为被置换出来的I2在KI溶液中溶解度、较大,所以溶液颜色逐渐加深,但随着反应KI被消耗,平衡I2(S)+I-⇌I3-(aq)向左移动,碘在水中的溶解度较小,所以部分碘以沉淀的形式析出,
故答案为:溶液变棕黄色,被置换出来的I2在KI溶液中溶解度、较大,所以溶液颜色逐渐加深,但随着反应KI被消耗,平衡I2(S)+I-⇌I3-(aq)向左移动,碘在水中的溶解度较小,所以部分碘以沉淀的形式析出;
(4)氯气过量时会将碘继续氧化成HIO3;Na2S2O3的物质的量=0.625×0.024=0.015mol,C中原I-的物质的量=0.005×0.5=0.0025mol,
设被氯气氧化为x价,据反应I2+2S2O32-→2I-+S4O62-,得反应的碘单质物质的量=0.015mol×
| 1 |
| 2 |
x价碘生成的占0.0025mol,则碘离子生成的为0.015-0.0025=0.0125mol,
据化合价升降相等得:0.0025x=0.0125,x=5,
所以碘元素的化合价为+5价,
故答案为:HIO3,+5;
(5)检验某溶液中是否含有I-,取样,滴加淀粉溶液,振荡均匀后再逐滴加入氯水并振荡,
故答案为:取样滴加淀粉溶液,振荡均匀后再逐滴加入氯水并振荡;
看了某小组欲探究Cl2与KI溶液的...的网友还看了以下:
试用离子反应式和简要文字表述以下事实:(1)盛纯碱溶液的试剂瓶用玻璃塞,时间长了不易打开。(2)盛 2020-05-02 …
谁能告诉我爱情公式爱情={[(F+Ch+P)/2]+[3(C+I)]/10}/[(5-SI)2+2 2020-05-21 …
线怀代数证明题.设n阶矩阵B满足B^2=B,I为n阶单位矩阵,证明:1,若B不等于I,则B不可逆2 2020-06-03 …
2.在盛世繁荣中,社会危机隐隐浮现,给盛世投下阴影。其主要表现有()①人口增长过快②官场风气腐败, 2020-06-19 …
设正弦电流i=100sin(314t-6o度)A.试问(1)它的频率周期最大值有效值初相位各是多少 2020-07-19 …
关于复数的(1)试求i,i^2,i^3,i^4,i^5,i^6,i^7,i^8的值;(2)由(1) 2020-07-26 …
虚数化简1/4*(-4+4*i*3^(1/2))^(1/3)+1/(-4+4*i*3^(1/2)) 2020-07-30 …
我们将学习虚数i,(i叫虚数单位).规定i2=-1,如-2=2×(-1)=(±)2•i2=(±i) 2020-07-30 …
高中选修2—2的第三章数系的扩充和复数的概念的习题试求i^1,i^2,i^3,i^4,i^5,i^6 2020-10-30 …
某化学小组同学按下图所示装置和表中所给试剂进行实验(图中铁架台等夹持仪器均已略去):组别A组B组C组 2020-12-19 …