下图Ⅰ、Ⅱ分别是甲、乙两组同学将反应“AsO+2I-+2H+AsO+I2+H2O”设计成的原电池装置,其中C1、C2均为碳棒。甲组向图Ⅰ烧杯中逐
下图Ⅰ、Ⅱ分别是甲、乙两组同学将反应 “AsO ![]() + 2I -+ 2H + AsO
+ 2I -+ 2H + AsO ![]() + I2 + H2O” 设计成的原电池装置,其中 C1 、 C2 均为碳棒。甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图Ⅱ B 烧杯中逐滴加入适量 40% NaOH 溶液。
+ I2 + H2O” 设计成的原电池装置,其中 C1 、 C2 均为碳棒。甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图Ⅱ B 烧杯中逐滴加入适量 40% NaOH 溶液。
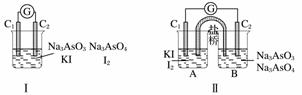
下列叙述中正确的是 ( )
A .甲组操作时,电流计 (G) 指针发生偏转
B .甲组操作时,溶液颜色变浅
C .乙组操作时, C2 作正极
D .乙组操作时, C1 上发生的电极反应为 I2 + 2e - ===2I -
答案 D
解析 装置Ⅰ中的反应, AsO ![]() + 2I -+ 2H + AsO
+ 2I -+ 2H + AsO ![]() + I2 + H2O ,当加入适量浓盐酸时,平衡向右移动,有电子转移,但电子不会沿导线通过,所以甲组操作时,电流计 (G) 指针不会发生偏转,但由于 I2 浓度增大,所以溶液颜色变深;向装置Ⅱ B 烧杯中加入 NaOH 溶液中, AsO
+ I2 + H2O ,当加入适量浓盐酸时,平衡向右移动,有电子转移,但电子不会沿导线通过,所以甲组操作时,电流计 (G) 指针不会发生偏转,但由于 I2 浓度增大,所以溶液颜色变深;向装置Ⅱ B 烧杯中加入 NaOH 溶液中, AsO ![]() - 2e -+ H2O===AsO
- 2e -+ H2O===AsO ![]() + 2H +,电子沿导线到 C1 棒, I2 + 2e - ===2I -,所以 C2 为负极, C1 为正极。
+ 2H +,电子沿导线到 C1 棒, I2 + 2e - ===2I -,所以 C2 为负极, C1 为正极。
已知:2H2(g)+O2(g)=2H2O(l)ΔH=-571.6kJ·mol-1①2CH3OH(l 2020-04-07 …
NaOH的溶液的PH值为9,所以溶液的H+为10-9.OH-为10-5,那么水电离的OH-和H+浓 2020-05-16 …
进行下列数的数制转换(213)D=()B=()H=()O(69.625)D=()B=()H=()O 2020-05-21 …
H-1、H-2、H-3与O-16、O-17、O-18六种核素,组成水的分子类型总数是( )A.6种B 2020-06-07 …
请教几个关于国际贸易的问题1、赫克歇尔-俄林模型(即H-O模型)比古典学派贸易模型多的一个投入要素 2020-06-19 …
H-O-H,每mol水中含2molH-O键含2mol的H-O键,H-O-H中的H-O?H-O是什么 2020-06-28 …
进制换算(213)D=()B=()H=()O(69.625)D=()D=()B=()O(127)D 2020-07-19 …
已知:2H2(g)+O2(g)=2H2O(g)ΔH=-483.6kJ/mol下列说法不正确的是A. 2020-07-19 …
第二步不理解,泰勒公式的余项与多项式的运算法则是什么㏑(1-2x+3x^2)=-2x+3x^2-0. 2020-11-07 …
某有机物由C,H,O三种元素组成,它的红外吸收光谱表明有羟基中O—H键和烃基中C—H键的红外某有机物 2020-11-25 …