已知:还原性HSO3->I-,氧化性IO3->I2.在含3molNaHSO3的溶液中逐滴加入NaIO3溶液.加入NaIO3的物质的量和析出的I2的物质的量的关系曲线如图所示.下列说法正确的是()A.反应过程中的
已知:还原性HSO3->I-,氧化性IO3->I2.在含3molNaHSO3的溶液中逐滴加入NaIO3溶液.加入NaIO3的物质的量和析出的I2的物质的量的关系曲线如图所示.下列说法正确的是( )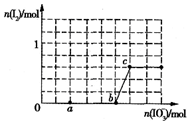
A. 反应过程中的氧化产物均为Na2HSO4
B. a点时剩余NaHSO3的物质的量为1.0 mol
C. 0~b间的反应可用如下离子方程式表示:3HSO3-+IO3-+3OH-=3SO43-+I-+3H2O
D. 当溶液中I-与I2的物质的量之比为5:3时,加入的NaIO3为1.1mol
B.a点碘酸钾的物质的量是0.4mol,根据碘酸钾和亚硫酸氢钠的关系式知,消耗NaHSO3的物质的量=
| 0.4mol |
| 1 |
C.0~b间没有碘单质生成,说明碘酸根离子和亚硫酸氢根离子发生氧化还原反应生成碘离子,加入碘酸钾的物质的量是1mol,亚硫酸氢钠的物质的量是3mol,亚硫酸氢根被氧化生成硫酸根离子,根据转移电子守恒知,生成碘离子,所以其离子方程式为:3HSO3-+IO3-═3SO42-+I-+3H+,故C错误;
D.根据反应IO3-+3HSO3-═I-+3SO42-+3H+,3mol NaHSO3的溶液消耗KIO3溶液的物质的量为1mol,生成碘离子的量为1mol,设生成的碘单质的物质的量为n,则根据反应IO3-+6H++5I-=3H2O+3I2,消耗的KIO3的物质的量为
| n |
| 3 |
| 5n |
| 3 |
| 5n |
| 3 |
| 5n |
| 3 |
| 3 |
| 10 |
| n |
| 3 |
| 1 |
| 10 |
故选D.
在平行四边形ABCD中E为CD上一点,DE:EC=1:2,连接AE、BE、BD,且AE、BD交于点 2020-05-13 …
当n为正整数时,定义函数N(n)表示n的最大奇因数.如N(3)=3,N(10)=5,….记S(n) 2020-05-13 …
当n为正整数时,定义函数N(n)表示n的最大奇因数.如N(3)=3,N(10)=5,….记S(n) 2020-05-13 …
8.如图示电路中,电源电动势E = 9V8.如图示电路中,电源电动势E = 9V、内阻r = 3Ω 2020-05-16 …
求函数的拉氏反变换:X(s)=(s+2)/[s·(s+1)^2·(s+3)]我的解法如下:X(s) 2020-05-22 …
物理单位换算问题(1km/h=多少m/s)需要换算过程按理说1km/h=1000m/3600s=1 2020-06-09 …
设a32a2ra14a51a4s是五阶行列式中的项,则下列中的值及该项的符号均对的是().A.r= 2020-07-25 …
称为“可倒数集”,试写出1个“可倒数集”集合S=3,1/3不对举个并说理由急对于1个数集S,若a属于 2020-11-02 …
20、有一个字符串变量s,要得到该字符串变量从第3个字符开始的共4个字符的函数是()。A.Right 2020-11-07 …
已知C(石墨,s)=C(金刚石,s)△H1>0,P(白磷,s)=P(红磷,s)△H2<0下列判断正确 2020-12-24 …