早教吧作业答案频道 -->化学-->
砷的常见酸性氧化物有As2O3和As2O5,根据图中信息回答下列问题:(1)As2O5分解生成As2O3和O2的反应中,加入催化剂,E(填“增大”、“减小”或“不变”,下同),△H1.(2)As2O3分解
题目详情
砷的常见酸性氧化物有As2O3和As2O5,根据图中信息回答下列问题:
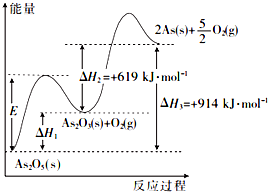
(1)As2O5分解生成As2O3和O2的反应中,加入催化剂,E___(填“增大”、“减小”或“不变”,下同),△H1___.
(2)As2O3分解生成As和O2的热化学方程式为___.
(3)As2O3和O2反应生成As2O5的热化学方程式为___.
(4)若1mol As2O5分解生成0.4mol As2O3和1.2mol As,则该分解过程中,需吸收的总能量为___kJ.

(1)As2O5分解生成As2O3和O2的反应中,加入催化剂,E___(填“增大”、“减小”或“不变”,下同),△H1___.
(2)As2O3分解生成As和O2的热化学方程式为___.
(3)As2O3和O2反应生成As2O5的热化学方程式为___.
(4)若1mol As2O5分解生成0.4mol As2O3和1.2mol As,则该分解过程中,需吸收的总能量为___kJ.
▼优质解答
答案和解析
(1)加入催化剂能降低反应的活化能,所以E会减小;反应热与反应物的总能量和生成物的总能量有关,加入催化剂后,反应物的总能量和生成物的总能量不变,所以反应热不变;
故答案为:减小;不变;
(2)由图象可知As2O3分解生成As和O2的反应热为+619kJ/mol,则反应的热化学方程式为:As2O3(s)=2As(s)+
O2(g)△H=+619kJ/mol;
故答案为:As2O3(s)=2As(s)+
O2(g)△H=+619kJ/mol;
(4)由图象可知As2O3生成As2O5的反应热为(-914kJ/mol+619kJ/mol)=-295kJ/mol,所以热化学方程式为As2O3(s)+O2(g)=As2O5(s)△H=-295 kJ•mol-1,
故答案为:As2O3(s)+O2(g)=As2O5(s)△H=-295 kJ•mol-1;
(4)As2O5分解生成0.4mol As2O3吸热为295 kJ•mol-1×0.4mol,As2O5分解生成1.2mol As吸热为
×914 kJ•mol-1×1.2mol,则1mol As2O5分解生成0.4mol As2O3和1.2mol As吸热为295kJ•mol-1×0.4mol+
×914 kJ•mol-1×1.2mol=666.4kJ;
故答案为:666.4.
故答案为:减小;不变;
(2)由图象可知As2O3分解生成As和O2的反应热为+619kJ/mol,则反应的热化学方程式为:As2O3(s)=2As(s)+
| 3 |
| 2 |
故答案为:As2O3(s)=2As(s)+
| 3 |
| 2 |
(4)由图象可知As2O3生成As2O5的反应热为(-914kJ/mol+619kJ/mol)=-295kJ/mol,所以热化学方程式为As2O3(s)+O2(g)=As2O5(s)△H=-295 kJ•mol-1,
故答案为:As2O3(s)+O2(g)=As2O5(s)△H=-295 kJ•mol-1;
(4)As2O5分解生成0.4mol As2O3吸热为295 kJ•mol-1×0.4mol,As2O5分解生成1.2mol As吸热为
| 1 |
| 2 |
| 1 |
| 2 |
故答案为:666.4.
看了砷的常见酸性氧化物有As2O3...的网友还看了以下:
关于Cl[2]O的一道题Cl[2]O常用NaClO[3]和Na[2]SO[3]溶液混合并加H[2] 2020-04-11 …
按要求填空.1.如按要求填空.1.如果你不认识“熨”字,应按()查字法查字典,先查到(),再查() 2020-05-16 …
一道有关平面向量的高一数学题O是平面上的坐标原点,A,B,C是平面上三点(不在一条直线上).且向量 2020-05-16 …
关于化合价的问题,O的化合价为-2,是不是也就是说在O在反应中要得到两个负电荷?和O反应的那种物质 2020-05-20 …
帮我做道几何题在O处测得北偏东30度的小岛A处有一暗礁区,为避开这一危险区,轮船在O处应改为东北方 2020-07-02 …
总体X服从N(u,sigma^2).x1.xn为样本,u已知,sigma^2未知x为样本平均值s^ 2020-08-03 …
请教一个关于无穷小计算的问题O(x3)中将x替换为x-x3/3+O(x3)对于无穷小括号的计算,用一 2020-10-31 …
NO的生物性已引起科学家的高度重视。它与超氧离子(O-2)反应,该反应的产物本题用A代号表示。A被认 2020-11-22 …
初三数学题——《新观察》(不会插图片,题目都是新观察上的)1.如图,A(4,0),B(0,4),圆O 2020-11-24 …
中考二次函数应用题例2(东阳卷)如图,足球场上守门员在O处开出一高球,球从离地面1米的A处飞出(A在 2020-11-28 …