早教吧作业答案频道 -->化学-->
卤块的主要成分是MgCl2,此外还含有Fe3+、Fe2+和Mn2+等离子.若以它为原料按如图所示工艺流程进行生产,可制得轻质氧化镁.已知1:生成氢氧化物沉淀的pH
题目详情
卤块的主要成分是MgCl2,此外还含有Fe3+、Fe2+和Mn2+等离子.若以它为原料按如图所示工艺流程进行生产,可制得轻质氧化镁.
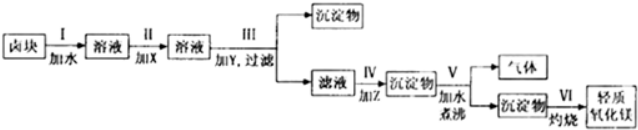
已知1:生成氢氧化物沉淀的pH
已知2:几种难容电解质的溶解度(20℃)
(已知:Fe+氢氧化物呈絮状,不易从溶液中除去)
请回答:
(1)步骤Ⅱ中加入的试剂X为漂液(含25.2%NaClO).
①用玻璃棒蘸取漂液滴在pH试纸上,pH试纸先变蓝,后褪色.说明漂液就有的性质是___.
②用化学用语表示NaClO溶液使pH试纸变蓝的原因___.
③步骤Ⅱ中漂液的主要作用是___.
④若用H2O2代替漂液,发生反应的离子方程式为___.
(2)步骤Ⅲ中加入的试剂Y为NaOH,应将溶液的pH调节为___,目的是___.
(3)步骤Ⅳ中加入的试剂Z为Na2CO3,发生反应的离子方程式为___.
(4)结合化学用语,应用化学平衡移动原理解释步骤Ⅴ中反应发生的原因___.

已知1:生成氢氧化物沉淀的pH
| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)2 | 7.6 | 9.6 |
| Fe(OH)3 | 2.7 | 3.7 |
| Mn(OH)2 | 8.3 | 9.8 |
| Mg(OH)2 | 9.6 | 11.1 |
| 物质 | 溶解度/g |
| Fe(OH)2 | 5.2×10-5 |
| Fe(OH)3 | 3×10-9 |
| MgCO3 | 3.9×10-2 |
| Mg(OH)2 | 9×10-4 |
请回答:
(1)步骤Ⅱ中加入的试剂X为漂液(含25.2%NaClO).
①用玻璃棒蘸取漂液滴在pH试纸上,pH试纸先变蓝,后褪色.说明漂液就有的性质是___.
②用化学用语表示NaClO溶液使pH试纸变蓝的原因___.
③步骤Ⅱ中漂液的主要作用是___.
④若用H2O2代替漂液,发生反应的离子方程式为___.
(2)步骤Ⅲ中加入的试剂Y为NaOH,应将溶液的pH调节为___,目的是___.
(3)步骤Ⅳ中加入的试剂Z为Na2CO3,发生反应的离子方程式为___.
(4)结合化学用语,应用化学平衡移动原理解释步骤Ⅴ中反应发生的原因___.
▼优质解答
答案和解析
为除去Fe2+,先将Fe2+氧化成Fe3+,然后加入NaOH调节pH为9.8,然后在滤液中加入纯碱将Mg2+从溶液中以MgCO3沉淀出来,然后加热煮沸可得到Mg(OH)2,灼烧后得到MgO,
(1)①漂液(含25.2%NaClO)中NaClO溶液中水解显碱性,PH变蓝色,蓝色褪去是水解生成的次氯酸具有漂白性,用玻璃棒蘸取漂液滴在pH试纸上,pH试纸先变蓝,后褪色.说明漂液就有的性质是碱性、漂白性,
故答案为:碱性、强氧化性(漂白性);
②NaClO溶液使pH试纸变蓝是次氯酸根离子水解生成次氯酸和氢氧根离子,溶液显碱性,反应的离子方程式为:ClO-+H2O⇌HClO+OH-,
故答案为:ClO-+H2O⇌HClO+OH-;
③步骤Ⅱ中漂液是强氧化剂,氧化亚铁离子为铁离子,反应的离子方程式为:2Fe2++H2O2+2H+=2Fe3++2H2O,
故答案为:2Fe2++H2O2+2H+=2Fe3++2H2O;
④过氧化氢具有氧化性,酸性溶液中能氧化亚铁离子为铁离子,反应的离子方程式为:2Fe2++H2O2+2H+=2Fe3++2H2O,
故答案为:2Fe2++H2O2+2H+=2Fe3++2H2O;
(2)骤Ⅲ中加入的试剂Y为NaOH,应将溶液的pH调节为9.8,使除Mg2+以外的各种杂质金属离子都生成氢氧化物沉淀以便通过过滤而除去,
故答案为:9.8;使除Mg2+以外的各种杂质金属离子都生成氢氧化物沉淀以便通过过滤而除去;
(3)步骤Ⅳ中加入的试剂Z为Na2CO3,加入后沉淀镁离子,发生反应的离子方程式为:Mg2++CO32-=MgCO3↓,
故答案为:Mg2++CO32-=MgCO3↓;
(4)沉淀物MgCO3存在溶解平衡MgCO3(s)⇌Mg2+(aq)+CO32-(aq),CO32-发生水解CO32-+H2O⇌HCO3-+OH-,HCO3-+H2O⇌H2CO3+OH-,在煮沸情况下促进CO32-水解生成氢氧化镁沉淀,促进CO32-彻底水解为H2CO3,分解为CO2和H2O,最后MgCO3转化为Mg(OH)2,
故答案为:沉淀物MgCO3存在溶解平衡MgCO3(s)⇌Mg2+(aq)+CO32-(aq),CO32-发生水解CO32-+H2O⇌HCO3-+OH-,HCO3-+H2O⇌H2CO3+OH-,在煮沸情况下促进CO32-水解生成氢氧化镁沉淀,促进CO32-彻底水解为H2CO3,分解为CO2和H2O,最后MgCO3转化为Mg(OH)2.
(1)①漂液(含25.2%NaClO)中NaClO溶液中水解显碱性,PH变蓝色,蓝色褪去是水解生成的次氯酸具有漂白性,用玻璃棒蘸取漂液滴在pH试纸上,pH试纸先变蓝,后褪色.说明漂液就有的性质是碱性、漂白性,
故答案为:碱性、强氧化性(漂白性);
②NaClO溶液使pH试纸变蓝是次氯酸根离子水解生成次氯酸和氢氧根离子,溶液显碱性,反应的离子方程式为:ClO-+H2O⇌HClO+OH-,
故答案为:ClO-+H2O⇌HClO+OH-;
③步骤Ⅱ中漂液是强氧化剂,氧化亚铁离子为铁离子,反应的离子方程式为:2Fe2++H2O2+2H+=2Fe3++2H2O,
故答案为:2Fe2++H2O2+2H+=2Fe3++2H2O;
④过氧化氢具有氧化性,酸性溶液中能氧化亚铁离子为铁离子,反应的离子方程式为:2Fe2++H2O2+2H+=2Fe3++2H2O,
故答案为:2Fe2++H2O2+2H+=2Fe3++2H2O;
(2)骤Ⅲ中加入的试剂Y为NaOH,应将溶液的pH调节为9.8,使除Mg2+以外的各种杂质金属离子都生成氢氧化物沉淀以便通过过滤而除去,
故答案为:9.8;使除Mg2+以外的各种杂质金属离子都生成氢氧化物沉淀以便通过过滤而除去;
(3)步骤Ⅳ中加入的试剂Z为Na2CO3,加入后沉淀镁离子,发生反应的离子方程式为:Mg2++CO32-=MgCO3↓,
故答案为:Mg2++CO32-=MgCO3↓;
(4)沉淀物MgCO3存在溶解平衡MgCO3(s)⇌Mg2+(aq)+CO32-(aq),CO32-发生水解CO32-+H2O⇌HCO3-+OH-,HCO3-+H2O⇌H2CO3+OH-,在煮沸情况下促进CO32-水解生成氢氧化镁沉淀,促进CO32-彻底水解为H2CO3,分解为CO2和H2O,最后MgCO3转化为Mg(OH)2,
故答案为:沉淀物MgCO3存在溶解平衡MgCO3(s)⇌Mg2+(aq)+CO32-(aq),CO32-发生水解CO32-+H2O⇌HCO3-+OH-,HCO3-+H2O⇌H2CO3+OH-,在煮沸情况下促进CO32-水解生成氢氧化镁沉淀,促进CO32-彻底水解为H2CO3,分解为CO2和H2O,最后MgCO3转化为Mg(OH)2.
看了 卤块的主要成分是MgCl2,...的网友还看了以下:
丰富多彩的材料为人类的生存和发展创造了完美的物质条件.(1)人类使用最早的合金是.(2)三大合成材 2020-04-10 …
有人说,只要能够促进经济的发展,是坚持生产资料公有制,还是坚持生产资料私有制,都是无所谓的。这一观 2020-05-13 …
判断一种生产关系是否先进的根本标志在于它是()[]A.生产资料公有制还是生产资料私有制B.社会化大 2020-05-13 …
我国社会主义经济制度的基础是A.生产资料公有制B.生产资料集体所有制C.生产资料混合所有制D.生产 2020-05-13 …
我国实行按劳分配的原因是()①生产力总体水平低、多层次②生产资料公有制③社会主义条件下人们劳动的性 2020-05-13 …
奴隶社会、封建社会、资本主义社会在生产关系方面的共同点是[]A.存在阶级剥削B.劳动者不占有任何生 2020-05-13 …
家庭是一个生活消费单位,消费着物质生活资料、精神生活资料和各种劳务。这说明家庭具有[]A.娱乐功能 2020-05-17 …
(2012•崇明县一模)回答下列关于微生物培养的问题.甘蔗是一种高光效的C4植物,目前已成为南方地 2020-05-17 …
花生是油料作物,种子含有大量的蛋白质和脂肪.请回答下列有关问题:(1)人们用“麻屋子,红帐子,里面 2020-06-20 …
生物-生物技术实践].生物乙醇是汽油的良好替代品,美国主要以玉米为原料生产燃料乙醇.我国则坚持“不 2020-06-26 …