早教吧作业答案频道 -->化学-->
某硫酸厂以含有SO2的尾气、氨水等为原料,合成有重要应用价值的硫化钙、硫酸钾、亚硫酸铵等物质.合成路线如下:(1)写出反应Ⅲ的化学方程式:(2)下列有关说法正确的是(填
题目详情
某硫酸厂以含有SO2的尾气、氨水等为原料,合成有重要应用价值的硫化钙、硫酸钾、亚硫酸铵等物质.合成路线如下:
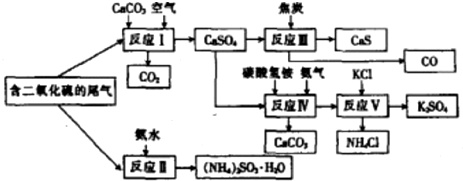
(1)写出反应Ⅲ的化学方程式:___
(2)下列有关说法正确的是___(填字母).
A反应Ⅰ中需鼓入足量空气,以保证二氧化硫充分氧化生成硫酸钙
B.反应Ⅱ和反应Ⅲ的基本反应类型相同
C.反应Ⅳ需控制在60-70℃,目的之一是减少碳酸氢铵的分解
D.反应Ⅴ中的副产物氯化铵可用作氮肥
(3)(NH4 )2SO3可用于电厂等烟道气中脱氮,将氮氧化物转化为氮气,同时生成一种氮肥,形成共生系统.写出二氧化氮与亚硫酸铵反应的化学方程式:___.
(4)很多硫酸厂为回收利用SO2,直接用氨水吸收法处理尾气.
①用15.0mL2.0mol•L-1氨水吸收标准状况下448mLSO2,吸收液中的溶质为___
②某同学用酸性KMnO4溶液滴定上述吸收液,当达到滴定终点时,消耗KMnO4溶液25.00mL,则酸性KMnO4溶液中,c(KMnO4)=___
(5)氨气用途广泛,可以直接用于燃料电池,如图是用氨水作燃料的燃料电池的工作原理.
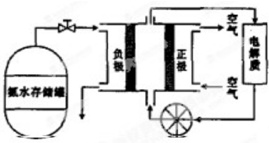
氨气燃料电池的电解质溶液最好选择___ (填“酸性”“碱性”或“中性”)溶液,氮气燃料电池的反应是氨气与氧气生成一种常见的无毒气体和水,该电池总反应的化学方程式是___,负极的电极反应式是___.

(1)写出反应Ⅲ的化学方程式:___
(2)下列有关说法正确的是___(填字母).
A反应Ⅰ中需鼓入足量空气,以保证二氧化硫充分氧化生成硫酸钙
B.反应Ⅱ和反应Ⅲ的基本反应类型相同
C.反应Ⅳ需控制在60-70℃,目的之一是减少碳酸氢铵的分解
D.反应Ⅴ中的副产物氯化铵可用作氮肥
(3)(NH4 )2SO3可用于电厂等烟道气中脱氮,将氮氧化物转化为氮气,同时生成一种氮肥,形成共生系统.写出二氧化氮与亚硫酸铵反应的化学方程式:___.
(4)很多硫酸厂为回收利用SO2,直接用氨水吸收法处理尾气.
①用15.0mL2.0mol•L-1氨水吸收标准状况下448mLSO2,吸收液中的溶质为___
②某同学用酸性KMnO4溶液滴定上述吸收液,当达到滴定终点时,消耗KMnO4溶液25.00mL,则酸性KMnO4溶液中,c(KMnO4)=___
(5)氨气用途广泛,可以直接用于燃料电池,如图是用氨水作燃料的燃料电池的工作原理.

氨气燃料电池的电解质溶液最好选择___ (填“酸性”“碱性”或“中性”)溶液,氮气燃料电池的反应是氨气与氧气生成一种常见的无毒气体和水,该电池总反应的化学方程式是___,负极的电极反应式是___.
▼优质解答
答案和解析
(1)根据题中的流程可知,反应Ⅲ是硫酸钙与焦碳高温条件下反应生成硫化钙和一氧化碳,反应方程式为CaSO4+4C
CaS+4CO↑,
故答案为:CaSO4+4C
CaS+4CO↑;
(2)A.过量的空气把亚硫酸钙氧化为硫酸钙,故A正确;
B.反应Ⅲ化学方程式为:CaSO4+4C=CaS+4CO↑,是氧化还原反应,反应Ⅱ为二氧化硫与氨水的反应,是复分解反应,所以反应类型不同,故B错误;
C.防止碳酸氢铵在温度过高时分解得不到需要的目标产物,故C正确;
D、氯化铵含N元素,是一种氮肥,故D正确;
故答案为:ACD;
(3)(NH4 )2SO3与氮氧化物生成氮气,根据电子得失守恒可知,同时生成一种氮肥应为硫酸铵,所以二氧化氮与亚硫酸铵反应的化学方程式为4(NH4 )2SO3+2NO2=N2+4(NH4 )2SO4,
故答案为:4(NH4)2SO3+2NO2=N2+4(NH4)2SO4;
(4)①氨气与二氧化硫按1:1反应生成NH4HSO3,按2:1反应生成(NH4)2SO3,15.0mL2.0mol•L-1氨水的物质的量为0.03mol,标准状况下448mLSO2,SO2的物质的量为0.02mol,它们的物质的量之比为3:2,介于1:1与2:1之间,所以吸收液中的溶质为NH4HSO3、(NH4)2SO3,
故答案为:NH4HSO3、(NH4)2SO3;
②根据电子得失守恒有关系式5SO2~2KMnO4,根据①可知SO2的物质的量为0.02mol,则KMnO4的物质的量为
×0.02mol=0.008mol,所以c(KMnO4)=
=0.32mol/L,
故答案为:0.32mol/L;
(5)氨气是碱性气体,所以电解液最好选择碱性的;生成的无毒气体时N2,据此书写化学方程式为:4NH3+3O2=2N2+6H2O,负极发生还原反应,氨气在负极反应,注意时碱性环境,所以,正极的电极反应式为:2NH3-6e-+6OH-=N2+6H2O,
故答案为:碱性;4NH3+3O2=2N2+6H2O;2NH3-6e-+6OH-=N2+6H2O.
| ||
故答案为:CaSO4+4C
| ||
(2)A.过量的空气把亚硫酸钙氧化为硫酸钙,故A正确;
B.反应Ⅲ化学方程式为:CaSO4+4C=CaS+4CO↑,是氧化还原反应,反应Ⅱ为二氧化硫与氨水的反应,是复分解反应,所以反应类型不同,故B错误;
C.防止碳酸氢铵在温度过高时分解得不到需要的目标产物,故C正确;
D、氯化铵含N元素,是一种氮肥,故D正确;
故答案为:ACD;
(3)(NH4 )2SO3与氮氧化物生成氮气,根据电子得失守恒可知,同时生成一种氮肥应为硫酸铵,所以二氧化氮与亚硫酸铵反应的化学方程式为4(NH4 )2SO3+2NO2=N2+4(NH4 )2SO4,
故答案为:4(NH4)2SO3+2NO2=N2+4(NH4)2SO4;
(4)①氨气与二氧化硫按1:1反应生成NH4HSO3,按2:1反应生成(NH4)2SO3,15.0mL2.0mol•L-1氨水的物质的量为0.03mol,标准状况下448mLSO2,SO2的物质的量为0.02mol,它们的物质的量之比为3:2,介于1:1与2:1之间,所以吸收液中的溶质为NH4HSO3、(NH4)2SO3,
故答案为:NH4HSO3、(NH4)2SO3;
②根据电子得失守恒有关系式5SO2~2KMnO4,根据①可知SO2的物质的量为0.02mol,则KMnO4的物质的量为
| 2 |
| 5 |
| 0.008mol |
| 0.025L |
故答案为:0.32mol/L;
(5)氨气是碱性气体,所以电解液最好选择碱性的;生成的无毒气体时N2,据此书写化学方程式为:4NH3+3O2=2N2+6H2O,负极发生还原反应,氨气在负极反应,注意时碱性环境,所以,正极的电极反应式为:2NH3-6e-+6OH-=N2+6H2O,
故答案为:碱性;4NH3+3O2=2N2+6H2O;2NH3-6e-+6OH-=N2+6H2O.
看了某硫酸厂以含有SO2的尾气、氨...的网友还看了以下:
已知K2O、K2O2、KO2的名称依次是氧化钾、过氧化钾、超氧化钾。那么BaO2的名称是()A.氧 2020-04-08 …
(1)高锰酸钾的相对分子质量为.(2)高锰酸钾中钾、锰、氧原子的个数比是.(3)高锰酸钾�(1)高 2020-05-12 …
防腐剂山梨酸钾的化学式为C6H7KO2,试回答:(1)山梨酸钾分子中所含的碳、氢、钾、氧各种原子的 2020-05-12 …
高锰酸钾(KMnO4)是一种紫红色的固体,受热时易分解.据此请计算:(1)高锰酸钾是由种元素组成的 2020-05-12 …
(1)高锰酸钾的相对分子质量为.(2)高锰酸钾中钾、锰、氧原子的个数比是.(3)高锰酸钾中钾、锰、 2020-05-14 …
如图是实验室制取气体的常用装置.(1)仪器①的名称是.(2)用文字式(或化学符号)表示用高锰酸钾制 2020-05-14 …
某实验小组的同学把用氯酸钾制氧气时,误将高锰酸钾当作二氧化锰放入氯酸钾固体中,发现加热后反应的速度 2020-06-18 …
将石墨置于熔融的钾或气态钾中,石墨会吸收钾而形成称为钾石墨的物质,其组成是C8K、C24K、C36 2020-07-03 …
实验室常用高锰酸钾来制取氧气.(1)高锰酸钾是一种色固体.(2)高锰酸钾的相对分子质量是.(3)高锰 2020-11-01 …
(1)将石墨置于熔融的钾或气态钾中,石墨会吸收钾而形成称为钾石墨的物质,其组成是C8K、C24K、C 2020-11-05 …