早教吧作业答案频道 -->化学-->
某实验小组用如图1所示装置对SO2与BaCl2溶液和Ba(NO3)2溶液反应进行探究(夹持装置和A中加热装置已略,气密性已检验).(1)B装置的作用是.(2)实验过程中C、D均出现白色沉淀.实
题目详情
某实验小组用如图1所示装置对SO2与BaCl2溶液和Ba(NO3)2溶液反应进行探究 (夹持装置和A中加热装置已略,气密性已检验).
(1)B装置的作用是___.
(2)实验过程中C、D均出现白色沉淀.实验结束后分别向C、D中加入足量稀盐酸,白色沉淀均不溶解.C、D试管中的白色沉淀的化学式是___.
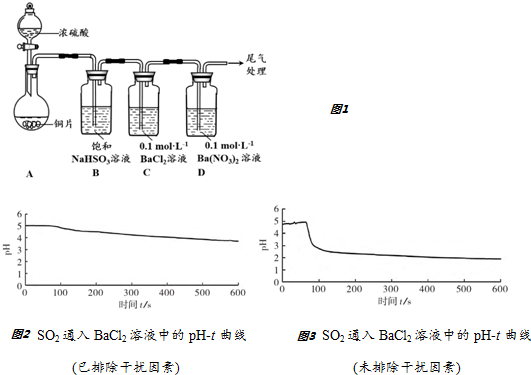
(3)小组同学进一步探究C中出现白色沉淀的原因,获得的实验数据如图2、3所示.
请结合化学用语分别解释图1、2中pH下降的原因.
图2中pH下降的原因:___.
图3中pH下降的原因:___.
(4)依据以上实验获得的结论,小组同学进一步推断D中产生白色沉淀的原因可能是___或___,可以证明其推断的实验方案是___.
(5)小组同学又进一步设计了如下实验方案:通过相应的实验手段监测并获得SO2通入Ba(NO3)2溶液后,产生白色沉淀过程中NO3-浓度随时间变化情况的曲线.小组同学设计此实验方案想进一步探究的实验问题可能是___.

(1)B装置的作用是___.
(2)实验过程中C、D均出现白色沉淀.实验结束后分别向C、D中加入足量稀盐酸,白色沉淀均不溶解.C、D试管中的白色沉淀的化学式是___.
(3)小组同学进一步探究C中出现白色沉淀的原因,获得的实验数据如图2、3所示.
请结合化学用语分别解释图1、2中pH下降的原因.
图2中pH下降的原因:___.
图3中pH下降的原因:___.
(4)依据以上实验获得的结论,小组同学进一步推断D中产生白色沉淀的原因可能是___或___,可以证明其推断的实验方案是___.
(5)小组同学又进一步设计了如下实验方案:通过相应的实验手段监测并获得SO2通入Ba(NO3)2溶液后,产生白色沉淀过程中NO3-浓度随时间变化情况的曲线.小组同学设计此实验方案想进一步探究的实验问题可能是___.
▼优质解答
答案和解析
(1)装置A:加热条件下,Cu和浓硫酸反应生成硫酸铜、二氧化硫和水;浓硫酸的沸点为338℃,加热时酒精灯火焰的温度为400℃~500℃”,说明浓硫酸在温度较高时也能挥发出H2SO4蒸气,C、D中有可能是挥发出的H2SO4提供的SO42-与Ba2+反应生成BaSO4:SO42-+Ba2+═BaSO4↓,需排除,所以用饱和的亚硫酸氢钠溶液吸收吸收装置A中产生的H2SO4酸雾,
故答案为:吸收装置A中产生的H2SO4酸雾;
(2)由白色沉淀,发现均不溶于稀盐酸,白色沉淀为硫酸钡,装置C:可能是溶液中溶解的氧气与SO2作用产生了硫酸,进而得到BaSO4:2Ba2++2SO2+O2+2H2O═2BaSO4↓+4H+,
装置D:可能是硝酸根离子具有氧化性,NO3-氧化了SO2,生成硫酸钡沉淀,3SO2+2NO3-+3Ba2++2H2O=3BaSO4↓+2NO↑+4H+,
故答案为:BaSO4;
(3)图2中pH下降曲线比较平缓,可能为二氧化硫和水反应生成亚硫酸,亚硫酸电离导致PH下降,反应方程式为:SO2+H2O⇌H2SO3⇌H++HSO3-;图3中PH下降曲线属于斜率较大的情况,可能为弱酸亚硫酸被氧化成强酸硫酸所致,反应方程式为:2SO2+2H2O+O2═2SO42-+4H+,
故答案为:SO2+H2O⇌H2SO3⇌H++HSO3-;2SO2+2H2O+O2═2SO42-+4H+;
(4)酸性条件下,SO2被O2氧化成+6价的硫,在溶液中硫酸根离子和钡离子形成沉淀,也可能为SO2被NO3-氧化生成SO42-,为排除氧气的干扰,可在排除O2干扰前提下,向盛有等体积0.1 mol•L-1Ba(NO3)2溶液的洗气瓶D中通入SO2,若出现白色沉淀,则证明酸性条件下NO3-氧化了SO2,反之则说明原D洗气瓶中沉淀的出现是O2氧化SO2所致,
故答案为:酸性条件下,SO2被O2氧化;被NO3-氧化生成SO42-;在排除O2干扰前提下,向盛有等体积0.1 mol•L-1Ba(NO3)2溶液的洗气瓶D中通入SO2,若出现白色沉淀,则证明酸性条件下NO3-氧化了SO2,反之则说明原D洗气瓶中沉淀的出现是O2氧化SO2所致;
(5)不同的氧化剂对同一还原剂氧化能力不同,小组同学设计此实验方案想进一步探究可能为若NO3-和O2均参与反应,则相同条件下二者氧化SO2的能力或反应速率的差异等,
故答案为:若NO3-和O2均参与反应,则相同条件下二者氧化SO2的能力或反应速率的差异等.
故答案为:吸收装置A中产生的H2SO4酸雾;
(2)由白色沉淀,发现均不溶于稀盐酸,白色沉淀为硫酸钡,装置C:可能是溶液中溶解的氧气与SO2作用产生了硫酸,进而得到BaSO4:2Ba2++2SO2+O2+2H2O═2BaSO4↓+4H+,
装置D:可能是硝酸根离子具有氧化性,NO3-氧化了SO2,生成硫酸钡沉淀,3SO2+2NO3-+3Ba2++2H2O=3BaSO4↓+2NO↑+4H+,
故答案为:BaSO4;
(3)图2中pH下降曲线比较平缓,可能为二氧化硫和水反应生成亚硫酸,亚硫酸电离导致PH下降,反应方程式为:SO2+H2O⇌H2SO3⇌H++HSO3-;图3中PH下降曲线属于斜率较大的情况,可能为弱酸亚硫酸被氧化成强酸硫酸所致,反应方程式为:2SO2+2H2O+O2═2SO42-+4H+,
故答案为:SO2+H2O⇌H2SO3⇌H++HSO3-;2SO2+2H2O+O2═2SO42-+4H+;
(4)酸性条件下,SO2被O2氧化成+6价的硫,在溶液中硫酸根离子和钡离子形成沉淀,也可能为SO2被NO3-氧化生成SO42-,为排除氧气的干扰,可在排除O2干扰前提下,向盛有等体积0.1 mol•L-1Ba(NO3)2溶液的洗气瓶D中通入SO2,若出现白色沉淀,则证明酸性条件下NO3-氧化了SO2,反之则说明原D洗气瓶中沉淀的出现是O2氧化SO2所致,
故答案为:酸性条件下,SO2被O2氧化;被NO3-氧化生成SO42-;在排除O2干扰前提下,向盛有等体积0.1 mol•L-1Ba(NO3)2溶液的洗气瓶D中通入SO2,若出现白色沉淀,则证明酸性条件下NO3-氧化了SO2,反之则说明原D洗气瓶中沉淀的出现是O2氧化SO2所致;
(5)不同的氧化剂对同一还原剂氧化能力不同,小组同学设计此实验方案想进一步探究可能为若NO3-和O2均参与反应,则相同条件下二者氧化SO2的能力或反应速率的差异等,
故答案为:若NO3-和O2均参与反应,则相同条件下二者氧化SO2的能力或反应速率的差异等.
看了某实验小组用如图1所示装置对S...的网友还看了以下:
某研究性学习小组设计了一组实验来探究元素周期律.甲同学设计了如图1装置来一次性完成验证非金属性S> 2020-06-10 …
某研究性学习小组为了探究合成氨的原理,设计了下列实验装置。下图中A是简易的氢气发生器,B是圆底烧瓶 2020-07-21 …
如图为探究酵母菌呼吸作用的实验装置,以下说法不正确的是()A.装置A中加NaOH的目的是吸收空气中 2020-07-25 …
有如图所示的探究性实验装置共6个,6个装置中分别加入葡萄糖饱和溶液和两个凝胶珠,实验开始时,小液滴都 2020-10-29 …
下列对应生理现象描述正确的是()A.甲装置可以用来探究植物的蒸腾作用B.乙装置可以用来验证植物的光合 2020-11-03 …
某化学兴趣小组设计如下实验方案.将浓硫酸与铜片反应制备SO2并进行相关实验探究,实验装置如图所示:请 2020-11-28 …
某兴趣小组设计了如图所示装置(部分夹持装置已略去)进行实验探究.实验一探究影响化学反应速率的因素.圆 2020-12-19 …
如图是研究植物散失水分的四个实验装置,将A、B、C、D实验装置在阳光下照射2小时.请分析回答:(1) 2020-12-25 …
如图是研究植物散失水分的四个实验装置,将A、B、C、D实验装置在阳光下照射2小时.请分析回答:(4分 2020-12-25 …
某化学探究小组为探究能与碳反应的浓硫酸的最低浓度,设计了如图实验装置进行实验.请回答下列问题:(1) 2021-01-22 …