早教吧作业答案频道 -->化学-->
某化学兴趣小组设计如下实验方案.将浓硫酸与铜片反应制备SO2并进行相关实验探究,实验装置如图所示:请回答下列问题:(1)装置B的作用是(2)设计装置C的目的是验证SO2的性,装
题目详情
某化学兴趣小组设计如下实验方案.将浓硫酸与铜片反应制备SO2并进行相关实验探究,实验装置如图所示:
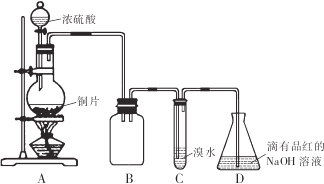
请回答下列问题:
(1)装置B的作用是___
(2)设计装置C的目的是验证SO2的___性,装置C中发生反应的离子方程式是___.装置D中NaOH全部转化为NaHSO3的标志是___.
(3)向NaHSO3溶液中加入NaCl0溶液时,反应有三种可能的情况:
I.HSO3-与ClO-恰好反应
Ⅱ.NaClO不足
Ⅲ.NaClO过量
甲同学分别取上述混合溶液于试管中,通过下列实验确定该反应属于哪一种情况,请完成下表:(已知酸性:H2SO3>H2CO3>HCl0)
(4)请设计简单实验证明:室温下HS03-的电离平衡常数Ka与水解平衡常数Kb,的相对大小:___.

请回答下列问题:
(1)装置B的作用是___
(2)设计装置C的目的是验证SO2的___性,装置C中发生反应的离子方程式是___.装置D中NaOH全部转化为NaHSO3的标志是___.
(3)向NaHSO3溶液中加入NaCl0溶液时,反应有三种可能的情况:
I.HSO3-与ClO-恰好反应
Ⅱ.NaClO不足
Ⅲ.NaClO过量
甲同学分别取上述混合溶液于试管中,通过下列实验确定该反应属于哪一种情况,请完成下表:(已知酸性:H2SO3>H2CO3>HCl0)
| 序号 | 实 验操作 | 现 象 | 结 论 |
| ① | 加几小块CaCO3固体 | 有气泡产生 | I或Ⅱ |
| ② | 滴加少量淀粉KI溶液,振荡 | Ⅲ | |
| ③ | 滴加少量溴水,振荡 | Ⅱ | |
| ④ | 滴加少量酸性KMn04溶液、振荡 | 溶液为紫色 |
▼优质解答
答案和解析
由图可知,A中发生Cu与浓硫酸的反应生成二氧化硫,B作安全瓶,可防止倒吸,C中发生SO2+Br2+2H2O=H2SO4+2HBr,D中NaOH溶液吸收尾气,
(1)装置B的作用是防倒吸(或安全瓶),故答案为:防倒吸(或安全瓶);
(2)C中发生的反应中S元素的化合价升高,则设计装置C的目的是验证SO2的还原性,装置C中发生反应的离子方程式是SO2+Br2+2H2O=4H++SO42-+2Br-.装置D中NaOH全部转化为NaHSO3时碱性降低,装置D中NaOH全部转化为NaHSO3的标志是溶液由红色变为无色,
故答案为:还原;SO2+Br2+2H2O=4H++SO42-+2Br-;溶液由红色变为无色;
(3)②NaClO可氧化KI,则观察到溶液变为蓝色;
③溴水可氧化HSO3-,则观察到溴水褪色,
④HSO3-与高锰酸钾可发生氧化还原反应,由溶液为紫色可知,不存在HSO3-,则I或Ⅲ成立,
故答案为:
;
(4)电离显酸性,水解显碱性,则测定pH即可,则设计实验为常温下,用pH试纸(或pH计)测定NaHS03溶液的pH,若pH<7,则Ka>Kb,若pH>7,则Ka故答案为:常温下,用pH试纸(或pH计)测定NaHS03溶液的pH,若pH<7,则Ka>Kb,若pH>7,则Ka
(1)装置B的作用是防倒吸(或安全瓶),故答案为:防倒吸(或安全瓶);
(2)C中发生的反应中S元素的化合价升高,则设计装置C的目的是验证SO2的还原性,装置C中发生反应的离子方程式是SO2+Br2+2H2O=4H++SO42-+2Br-.装置D中NaOH全部转化为NaHSO3时碱性降低,装置D中NaOH全部转化为NaHSO3的标志是溶液由红色变为无色,
故答案为:还原;SO2+Br2+2H2O=4H++SO42-+2Br-;溶液由红色变为无色;
(3)②NaClO可氧化KI,则观察到溶液变为蓝色;
③溴水可氧化HSO3-,则观察到溴水褪色,
④HSO3-与高锰酸钾可发生氧化还原反应,由溶液为紫色可知,不存在HSO3-,则I或Ⅲ成立,
故答案为:
| 序号 | 实 验操作 | 现 象 | 结 论 |
| ① | 加几小块CaCO3固体 | 有气泡产生 | I或Ⅱ |
| ② | 滴加少量淀粉KI溶液,振荡 | 溶液变为蓝色 | Ⅲ |
| ③ | 滴加少量溴水,振荡 | 溴水褪色 | Ⅱ |
| ④ | 滴加少量酸性KMn04溶液、振荡 | 溶液为紫色 | I或Ⅲ |
(4)电离显酸性,水解显碱性,则测定pH即可,则设计实验为常温下,用pH试纸(或pH计)测定NaHS03溶液的pH,若pH<7,则Ka>Kb,若pH>7,则Ka
看了某化学兴趣小组设计如下实验方案...的网友还看了以下:
相似图像都一样吗比如三角形的相似图形就是三角形那么是不是可以这么两个相似图形的名称是一样的就是相似图 2020-03-31 …
求救如图,点A在反比例函数y=4/x的图像上,点B在反比例函数y=k/x(k<0)的图像上,且∠A 2020-04-08 …
9.图7-1-2-4是蝴蝶发育过程的相关图解,下列说法正确的是()A.蝴蝶是不完全变态发育的昆虫B 2020-04-11 …
古汉语词典在线《小石潭记》中的“似与游者相乐”中的“相”是什么意思/ 2020-05-13 …
凡是能提供某种形式能量的物质,或是物质的各种各样运动,统称为能源.下面是一组关于能源的问题,请完成 2020-05-16 …
如图是有关黄瓜绿叶组织的相关图解,其中图1是叶肉细胞的光合作用过程图解;图2表示种植黄瓜的密闭大棚 2020-05-17 …
语文题:刮目相看的相是什么意思 2020-05-17 …
“弹冠相庆”的“相”是什么意思A互相BC是其他的答案,请写下来, 2020-05-23 …
金属学.能出现枝晶偏析的相是不是都是二元或多元相.或者说单相就不会出现枝晶偏析现象看课件上说,匀晶 2020-05-24 …
在交流电路的相量图中,必须按逆时针旋转的方向来观察各有关量的相位关系。 () 2020-05-29 …