早教吧作业答案频道 -->化学-->
铝土矿是工业炼铝的主要原料,某铝土矿样品组成如下:主要成分:Al2O3杂质:Fe2O3、SiO2及其他不溶且不参与化学反应的物质为测定该样品中Al的含量,某化学兴趣小组设计了如下两个方案:
题目详情
铝土矿是工业炼铝的主要原料,某铝土矿样品组成如下:
主要成分:Al2O3杂质:Fe2O3、SiO2及其他不溶且不参与化学反应的物质为测定该样品中Al的含量,某化学兴趣小组设计了如下两个方案:
【查阅资料】各相关离子开始沉淀和沉淀完全时溶液的pH如表:
方案一:将铝土矿加足量盐酸溶解,再调节pH,使Fe3+沉淀完全而Al3+不沉淀.需调节pH范围应是___,若想得到氯化铝固体需将其溶液通入___直至蒸干.
方案二:
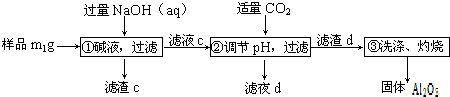
(1)②反应的离子方程式为___.CO2不可过量的原因是___.
(2)若在步骤②中加入乙酸乙酯调节pH,加热也可得到d的沉淀,写出生成d沉淀的化学方程式___.
主要成分:Al2O3杂质:Fe2O3、SiO2及其他不溶且不参与化学反应的物质为测定该样品中Al的含量,某化学兴趣小组设计了如下两个方案:
【查阅资料】各相关离子开始沉淀和沉淀完全时溶液的pH如表:
| Al3+ | Fe3+ | AlO2- | SiO32- | |
| 开始沉淀时 | 3.4 | 1.9 | 10.6 | 7.3 |
| 沉淀完全时 | 4.7 | 3.2 | 9.3 | 5.3 |
方案二:

(1)②反应的离子方程式为___.CO2不可过量的原因是___.
(2)若在步骤②中加入乙酸乙酯调节pH,加热也可得到d的沉淀,写出生成d沉淀的化学方程式___.
▼优质解答
答案和解析
方案一:将铝土矿加足量盐酸溶解,再调节pH,使Fe3+沉淀完全而Al3+不沉淀,分析图表中数据选择铁离子沉淀完全,铝离子不沉淀的PH为3.2~3.4,氯化铝溶液水解生成氢氧化铝和盐酸,若想得到氯化铝固体需将其溶液通入氯...
看了铝土矿是工业炼铝的主要原料,某...的网友还看了以下:
三聚氰酸[C3N3(OH)3]可用于消除汽车尾气中的NO2.其反应原理为:①C3N3(OH)3△. 2020-05-14 …
运用化学反应原理研究物质的性质具有重要意义.请回答下列问题:(1)氨气可以构成燃料电池,其电池反应 2020-05-15 …
C0高温还原MgSO4可用于制备Mg0,反应生成的气体产物有CO2、SO2、SO3.为探究反应原理 2020-07-24 …
2-氯乙醇是一种重要的有机化工原料,受热时易分解.通常是以适量的2-氯乙醇为溶剂,用氯化氢与环氧乙 2020-07-26 …
化学反应原理在科研和生产中有广泛应用。(1)利用“化学蒸气转移法”提纯金属钨的反应原理为W(s)+I 2020-11-01 …
某研究性学习小组通过下列反应原理制备SO2并进行性质探究.反应原理为:Na2SO3(固)+H2SO4 2020-11-28 …
工业上常用电解饱和食盐水的方法制取烧碱,其反应原理为:2NaCl+2H2O2NaOH+H2↑+Cl2 2020-12-01 …
工业上以黄铁矿(主要成分FeS2,杂质不含硫元素)为原料生产硫酸.其反应原理为:①FeS2与O2高温 2020-12-02 …
HCNO可用于消除汽车尾气中的NO和NO2,其反应原理为:HCNO+NOx→N2+CO2+H2O,下 2020-12-21 …
在化学分析中,为了测定某试样中FeSO4·7H2O的质量分数,一般采用在酸性条件下用高锰酸钾标准溶液 2021-01-22 …