早教吧作业答案频道 -->化学-->
将海水淡化与浓海水资源结合起来是综合利用海水的重要途径.(1)先把浓海水中溴离子氧化成Br2,再利用“空气吹出法”从浓海水中吹出Br2,用纯碱来吸收,Br2又变成化合态溴,这样做的
题目详情
将海水淡化与浓海水资源结合起来是综合利用海水的重要途径.
(1)先把浓海水中溴离子氧化成Br2,再利用“空气吹出法”从浓海水中吹出Br2,用纯碱来吸收,Br2又变成化合态溴,这样做的目的是___.利用纯碱吸收溴单质的主要反应式是:Br2+Na2CO3+H2O→NaBr+NaBrO3+NaHCO3则纯碱吸收了6molBr2时,转移的电子为___mol
(2)从浓海水中生产镁单质的一段工艺流程如图:
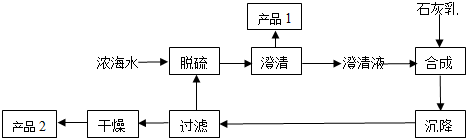
又知浓海水的主要成分如下表:
①该工艺过程中,产品1中一定含有的离子是___,产品2的化学式为___.
②1m3浓海水最多可得产品2的质量为___ kg.
(3)工业生产镁单质的化学方程式为___.
(4)从海水中提取出的氯化钠可用于氯碱工业,则氯碱工业主要反应原理的离子方程式为___.
(1)先把浓海水中溴离子氧化成Br2,再利用“空气吹出法”从浓海水中吹出Br2,用纯碱来吸收,Br2又变成化合态溴,这样做的目的是___.利用纯碱吸收溴单质的主要反应式是:Br2+Na2CO3+H2O→NaBr+NaBrO3+NaHCO3则纯碱吸收了6molBr2时,转移的电子为___mol
(2)从浓海水中生产镁单质的一段工艺流程如图:

又知浓海水的主要成分如下表:
| 离子 | Na+ | Mg2+ | Cl- | SO42- |
| 浓度/(g/L) | 63.7 | 28.8 | 144.6 | 46.4 |
②1m3浓海水最多可得产品2的质量为___ kg.
(3)工业生产镁单质的化学方程式为___.
(4)从海水中提取出的氯化钠可用于氯碱工业,则氯碱工业主要反应原理的离子方程式为___.
▼优质解答
答案和解析
(1)吹出Br2,用SO2吸收,发生氧化还原反应生成硫酸和HBr,其目的是使Br2富集;Br2+Na2CO3+H2O→NaBr+NaBrO3+NaHCO3中Br由0降低为-1,由0升高为+5价,可知吸收3mol溴转移5mol电子,则吸收6mol Br2时,转移的电子为6...
看了将海水淡化与浓海水资源结合起来...的网友还看了以下:
一个重要的量子力学问题如果当x0,势函数为V(x)=mgx.则当x0时,解为Airy函数,也有相应 2020-05-13 …
胶片或照相纸的感光乳剂中使用的银盐种类()。A.主要是溴化银B.主要是溴化银、氯化银、氟化银C.溴化 2020-05-31 …
中国现在比唐朝来说综合来说怎么样?综合来说就各方面来说,你认为中国是否会比唐朝时强大,请列举实例理 2020-06-11 …
下列叙述中错误的是()A.煤是工业上获得苯、甲苯、二甲苯等芳香烃的重要来源物质B.海水提溴、海带提 2020-06-27 …
一个有机物有一个苯环,一个碳碳双键,一个醛基,若要检测其中的碳碳双键为什么要用溴的四氯化碳溶液而不 2020-07-20 …
溴及其化合物在生活和生产中都有重要应用,自然界中的溴绝大多数都分布在海洋中,从海水中提取溴是溴的最 2020-07-24 …
为什么苯和溴反应必须在无水的前提下催化剂一定要是溴化铁的为嘛 2020-07-24 …
卤族元素在自然界中都以典型的盐类存在,包括氟、氯、溴、碘和砹五种元素,位于元素周期表的第ⅦA族,其 2020-07-29 …
下列说法不正确的是()A.直馏汽油能使溴水因化学反应而褪色B.常温下,含碳量最高的气态烃是乙炔C.石 2020-11-16 …
GDP即国内生产总值,是目前各个国家和地区用来衡量该国或地区的经济发展综合水平通用的指标。它是一个国 2020-12-01 …