早教吧作业答案频道 -->化学-->
研究碳及其化合物的利用对促进低碳社会的构建具有重要的意义.某学习小组查阅资料并进行相关探究,请帮忙完成以下探究.I、碳单质能够参与反应制备重要材料半导体,其化学反应方程
题目详情
研究碳及其化合物的利用对促进低碳社会的构建具有重要的意义.某学习小组查阅资料并进行相关探究,请帮忙完成以下探究.
I、碳单质能够参与反应制备重要材料半导体,其化学反应方程式为:___
II、碳氢化合物是重要的能源物质.丙烷脱氢可得丙烯.
(1)已知:C3H8(g)→CH4(g)+HC≡CH(g)+H2(g)
△H1=156.6kJ•mol-1
CH3CH═CH2(g)→CH4(g)+HC≡CH(g )△H2=32.4kJ•mol-1
则相同条件下,由气态C3H8生成丙烯和氢气的热化学方程式为:___
(2)以甲烷为燃料制作新型燃料电池,电池的正极通入O2,负极通入甲烷,电解质是氢氧化钾溶液.电池负极反应式为___;
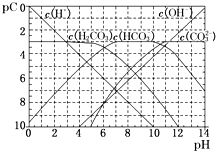
Ⅲ、pC类似于pH,是指极稀溶液中的溶质浓度的常用对数的负值.如某溶液中某溶质的浓度为1×10-3 mol/L,则该溶液中该溶质的pC=-lg(1×10-3)=3.如图为25℃时H2CO3溶液的pC-pH图.请回答下列问题:(若离子浓度小于10-5mol/L,可认为该离子不存在)
①在同一溶液中,H2CO3、HCO3-、CO32-___(填“能”或“不能”)大量共存.
②H2CO3一级电离平衡常数的数值Ka1≈___.
③人体血液里主要通过碳酸氢盐缓冲体系(H2CO3/HCO3-)可以抵消少量酸或碱,维持pH≈7.4.当过量的酸进入血液中时,血液缓冲体系中的
最终将___.
A.变大 B.变小 C.基本不变 D.无法判断.
I、碳单质能够参与反应制备重要材料半导体,其化学反应方程式为:___
II、碳氢化合物是重要的能源物质.丙烷脱氢可得丙烯.

(1)已知:C3H8(g)→CH4(g)+HC≡CH(g)+H2(g)
△H1=156.6kJ•mol-1
CH3CH═CH2(g)→CH4(g)+HC≡CH(g )△H2=32.4kJ•mol-1
则相同条件下,由气态C3H8生成丙烯和氢气的热化学方程式为:___
(2)以甲烷为燃料制作新型燃料电池,电池的正极通入O2,负极通入甲烷,电解质是氢氧化钾溶液.电池负极反应式为___;
Ⅲ、pC类似于pH,是指极稀溶液中的溶质浓度的常用对数的负值.如某溶液中某溶质的浓度为1×10-3 mol/L,则该溶液中该溶质的pC=-lg(1×10-3)=3.如图为25℃时H2CO3溶液的pC-pH图.请回答下列问题:(若离子浓度小于10-5mol/L,可认为该离子不存在)
①在同一溶液中,H2CO3、HCO3-、CO32-___(填“能”或“不能”)大量共存.
②H2CO3一级电离平衡常数的数值Ka1≈___.
③人体血液里主要通过碳酸氢盐缓冲体系(H2CO3/HCO3-)可以抵消少量酸或碱,维持pH≈7.4.当过量的酸进入血液中时,血液缓冲体系中的
| c(H+) |
| c(H2CO3) |
A.变大 B.变小 C.基本不变 D.无法判断.
▼优质解答
答案和解析
Ⅰ.碳单质能够参与反应制备重要材料半导体诶硅,反应的化学方程式为:SiO2+2C
Si+2CO↑,故答案为:SiO2+2C
Si+2CO↑;
Ⅱ.(1)①C3H8(g)=CH4(g)+HC≡CH(g)+H2(g)△H1=+156.6kJ•mol-1
②CH3CH=CH2(g)=CH4(g)+HC≡CH(g )△H2=+32.4kJ•mol-1
依据盖斯定律①-②得到热化学方程式为:C3H8(g)=CH3CH=CH2(g)+H2(g)△H=+124.2 kJ•mol-1 ;
故答案为:C3H8(g)=CH3CH=CH2(g)+H2(g)△H=+124.2 kJ•mol-1 ;
(2)甲烷燃料电池中,负极上甲烷失电子和氢氧根离子反应生成碳酸根离子和水,电极反应式为:CH4-8e-+10OH-=CO32-+7H2O,
故答案为:CH4-8e-+10OH-=CO32-+7H2O;
Ⅲ.①碳酸存在的溶液中酸性较强、碳酸根离子存在的溶液中碱性较强,所以碳酸根离子和碳酸不能大量共存,故答案为:不能;
②由图象可知当pH=6时,pC(H2CO3)=pC(HCO3-),结合Ka1(H2CO3)=
=
=10-6,故答案为:10-6;
③氢离子浓度增大,平衡向左移动放出CO2,碳酸浓度基本不变,则c(H+)/c(H2CO3)最终将变大,故选A,故答案为:A;
| ||
| ||
Ⅱ.(1)①C3H8(g)=CH4(g)+HC≡CH(g)+H2(g)△H1=+156.6kJ•mol-1
②CH3CH=CH2(g)=CH4(g)+HC≡CH(g )△H2=+32.4kJ•mol-1
依据盖斯定律①-②得到热化学方程式为:C3H8(g)=CH3CH=CH2(g)+H2(g)△H=+124.2 kJ•mol-1 ;
故答案为:C3H8(g)=CH3CH=CH2(g)+H2(g)△H=+124.2 kJ•mol-1 ;
(2)甲烷燃料电池中,负极上甲烷失电子和氢氧根离子反应生成碳酸根离子和水,电极反应式为:CH4-8e-+10OH-=CO32-+7H2O,
故答案为:CH4-8e-+10OH-=CO32-+7H2O;
Ⅲ.①碳酸存在的溶液中酸性较强、碳酸根离子存在的溶液中碱性较强,所以碳酸根离子和碳酸不能大量共存,故答案为:不能;
②由图象可知当pH=6时,pC(H2CO3)=pC(HCO3-),结合Ka1(H2CO3)=
| c(H+)c(HCO3-) |
| c(H2CO3) |
| 10-6c(HCO3-) |
| c(H2CO3) |
③氢离子浓度增大,平衡向左移动放出CO2,碳酸浓度基本不变,则c(H+)/c(H2CO3)最终将变大,故选A,故答案为:A;
看了研究碳及其化合物的利用对促进低...的网友还看了以下:
提问一个逻辑学上的菜鸟问题这里有一个例子,“参加会议的都不是企业家”和“参加会议的不都是企业家”这 2020-04-27 …
科学家发现在月球上含有丰富的23He(氦3),它是一种高效、清洁、安全的核聚变燃料,其参与的一种核 2020-06-11 …
下列关于膝反射的叙述,错误的是()A.反射活动由一定的刺激引起B.反射活动的发生需要反射弧结构完整 2020-06-28 …
关于转化率的一个小问题,对于多物质参与的反应,增加某一物质的量,则该物质的转化率降低,其他反应物的 2020-07-07 …
科学家发现在月球上含有丰富的(氦3),它是一种高效、清洁、安全的核聚变燃料,其参与的一种核聚变反应 2020-07-29 …
科学家发现在月球上含有丰富的32He(氦3)它是一种高效、清洁、安全的核聚变燃料,其参与的一种核聚 2020-07-29 …
关于参数方程的问题1.x=e^t+e^(-t)y=2(e^t-e^(-t))e=2.71828(t 2020-08-02 …
中科大研究人员通过构成二维RhW纳米片实现高效CO2催化剂氢生成甲醇,其反应微观示意图如下,下列关于 2021-01-01 …
化学的几道不同类型的例题求化学的几道不同类型有关化学方程式的计算的例题,包括:1含杂质(不参与反应) 2021-01-21 …
化学的几道不同类型的例题求化学的几道不同类型有关化学方程式的计算的例题,包括:1含杂质(不参与反应) 2021-01-21 …