早教吧作业答案频道 -->化学-->
某化学兴趣小组为了研究外界条件对化学反应速率的影响,进行了如下实验:实验原理2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+10CO2↑+8H2O实验内容及记录实验编号室温下,试管中所加试
题目详情
某化学兴趣小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
【实验原理】2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+10CO2↑+8H2O
【实验内容及记录】
请回答:
(1)根据上表中的实验数据,可以得到的结论是___.
(2)利用实验1数据计算,用KMnO4的浓度变化表示反应速率 (KMnO4)=___.
(3)该小组同学根据经验绘制了 (Mn2+) 随时间变化趋势的示意图,如图甲所示.但有同学查阅已有的实验资料发现,该实验过程中 (Mn2+) 随时间变化的趋势应如图乙所示. 该小组同学根据图乙所示信息提出了新的假设,并继续进行实验探究.
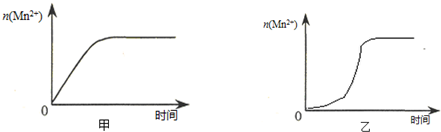
①该小组同学提出的假设是___.
②请你帮助该小组同学完成实验方案,并选择表中空白处应加入的物质.
A.KMnO4 B.H2C2O4 C.K2SO4 D.MnSO4
③若该小组同学提出的假设成立,应观察到的现象是___.
【实验原理】2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+10CO2↑+8H2O
【实验内容及记录】
| 实验编号 | 室温下,试管中所加试剂及其用量/mL | 室温下溶液颜色褪至无色所需时间/min | |||
| 0.6 mol/L H2C2O4溶液 | H2O | 0.2 mol/L KMnO4溶液 | 3 mol/L 稀硫酸 | ||
| 1 | 3.0 | 2.0 | 3.0 | 2.0 | 4.0 |
| 2 | 3.0 | 3.0 | 2.0 | 2.0 | 5.2 |
| 3 | 3.0 | 4.0 | 1.0 | 2.0 | 6.4 |
(1)根据上表中的实验数据,可以得到的结论是___.
(2)利用实验1数据计算,用KMnO4的浓度变化表示反应速率 (KMnO4)=___.
(3)该小组同学根据经验绘制了 (Mn2+) 随时间变化趋势的示意图,如图甲所示.但有同学查阅已有的实验资料发现,该实验过程中 (Mn2+) 随时间变化的趋势应如图乙所示. 该小组同学根据图乙所示信息提出了新的假设,并继续进行实验探究.

①该小组同学提出的假设是___.
②请你帮助该小组同学完成实验方案,并选择表中空白处应加入的物质.
| 实验编号 | 室温下,试管中所加试剂及其用量/mL | 再向试管中加入少量固体 | 室温下溶液颜色褪至无色所需时间/min | |||
| 0.6 mol/L H2C2O4溶液 | H2O | 0.2 mol/L KMnO4溶液 | 3 mol/L 稀硫酸 | |||
| 4 | 3.0 | 2.0 | 3.0 | 2.0 | ||
③若该小组同学提出的假设成立,应观察到的现象是___.
▼优质解答
答案和解析
(1)从表中数据,可知改变的条件是KMnO4浓度,其他条件相同时,增大KMnO4浓度,褪色时间变短,则反应速率增大,
故答案为:其他条件相同时,增大KMnO4浓度(或反应物浓度),反应速率增大;
(2)草酸的物质的量为:0.6mol•L-1×0.003L=0.0018mol,高锰酸钾的物质的量为:0.2mol•L-1×0.003L=0.0006mol,草酸和高锰酸钾的物质的量之比为:0.0018mol:0.0006mol=3:1,显然草酸过量,高锰酸钾完全反应,混合后溶液中高锰酸钾的浓度为:
=0.06mol/L,
这段时间内平均反应速率v(KMnO4)=
=1.5×10-2 mol/(L•min),
故答案为:1.5×10-2mol•L-1•min-1或0.015 mol•L-1•min-1;
(3)①由图乙可知,反应开始后速率增大的比较快,说明生成物中的MnSO4(或Mn2+)为该反应的催化剂,
故答案为:生成物中的MnSO4为该反应的催化剂(或Mn2+对该反应有催化作用);
②与实验1作对比实验,则加入的硫酸锰的量不同,其它条件必须相同,所以加入的少量固体为MnSO4,
故答案为:MnSO4;
③若该小组同学提出的假设成立,则反应速率加快,溶液褪色的时间小于4min,从而说明Mn2+是催化剂,
故答案为:实验4与实验1比较,溶液褪色所需时间短或:溶液褪色所用时间(t)小于4min.
故答案为:其他条件相同时,增大KMnO4浓度(或反应物浓度),反应速率增大;
(2)草酸的物质的量为:0.6mol•L-1×0.003L=0.0018mol,高锰酸钾的物质的量为:0.2mol•L-1×0.003L=0.0006mol,草酸和高锰酸钾的物质的量之比为:0.0018mol:0.0006mol=3:1,显然草酸过量,高锰酸钾完全反应,混合后溶液中高锰酸钾的浓度为:
| 0.2mol•L-1×0.003L |
| (3+2+3+2)×10-3L |
这段时间内平均反应速率v(KMnO4)=
| 0.06mol•L-1 |
| 4min |
故答案为:1.5×10-2mol•L-1•min-1或0.015 mol•L-1•min-1;
(3)①由图乙可知,反应开始后速率增大的比较快,说明生成物中的MnSO4(或Mn2+)为该反应的催化剂,
故答案为:生成物中的MnSO4为该反应的催化剂(或Mn2+对该反应有催化作用);
②与实验1作对比实验,则加入的硫酸锰的量不同,其它条件必须相同,所以加入的少量固体为MnSO4,
故答案为:MnSO4;
③若该小组同学提出的假设成立,则反应速率加快,溶液褪色的时间小于4min,从而说明Mn2+是催化剂,
故答案为:实验4与实验1比较,溶液褪色所需时间短或:溶液褪色所用时间(t)小于4min.
看了某化学兴趣小组为了研究外界条件...的网友还看了以下:
[N2O2]2-这个结构怎么写是[O=N-N=O]2-还是中心N与2个O和一个端基N相连 2020-04-06 …
如图,△ABC中,点O在边AB上,过点O作BC的平行线交∠ABC的平分线于点D,过点B作BE⊥BD 2020-04-09 …
将下面的2行5列方格纸的每一个方格染成黑色或红色,不管怎样染,至少有几列着色完全一样?为什么 2020-04-25 …
设AB为园X平方+Y平方=1上的2点O喂坐标远点A,O,B不共线求证:向量OA+向量OB与向量OA 2020-04-26 …
1,在梯形ABCD中,AD平行于BC,角BCD=90°,以CD为直径的半圆O切AB于点E,已知这个 2020-05-14 …
在平行四边形ABCD中,EF过对角线的交点O,若AD=8,AB=3,OE=2,则四边形ABFE的周 2020-05-15 …
如图,PB切⊙O于B点,直线PO交⊙O于点E,F,过点B作PO的垂线BA,垂足为点D,交⊙O于点A 2020-05-17 …
如图,射线PG平分∠EPF,O为射线PG上一点,以O为圆心10为半径作圆O,分别与∠EPF两边相交 2020-05-20 …
m物体静止于光滑斜面底用平行于斜面方向力作用物体上使沿斜面向上动当动到斜面中点撤F刚好滑行到斜面顶 2020-05-23 …
在直角坐标系中,以O,A,B,C为顶点的平行四边形的顶点O(0,0),A(1,2),C(4,0)若 2020-05-23 …