早教吧作业答案频道 -->化学-->
科研生产中常涉及碳的化合物.请回答下列问题:(1)700℃时,向容积为3L的密闭容器中充人一定量的CO和H2O,发生反应:CO(g)+H2O(g)⇌CO2(g)+H2(g),反应过程中测定的部分数据见表
题目详情
科研生产中常涉及碳的化合物.请回答下列问题:
(1)700℃时,向容积为3L的密闭容器中充人一定量的CO和H2O,发生反应:CO(g)+H2O(g)⇌CO2(g)+H2(g),反应过程中测定的部分数据见表(表中t2>t1):
①反应在t1 min内的平均速率为v(H2)=___;判定t1达平衡状态的理由是___.
②保持其他条件不变,起始时向容器中充入0.9mol CO和1.8mol H2O(g),达平衡时,CO2的物质的量浓度c(CO2)=___.
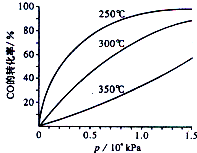
(2)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)⇌CH3OH(g).CO在不同温度下平衡转化率与压强的关系如图所示.该反应的△H___0(填“>”、“=”或“<”),实际生产条件控制在250℃,1.3×l04kPa左右,选择此压强的理由是___.
(3)CH4和H2O(g)通入聚焦太阳能反应器,发生反应:CH4(g)+H2O(g)⇌CO(g)+3H2(g),将等物质的量的CH4和H2O(g)充入2L恒容密闭反应器,某温度下反应达平衡,平衡常数值K=27,此时测得n(CO)=0.2mol,通过计算求CH4的平衡转化率(保留2位小数).

(1)700℃时,向容积为3L的密闭容器中充人一定量的CO和H2O,发生反应:CO(g)+H2O(g)⇌CO2(g)+H2(g),反应过程中测定的部分数据见表(表中t2>t1):
| 反应时间/min | N[CO(g)]mol | N[H2O(g)]mol |
| 0 | 1.8 | 0.9 |
| t1 | 1.2 | |
| t2 | y | 0.3 |
②保持其他条件不变,起始时向容器中充入0.9mol CO和1.8mol H2O(g),达平衡时,CO2的物质的量浓度c(CO2)=___.
(2)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)⇌CH3OH(g).CO在不同温度下平衡转化率与压强的关系如图所示.该反应的△H___0(填“>”、“=”或“<”),实际生产条件控制在250℃,1.3×l04kPa左右,选择此压强的理由是___.
(3)CH4和H2O(g)通入聚焦太阳能反应器,发生反应:CH4(g)+H2O(g)⇌CO(g)+3H2(g),将等物质的量的CH4和H2O(g)充入2L恒容密闭反应器,某温度下反应达平衡,平衡常数值K=27,此时测得n(CO)=0.2mol,通过计算求CH4的平衡转化率(保留2位小数).
▼优质解答
答案和解析
(1)①v(CO)=
=
mol/(L.min),速率之比等于化学计量数之比,则v(H2)=(CO)=
mol/(L.min);
t1 min时生成水的物质的量为0.3mol,与t2 min时生成水的物质的量相等,不再随时间发生变化,说明t1 min时到达平衡,
故答案为:
mol/(L.min);t1 min时生成水的物质的量为0.3mol,与t2 min时生成水的物质的量相等,不再随时间发生变化;
②CO、H2O按1:1反应,与原平衡相比二者物质的量互换,由于平衡常数不变,则平衡时二氧化碳的浓度相等,则达平衡时,CO2的物质的量浓度c(CO2)=
=0.2mol/L,
故答案为:0.2mol/L;
(2)由图可知,压强一定时,温度越高CO的转化率越小,说明升高温度平衡逆向移动,正反应为放热反应故△H<0;
在1.3×l04kPa左右,CO的转化率已经较高,再增大压强,对设备要求较高,增大成本,故选择1.3×l04kPa左右,
故答案为:<;在1.3×l04kPa左右,CO的转化率已经较高,再增大压强,对设备要求较高,增大成本;
(3)将等物质的量的CH4和H2O(g)充入2L恒容密闭反应器,某温度下反应达平衡,平衡常数值K=27,此时测得n(CO)=0.2mol,则:
CH4(g)+H2O(g)⇌CO(g)+3H2(g)
起始量(mol/L):x x 0 0
转化量(mol/L):0.1 0.1 0.1 0.3
平衡量(mol/L):x-0.1 x-0.1 0.1 0.3
故
=27,解得x=0.11,
则CH4的平衡转化率为
×100%≈90.91%,
答:CH4的平衡转化率为90.91%.
| ||
| t1min |
| 0.2 |
| t1 |
| 0.2 |
| t1 |
t1 min时生成水的物质的量为0.3mol,与t2 min时生成水的物质的量相等,不再随时间发生变化,说明t1 min时到达平衡,
故答案为:
| 0.2 |
| t1 |
②CO、H2O按1:1反应,与原平衡相比二者物质的量互换,由于平衡常数不变,则平衡时二氧化碳的浓度相等,则达平衡时,CO2的物质的量浓度c(CO2)=
| 1.8mol-1.2mol |
| 3L |
故答案为:0.2mol/L;
(2)由图可知,压强一定时,温度越高CO的转化率越小,说明升高温度平衡逆向移动,正反应为放热反应故△H<0;
在1.3×l04kPa左右,CO的转化率已经较高,再增大压强,对设备要求较高,增大成本,故选择1.3×l04kPa左右,
故答案为:<;在1.3×l04kPa左右,CO的转化率已经较高,再增大压强,对设备要求较高,增大成本;
(3)将等物质的量的CH4和H2O(g)充入2L恒容密闭反应器,某温度下反应达平衡,平衡常数值K=27,此时测得n(CO)=0.2mol,则:
CH4(g)+H2O(g)⇌CO(g)+3H2(g)
起始量(mol/L):x x 0 0
转化量(mol/L):0.1 0.1 0.1 0.3
平衡量(mol/L):x-0.1 x-0.1 0.1 0.3
故
| 0.1×0.33 |
| (x-0.1)×(x-0.1) |
则CH4的平衡转化率为
| 0.1mol/L |
| 0.11mol/L |
答:CH4的平衡转化率为90.91%.
看了科研生产中常涉及碳的化合物.请...的网友还看了以下:
为什么共价化合物最外层不是8个电子例如NO2一个O的最外层只有7个好像.在什么前提下会发生呢? 2020-04-08 …
22.09(时间)怎么读?Itistennine/tenO(欧)nine/tenzeronine? 2020-05-12 …
经过同一点O的三条直线a,b,c与另一条不经过点O的直线l分别交于点A,B,C,求证:这四条直线共 2020-05-13 …
一块长为L的板可绕过其一端O的水平轴转动,一开始板处于水平位置,在板正中间有一小物体.现使板突然以 2020-05-13 …
一道化学题,帮忙解答一下SiO2+4HF----SiF4+2 H2 O这个已经配平了是吧,然后问题 2020-05-13 …
已知:AB=CD,AD=BC,过BD上一点O的直线分别交DA、BC的延长线于E、F,求证:1.∩E 2020-05-20 …
含一个O的单词O在第二位比如pot越多越好 2020-06-02 …
已知A为⊙O上一点,⊙O的半径为1,该平面上另有一点P,PA=根号3,那么点P与⊙O有怎样 2020-06-04 …
求化学式子(就是比较简单那种!)比如H2+O=H2O什么的,不需要很复杂 2020-06-06 …
关于氢气纯度测量的问题,H2在CO2中和H2在Air中,仪表有两个选择,制氢后,测纯度一般用的H2 2020-06-06 …