铬是一种银白色金属化学性质稳定,以+2、+3和+6价为常见价态。工业上以铬铁矿(主要成分为FeO·Cr2O3,含有Al2O3、SiO2等杂质)为主要原料生产金属铬和重铬酸钠(Na2Cr2O7·2H2O),其
铬是一种银白色金属 化学性质稳定,以+2、+3和+6价为常见价态。工业上以铬铁矿(主要成分为FeO·Cr2O3,含有Al2O3、SiO2等杂质)为主要原料生产金属铬和重铬酸钠(Na2Cr2O7·2H2O),其主要工艺流程如下:
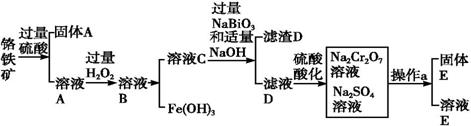
已知:①Na2Cr2O7是一种强氧化剂
②常温下,NaBiO3不溶于水,有强氧化性,在碱性条件下,能将Cr3+转化为CrO42—
⑴工业上常采用热还原法制备金属铬,写出以Cr2O3为原料,利用铝热反应制取金属铬的化学方程式:
⑵酸化滤液D时,不选用盐酸的原因是
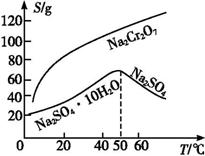
⑶固体E的主要成分是Na2SO4,根据下图分析操作a为
⑷已知含+6价铬的污水会污染环境。电镀厂产生的镀铜废水中往往含有一定量的Cr2O72—,处理该废水常用还原沉淀法,具体流程如下:

①Cr(OH)3的化学性质与Al(OH)3相似。在上述生产过程中加入NaOH溶液时要控制溶液的pH不能过高,是因为
②下列溶液中可以代替上述流程中Na2S2O3溶液的是 (填选项序号)
A.FeSO4溶液 B.浓H2SO4 C.酸性KMnO4溶液 D.Na2SO3溶液
③上述流程中,每消耗0.1molNa2S2O3转移0.8mole—,则加入Na2S2O3溶液时发生反应的
离子方程式为
⑸根据有关国家标准,含CrO42—的废水要经化学处理,使其浓度降至5.0×10—7mol·L—1以下才能排放。用以下方法处理废水:加入可溶性钡盐生成BaCrO4沉淀,再加入可溶性硫酸盐处理多余的Ba2+。则加入可溶性钡盐后的废水中Ba2+的浓度应不小于
mol·L—1,废水处理后方能达到国家排放标准。
L病毒侵染小鼠的脑膜细胞,引起脑膜炎,L蛋白是L病毒的抗原蛋白.科研人员将两只转基因小鼠进行杂交, 2020-06-11 …
下列四组中,物质组成相同的是()A.染色体和噬菌体B.肌细胞和大肠杆菌C.银杏和白细胞D.红细胞和 2020-07-17 …
L病毒侵染小鼠的脑膜细胞,引起脑膜炎,L蛋白是L病毒的抗原蛋白.科研人员将两只转基因小鼠进行杂交, 2020-07-25 …
人们往往把货币等同于金银,为什么说金银天然不是货币?作为贵重金属,不只是黄金和白银,像水银、钨、锰 2020-07-28 …
白斑银狐是银狐的一个突变种,用白斑银狐的皮毛制成的大衣可谓“千金裘”.白斑银狐与银狐的杂交后代中,总 2020-11-03 …
这些CP英文是什么?每个人名字第一个字母.如佐鸣是SN(佐SASUKE鸣NARUTO)宁鹿是NS.蝎 2020-11-07 …
某研究小组以银盐为实验对象,研究难溶盐时进行了如下实验:①0.1mol•L-1AgNO3溶液和0.1 2020-12-04 …
初二关于密度的物理题..如何鉴别银子和白金(用密度来的话..)水变成冰后体积为什么会变大(用密度来的 2020-12-08 …
清末墨西哥银元和白银的换算《南京条约》中,清政府赔偿英国2100万银圆(墨西哥银圆),想知道它和当时 2020-12-08 …
银杏和白果真的是一样的吗 2021-04-13 …